Čtverná vazba
Čtverná vazba je chemická vazba mezi dvěma atomy, které se účastní osm elektronů; jedná se o jakési rozšíření běžněji se vyskytujících typů, dvojné a trojné vazby[1] Stabilní čtverné vazby se nejčastěji objevují u přechodných kovů z prostřední části bloku d, jako jsou rhenium, wolfram, molybden a chrom. Ligandy, u kterých se může vyskytnout tento typ vazby, jsou obvykle donory π elektronů, nikoliv jejich akceptory.

Historie
První známou sloučeninou se čtvernou vazbou byl octan chromnatý (Cr2(μ-O2CCH3)4(H2O)2). Poprvé jej připravil roku 1844 Eugène-Melchior Péligot, ovšem čtverná vazba v něm byla nalezena až o století později.[2]
První krystalografické studie sloučenin se čtvernou vazbou byly provedeny u solí aniontu Re2Cl 2-
8 ; [3] byly zde popsány malé délky vazeb (a diamagnetické vlastnosti látky), což naznačovalo vazby mezi atomy rhenia. Uvedený anion byl mylně považován za anion dvojmocného rhenia, z čehož vyplynul původně navržený vzorec Re2Cl 4-
8 .
Krátce poté byla popsána krystalová struktura oktachlordirhenitanu draselného (K2[Re2Cl8]·2H2O).[4] Tato analýza odhalila chyby předchozích studií.[2] Délka vazby Re-Re v této sloučenině je pouze 224 pm; v teorii molekulových orbitalů se popisuje jako σ2π4δ2. tedy spojení jedné vazby sigma, dvou vazeb pí a jedné vazby delta.
Struktura
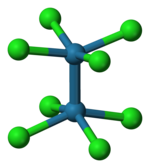

Iont Re2Cl 2-
8 se vyskytuje v zákrytové konformaci (viz obrázek vlevo). Vazebný orbital delta vzniká překryvem dvou orbitalů d jednotlivých atomů rhenia; tyto orbitaly jsou v poloze kolmé na osu Re-Re a nacházejí se mezi vazbami Re-Cl. Orbitaly d podél vazeb Re-Cl jsou stabilizovány interakcemi s orbitaly chlorových ligandů a nezapojují se do vazby Re-Re.[5] Iont Os2Cl 2-
8 , který má o dva elektrony více (σ2π4δ2δ*2) oproti tomu má mezi atomy osmia trojnou vazbu a vyskytuje se v nezákrytové konformaci.[5]
Bylo popsáno mnoho dalších sloučenin se čtvernými vazbami, například oktachlordimolybdenatan draselný (K4[Mo2Cl8])[6] a tetrakis(hexahydropyrimidinopyrimidin)diwolfram.
U prvků bloku s a bloku p nejsou sloučeniny se čtvernými vazbami známy. Podle teorie molekulových orbitalů se v sigma systému nacházejí dvě skupiny spárovaných elektronů (vazebná a protivazebná) a dvě skupiny spárovaných elektronů v degenerovaném vazebném orbitalu π, což dává řád vazby 2, což naznačuje, že v dvouatomové molekule uhlíku (C2) je dvojná vazba. Z diagramu molekulových orbitalů vyplývá, že vazba v C2 skládá z&dvou vazeb pí a vazby sigma zde nejsou přítomny. Byla však vydána práce, podle které je v uvedené molekule čtverná vazba.[7]
Odkazy
Související články
Reference
V tomto článku byl použit překlad textu z článku Quadruple bond na anglické Wikipedii.
- ↑ U. Radius; F. Breher. To Boldly Pass the Metal–Metal Quadruple Bond. Angewandte Chemie International Edition. 2006, s. 3006–3010. (anglicky)
- ↑ a b Frank Albert Cotton; R.A. Walton. Multiple Bonds Between Metal Atoms. Oxford: Oxford University Press, 1993. Dostupné online. ISBN 0-19-855649-7. (anglicky)
- ↑ Kuznetsov, V. G.; Koz'min, P. A. "The structure of (pyH)HReCl4" Zhurnal Strukturnoi Khimii 1963, 4, 55-62.
- ↑ Frank Albert Cotton; C.B. Harris. The Crystal and Molecular Structure of Dipotassium Octachlorodirhenate(III) Dihydrate, K2[Re2Cl8]·2H2O. Inorganic Chemistry. 1965, s. 330–333. (anglicky)
- ↑ a b G.L. Miessler; D.A. Tarr. Inorganic Chemistry. [s.l.]: Prentice-Hall, 1999. (2). Dostupné online. ISBN 0-13-841891-8. S. 531. (anglicky)
- ↑ G.S. Girolami; T.B. Rauchfuss; R.J. Angelici. Synthesis and Technique in Inorganic Chemistry. [s.l.]: University Science Books, 1999. Dostupné online. ISBN 0935702482. S. 531. (anglicky)
- ↑ Sason Shaik; David Danovich; Wei Wu; Peifeng Su; Henry S. Rzepa; Philippe C. Hiberty. Quadruple bonding in C2 and analogous eight-valence electron species. Nature Chemistry. 2012, s. 195–200. Bibcode 2012NatCh...4..195S. (anglicky)
Média použitá na této stránce
Ball-and-stick model of a chromium(II) acetate hydrate dimer, [Cr2(OAc)4(H2O)2].
Colour code:
- Chromium, Cr: blue-grey
- Carbon, C: grey
- Hydrogen, H: white
- Oxygen, O: red
Boundary surface diagram of the formation of a delta bond (bonding molecular orbital with δ symmetry) from two d orbitals


