(Diacetoxyjod)benzen
| (Diacetoxyjod)benzen | |
|---|---|
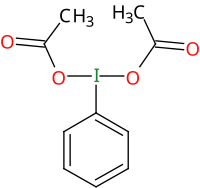 Strukturní vzorec | |
| Obecné | |
| Systematický název | fenyl-λ3-jodandiyldiacetát |
| Sumární vzorec | C10H11IO4 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 3240-34-4 |
| EC-no (EINECS/ELINCS/NLP) | 221-808-1 |
| PubChem | 76724 |
| SMILES | CC(=O)OI(C1=CC=CC=C1)OC(=O)C |
| InChI | 1S/C10H11IO4/c1-8(12)14-11(15-9(2)13)10-6-4-3-5-7-10/h3-7H,1-2H3 |
| Vlastnosti | |
| Molární hmotnost | 322,79 g/mol |
| Teplota tání | 163 až 165 °C (436 až 438 K) |
| Rozpustnost ve vodě | reaguje |
| Rozpustnost v polárních rozpouštědlech | rozpustný v acetonitrilu a kyselině octové |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v dichlormethanu |
| Bezpečnost | |
| [1] | |
| H-věty | H302 H312 H315 H319 H335[1] |
| P-věty | P261 P264 P264+265 P270 P271 P280 P301+317 P302+352 P304+340 P305+351+338 P317 P319 P321 P330 P332+317 P337+317 P362+364 P403+233 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
(Diacetoxyjod)benzen je organická sloučenina obsahující hypervalentní jod, se vzorcem C6H5I(OCOCH3)2. Používá se v organické syntéze jako oxidační činidlo.
Příprava
První přípravu této sloučeniny provedl Conrad Willgerodt[2] reakcí jodbenzenu se směsí kyseliny octové a peroctové:[3][4]
- C6H5I + CH3CO3H + CH3CO2H → C6H5I(O2CCH3)2 + H2O
Další možností je působení koncentrované kyseliny octové na jodosobenzen:[4]
- C6H5IO + 2 CH3CO2H → C6H5I(O2CCH3)2 + H2O
Byly popsány přímé přípravy z jodu, kyseliny octové a benzenu, s využitím dihydrogenboritanu sodného[5] nebo peroxodisíranu draselného jako oxidačního činidla:[6][7]
Struktura
Tato sloučenina patří mezi hypervalentní, protože její atom jodu má oxidační číslo +III a vyšší počet kovalentních vazeb, než je běžné.[8]
Molekula má tvar písmene T, kde fenylová skupina zaujímá jednu ze tří ekvatoriálních pozic v trigonální bipyramidě (zbylé dvě obsazují volné elektronové páry) a v axiálních pozicích jsou atomy kyslíku acetátových skupin. Tvar T je mírně narušen, takže úhly mezi vazbami fenyl-C a I-acetátový kyslík jsou menší než 90°.[9]
Krystalová struktura je kosočtverečná s prostorovou grupou Pnn2.[9][10] Délky vazeb z atomu jodu činí 208 pm u vazby na fenylový uhlík a 215,6 pm u vazby na acetátový kyslík. Narušení geometrie způsobuje přítomnost molekul vody, které vyvolávají dvě slabší mezimolekulové interakce mezi atomy jodu a kyslíku.[10]
Neobvyklé reakce
(Diacetoxyjod)benzen se používá na přípravu podobných činidel substitucemi na acetátových skupinách; například z něj lze získat (bis(trifluoracetoxy)jod)benzen zahříváním v kyselině trifluoroctové:[11][7]

Bis(trifluoracetoxy)jod)benzen může umožnit provedení Hofmannova přesmyku v mírně kyselém prostředí[12] namísto běžně používaných silně zásaditých podmínek.[13][14] Hofmannovu dekarboxylaci asparaginu chráněného na atomu dusíku je možné využít na přípravu β-aminoderivátů L-alaninu.[15]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku (Diacetoxyiodo)benzene na anglické Wikipedii.
- ↑ a b c https://pubchem.ncbi.nlm.nih.gov/compound/76724
- ↑ C. Willgerodt. Zur Kenntniss aromatischer Jodidchloride, des Jodoso- und Jodobenzols. Chemische Berichte. 1892, s. 3494–3502. Dostupné online. DOI 10.1002/cber.189202502221.
- ↑ SHAREFKIN, J. G.; SALTZMAN, H. Iodosobenzene Diacetate. Org. Synth.. 1963, s. 62. Dostupné online. DOI 10.15227/orgsyn.043.0062. (anglicky); Coll. Vol.. S. 660. (anglicky)
- ↑ a b Robert M. Moriarty; Calvin J. Chany; Jerome W. Kosmeder; Justin Du Bois. Encyclopedia of Reagents for Organic Synthesis. [s.l.]: John Wiley & Sons, 2001. ISBN 9780470842898. DOI 10.1002/047084289x.rd005m.pub2. Kapitola (Diacetoxyiodo)benzene.
- ↑ Md. Delwar Hossain; Tsugio Kitamura. Unexpected, Drastic Effect of Triflic Acid on Oxidative Diacetoxylation of Iodoarenes by Sodium Perborate. A Facile and Efficient One-Pot Synthesis of (Diacetoxyiodo)arenes. The Journal of Organic Chemistry. 2005, s. 6984–6986. DOI 10.1021/jo050927n. PMID 16095332.
- ↑ Md. Delwar Hossain; Tsugio Kitamura. New and Direct Approach to Hypervalent Iodine Compounds from Arenes and Iodine. Straightforward Synthesis of (Diacetoxyiodo)arenes and Diaryliodonium Salts Using Potassium μ-Peroxo-hexaoxodisulfate. Bulletin of the Chemical Society of Japan. 2007, s. 2213–2219. DOI 10.1246/bcsj.80.2213.
- ↑ a b Toshifumi Dohi; Yasuyuki Kita. Iodine Chemistry and Applications. Příprava vydání Tatsuo Kaiho. [s.l.]: John Wiley & Sons, 2015. ISBN 9781118878651. Kapitola Oxidizing Agents, s. 277–302.
- ↑ Toshifumi Dohi; Yasuyuki Kita. Iodine Chemistry and Applications. Příprava vydání Tatsuo Kaiho. [s.l.]: John Wiley & Sons, 2015. ISBN 9781118878651. Kapitola Hypervalent Iodine, s. 103–158.
- ↑ a b Chow-Kong Lee; Thomas C. W. Mak; Wai-Kee Li; John F. Kirner. Iodobenzene diacetate. Acta Crystallographica B. 1977, s. 1620–1622. DOI 10.1107/S0567740877006694.
- ↑ a b Nathaniel W. Alcock; Rachel M. Countryman; Esperås Steinar; Jeffery F. Sawyer. Secondary bonding. Part 5. The crystal and molecular structures of phenyliodine(III) diacetate and bis(dichloroacetate). Journal of the Chemical Society, Dalton Transactions. 1979, s. 854–860. DOI 10.1039/DT9790000854.
- ↑ ALMOND, M. R.; STIMMEL, J. B.; THOMPSON, E. A.; LOUDON, G. M. Hofmann Rearrangement Under Mildly Acidic Conditions Using [I,I-Bis(Trifluoroacetoxy)]Iodobenzene: Cyclobutylamine Hydrochloride from Cyclobutanecarboxamide. Org. Synth.. 1988, s. 132. Dostupné online. DOI 10.15227/orgsyn.066.0132. (anglicky); Coll. Vol.. S. 132. (anglicky)
- ↑ AUBÉ, Jeffrey; FEHL, Charlie; LIU, Ruzhang; MCLEOD, Michael C.; MOTIWALA, Hashim F. Heteroatom Manipulations. [s.l.]: [s.n.], 2014. (Comprehensive Organic Synthesis II; sv. 6). ISBN 9780080977430. DOI 10.1016/B978-0-08-097742-3.00623-6. Kapitola 6.15 Hofmann, Curtius, Schmidt, Lossen, and Related Reactions, s. 598–635. (anglicky)
- ↑ WALLIS, Everett S.; LANE, John F. The Hofmann Reaction. Organic Reactions. 1946, s. 267–306. DOI 10.1002/0471264180.or003.07. (anglicky)
- ↑ SURREY, Alexander R. Name Reactions in Organic Chemistry. 2nd. vyd. [s.l.]: Academic Press, 1961. ISBN 9781483258683. Kapitola Hofmann Reaction, s. 134–136. (anglicky)
- ↑ ZHANG, Lin-hua; KAUFFMAN, Goss S.; PESTI, Jaan A.; YIN, Jianguo. Rearrangement of Nα-Protected L-Asparagines with Iodosobenzene Diacetate. A Practical Route to β-Amino-L-alanine Derivatives. The Journal of Organic Chemistry. 1997, s. 6918–6920. DOI 10.1021/jo9702756. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu (Diacetoxyjod)benzen na Wikimedia Commons
Obrázky, zvuky či videa k tématu (Diacetoxyjod)benzen na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Reaction of (bisacetoxyiodo)benzene with trifluoroacetic acid gives (Bis(trifluoroacetoxy)iodo)benzene by exchange of the ester groups
Autor: tpa2067, Licence: CC BY-SA 3.0
Structure of (diacetoxyiodo)benzene or phenyliodosodiacetate



