1,8-bis(dimethylamino)naftalen
| 1,8-bis(dimethylamino)naftalen | |
|---|---|
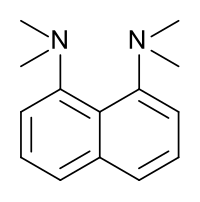 Strukturní vzorec | |
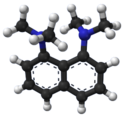
 Model molekuly | |
| Obecné | |
| Systematický název | N1,N1,N8,N8-tetramethylnaftalen-1,8-diamin |
| Ostatní názvy | N,N,N',N'-tetramethylnaftalen-1,8-diamin |
| Funkční vzorec | C10H6[N(CH3)2]2 |
| Sumární vzorec | C14H18N2 |
| Vzhled | bílý krystalický prášek |
| Identifikace | |
| Registrační číslo CAS | 106-23-0 |
| EC-no (EINECS/ELINCS/NLP) | 203-376-6 |
| PubChem | 88675 |
| SMILES | CN(C)C1=CC=CC2=C1C(=CC=C2)N(C)C |
| InChI | InChI=1S/C14H18N2/c1-15(2)12-9-5-7-11-8-6-10-13(14(11)12)16(3)4/h5-10H,1-4H3 |
| Vlastnosti | |
| Molární hmotnost | 214,31 g/mol |
| Teplota tání | 47,8 °C (321,0 K) |
| Rozpustnost ve vodě | 3,12 mg/100 ml[1] |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H301 H302 H315 H319 H335[1] |
| P-věty | P261 P264 P270 P271 P280 P301+310 P301+312 P302+352 P304+340 P305+351+338 P312 P321 P330 P332+313 P337+313 P362 P403+233 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
1,8-Bis(dimethylamino)naftalen, triviálním názvem protonová houba je organická sloučenina se vzorcem C10H6[N(CH3)2]2. Patří mezi perinaftaleny, 1,8-disubstituované deriváty naftalenu. Díky své neobvyklé struktuře je velmi silnou zásadou.
Struktura a vlastnosti
Tato látka je diaminem s dvěma dimethylaminovými skupinami navázanými na stejnou stranu (v poloze peri) na molekulu naftalenu. Vykazuje neobvykle silnou zásaditost a má též zajímavé spektroskopické vlastnosti.
S pKa 12,34[2] u konjugované kyseliny ve vodném roztoku je 1,8-bis(dimethylamino)naftalen jednou z nejsilnějších organických zásad. Takováto zásaditost je způsobována snížením napětí při protonaci a silnými interakcemi mezi volnými elektronovými páry na atomech dusíku.[3] Mnoho aromatických aminů má zásaditost naopak omezenou kvůli sp2 hybridizaci orbitalů dusíku, jehož volný pár zaujímá orbital 2p, interaguje s aromatickým jádrem a je z něj vytlačen. Toto u 1,8-bis(dimethylamino)naftalenu není možné, kvůli methylovým skupinám zabraňujícím molekule přejít do rovinného tvaru, ke kterému by bylo třeba tyto methylové skupiny odstranit a zásaditost tak není omezována vlivem, který se uplatňuje u jiných molekul. V molekule se vyskytují sterické efekty; díky jejich přítomnosti a současně silné zásaditosti se 1,8-bis(dimethylamino)naftalen používá v organické syntéze jako velmi selektivní nenukleofilní zásada.[2]
Tato látka má také vysokou afinitu k boru a může odštěpovat hydridové skupiny z boranu za vzniku párů boroniových a borohydridových iontů.[4]
Příprava
1,8-Bis(dimethylamino)naftalen lze zakoupit, dá se rovněž připravit methylací 1,8-diaminonaftalenu jodmethanem nebo dimethylsulfátem.[5]
Reference
V tomto článku byl použit překlad textu z článku 1,8-Bis(dimethylamino)naphthalene na anglické Wikipedii.
- ↑ a b c d e 1,8-Bis(dimethylamino)naphthalene. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ a b Alexander F. Pozharskii and Valery A. Ozeryanskii „Proton sponges and hydrogen transfer phenomena“ Mendeleev Commun., 2012, 22, 117–124. doi:10.1016/j.mencom.2012.05.001
- ↑ R. W. Alder. Strain effects on amine basicities. Chemical Reviews. 1989, s. 1215–1223. DOI 10.1021/cr00095a015.
- ↑ Marc-André Légaré; Marc-André Courtemanche; Frédéric-Georges Fontaine. Lewis base activation of borane–dimethylsulfide into strongly reducing ion pairs for the transformation of carbon dioxide to methoxyboranes. Chemical Communications. 2014-08-28. Dostupné online. ISSN 1364-548X. DOI 10.1039/c4cc04857a.
- ↑ Vladimir I. Sorokin; Valery A. Ozeryanskii; Alexander F. Pozharskii. A Simple and Effective Procedure for the N-Permethylation of Amino-Substituted Naphthalenes. European Journal of Organic Chemistry. 2003, s. 496. DOI 10.1002/ejoc.200390085.
Externí odkazy
 Obrázky, zvuky či videa k tématu 1,8-bis(dimethylamino)naftalen na Wikimedia Commons
Obrázky, zvuky či videa k tématu 1,8-bis(dimethylamino)naftalen na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
chemical structure of 1,8-Bis(dimethylamino)naphthalene (aka proton sponge), made using BKchem
Ball-and-stick model of the Proton Sponge molecule, 1,8-bis(dimethylamino)naphthalene, C14H18N2, as found in the crystal structure.
Colour code:
- Carbon, C: grey-black
- Hydrogen, H: white
- Nitrogen, N: blue
Structure by X-ray crystallography from J. Am. Chem. Soc. (1999). 121, 4640-4646.
Model constructed in CrystalMaker 8.3.
Image generated in Accelrys DS Visualizer.