2,3-dichlor-5,6-dikyano-1,4-benzochinon
| 2,3-dichlor-5,6-dikyano-1,4-benzochinon | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | 4,5-dichlor-3,6-dioxocyklohexa-1,4-dien-1,2-dikarbonitril |
| Ostatní názvy | 2,3-dichlor-5,6-dikyan-1,4-benzochinon |
| Funkční vzorec | C6(CN)2O2Cl2 |
| Sumární vzorec | C8N2O2Cl2 |
| Vzhled | žlutý až oranžový prášek |
| Identifikace | |
| Registrační číslo CAS | 84-58-2 |
| EC-no (EINECS/ELINCS/NLP) | 201-542-2 |
| PubChem | 6775 |
| SMILES | ClC=1C(=O)C(\C#N)=C(\C#N)C(=O)C=1Cl |
| InChI | InChI=1S/C8Cl2N2O2/c9-5-6(10)8(14)4(2-12)3(1-11)7(5)13 |
| Číslo RTECS | GU4825000 |
| Vlastnosti | |
| Molární hmotnost | 227,00 g/mol |
| Teplota tání | 210 až 215 °C (483 až 488 K) |
| Teplota varu | 301,8 °C (575,0 K) |
| Hustota | 1,7 g/cm3 |
| Rozpustnost ve vodě | reaguje |
| Bezpečnost | |
| [1] | |
| H-věty | H301 H317 H319[1] |
| P-věty | P261 P264 P270 P272 P280 P301+310 P302+352 P305+351+338 P321 P330 P333+313 P337+313 P363 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
2,3-dichlor-5,6-dikyano-1,4-benzochinon je organická sloučenina se vzorcem C6Cl2(CN)2O2. Používá se jako oxidační činidlo při dehydrogenacích alkoholů,[2] fenolů[3] a ketonů.[4]
Ve vodě se rozkládá, ve vodných roztocích anorganických kyselin je však stálý.[5]
Příprava
2,3-dichlor-5,6-dikyano-1,4-benzochinon se připravuje postupem zahrnujícím kyanací chloranilu. Jeho šestikrokovou přípravu popsali J. Thiele a F. Günther v roce 1906.[6] Sloučenina nebyla významným předmětem zájmu, dokud nebylo objeveno její možné využití k dehydrogenacím. Roku 1965 byla oznámena jednokroková příprava z 2,3-dikyanohydrochinonu.[7]
Reakce
Tato látka odštěpuje dvojice atomů vodíku z organických molekul; jako příklad může být uvedena přeměna tetralinu na naftalen:
- 2 C6Cl2(CN)2O2 + C10H12 → 2 C6Cl2(CN)2(OH)2 + C10H8
Vzniklý hydrochinon se špatně rozpouští v rozpouštědlech, která se při reakci obvykle používají (dioxanu, benzenu či alkanech).
Její roztoky v benzenu jsou v důsledku tvorby elektron-donor-akceptorových komplexů červené.[8]
Dehydrogenace
Aromatizace
Dehydrogenační párování
Bezpečnost
2,3-dichlor-5,6-dikyano-1,4-benzochinon reaguje s vodou za vývinu vysoce toxického kyanovodíku (HCN). Jeho stabilitu lze zlepšit snížením teploty a mírným okyselením.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku 2,3-Dichloro-5,6-dicyano-1,4-benzoquinone na anglické Wikipedii.
- ↑ a b c https://pubchem.ncbi.nlm.nih.gov/compound/6775
- ↑ E. A. Braude; R. P. Linstead; K. R. H. Wooldridge. Hydrogen Transfer. Part IX The Selective Dehydrogenation of Unsaturated Alcohols by High-potential Quinones. Journal of the Chemical Society. 1956, s. 3070–3074. doi:10.1039/JR9560003070.
- ↑ H. D. Becker. Quinone Dehydrogenation. I. Oxidation of Monohydric Phenols. Journal of Organic Chemistry. 1965, s. 982–989. doi:10.1021/jo01015a006.
- ↑ A. B. Turner; H. J. Ringold. Applications of High-potential Quinones. Part I. The Mechanism of Dehydrogenation of Steroidal Ketones by 2,3-Dichloro-5,6-Dicyanobenzoquinone. Journal of the Chemical Society C: Organic. 1967, s. 1720–1730. doi:10.1039/J39670001720.
- ↑ Derek R. Buckle, Steven J. Collier, Mark D. McLaws "2,3-Dichloro-5,6-dicyano-1,4-benzoquinone" in E-EROS ENCYCLOPEDIA OF REAGENTS FOR ORGANIC SYNTHESIS, 2005. doi:10.1002/047084289X.rd114.pub2
- ↑ J. Thiele; F. Günther. Ueber Abkömmlinge des Dicyanhydrochinons. Justus Liebig's Annalen der Chemie. 1906, s. 45–66. Dostupné online. doi:10.1002/jlac.19063490103.
- ↑ D. Walker; T. D. Waugh. 2,3-Dichloro-5,6-Dicyanobenzoquinone (DDQ). A New Preparation. The Journal of Organic Chemistry. 1965, s. 3240. doi:10.1021/jo01020a529.
- ↑ Rajendra Rathore; Jay K. Kochi. Donor/acceptor organizations and the electron-transfer paradigm for organic reactivity. Advances in Physical Organic Chemistry. 2000, s. 193–318. ISBN 9780120335350. doi:10.1016/s0065-3160(00)35014-6.
- ↑ W. Brown; A. B. Turner. Application of High-potential Quinones. 7. Synthesis of Steroidal Phenanthrenes by Double Methyl Migration. Journal of the Chemical Society C: Organic. 1971, s. 2566–2572. doi:10.1039/J39710002566. PMID 5167256.
- ↑ Y. Zhang; C. J. Li. DDQ-Mediated Direct Cross-Dehydrogenative-Coupling (CDC) between Benzyl Ethers and Simple Ketones. Journal of the American Chemical Society. 2006, s. 4242–4243. doi:10.1021/ja060050p. PMID 16568995.
Externí odkazy
 Obrázky, zvuky či videa k tématu 2,3-dichlor-5,6-dikyan-1,4-benzochinon na Wikimedia Commons
Obrázky, zvuky či videa k tématu 2,3-dichlor-5,6-dikyan-1,4-benzochinon na Wikimedia Commons - "Like Neurons in the Brain": A Molecular Computer that Evolves
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
dehydrogenation reaction use ddq
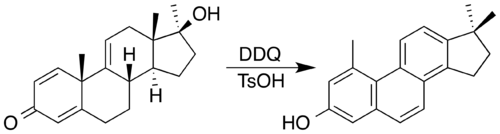
Skeletal structures for the aromatization/double-methyl-migration (Wagner–Meerwein rearrangement) of a testosterone derivative into a phenanthrene using DDQ and TsOH.
Autor: Jynto (talk), Licence: CC0
Space-filling model of the dichlorodicyanobenzoquinone molecule, also known as DDQ.
Color code:
- Carbon, C: black
- Oxygen, O: red
- Nitrogen, N: blue
- Chlorine, Cl: green
OXIDATION with ddq
Structure of Dichlorodicyanobenzoquinone; Dichlorodicyanoquinone; 2,3-Dichloro-5,6-dicyano-1,4-benzoquinone; 2,3-Dichloro-5,6-dicyanobenzoquinone
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances