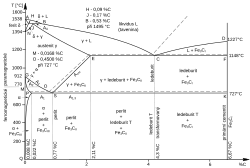
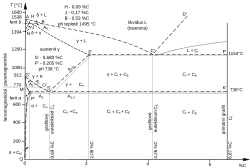
Binární diagram železo-uhlík
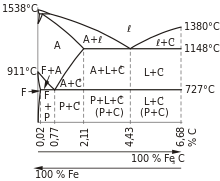
A – austenit, F – ferit, P – perlit, L – ledeburit, C – cementit, ℓ – tavenina (likvidus)
Binární diagram železo-uhlík popisuje rovnovážný binární systém, ve kterém lze v závislosti na obsahu uhlíku a teplotě odečíst fázové a strukturní přeměny ve slitině železo-uhlík, tj. technickém železe. Kromě železa v převažující koncentraci a uhlíku jsou v technickém železe obsaženy ještě další žádoucí prvky, jako jsou např. mangan, křemík atd., ale i nežádoucí, zejména fosfor a síra. Nejdůležitější prvek – kromě železa – obsažený ve slitině je uhlík, jehož i malé změny koncentrace mají zásadní dopad na vlastnosti materiálu. Jako oceli se označují slitiny do obsahu 2,14 %[zdroj?!] uhlíku,[pozn. 1] nad tuto koncentraci se slitiny železo-uhlík označují jako surová železa nebo litiny.
Podle formy vyloučení uhlíku se rozlišují dva typy rovnovážného binárního diagramu železo-uhlík: buď diagram metastabilní soustavy Fe-Fe3C nebo diagram stabilní soustavy Fe-C. Diagram metastabilní soustavy, ve které je uhlík vyloučen jako karbid železa Fe3C (někdy též cementit), se používá pro oceli a bílou litinu. Diagram stabilní soustavy, ve které je uhlík vyloučen v elementární formě, tj. jako grafit, se používá pro šedé litiny.
Rovnovážný diagram je relevantní pouze při velmi pomalém ochlazování slitiny, kdy se rychlost ochlazování limitně blíží nule. Při vyšších rychlostech ochlazování je nutné použít diagramy izotermického rozpadu austenitu (IRA) nebo anizotermického rozpadu austenitu (ARA).
Alotropické modifikace čistého železa
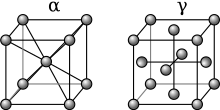
Čisté železo se vyskytuje v několika alotropických modifikacích. Železem α se nazývá kubická prostorově středěná struktura železa, která je stabilní do teploty 911 °C a nad 1392 °C. Železo α je feromagnetické až do teploty 769 °C, tzv. Curieovy teploty.[1][2] Nad touto teplotou se někdy označuje jako železo β. Velikost hrany atomové mřížky železa je závislá na teplotě a v případě nízkoteplotního železa α (β) je maximální rozměr 2,9×10−10 m.[3] Železo γ je kubická plošně středěná struktura železa, která je stálá mezi teplotami 911 °C a 1392 °C.[1][2] Železo γ, stejně jako železo β, je již paramagnetické.[4] Hrana atomové mřížky železa γ je větší než u železa α s rozměrem přibližně 3,65×10−10 m.[3] Vysokoteplotní modifikace železa α (nad 1392 °C) se často označuje jako železo δ.[1]
Strukturní fáze slitin železo-uhlík
Uhlík je jedním z prvků, které umožňují vytvářet s železem tzv. intersticiální tuhý roztok,[pozn. 2] kdy se atomy uhlíku vtěsnají do prostoru mezi atomy železa. Rozdílný typ a velikost atomové mřížky má vliv mj. i na rozdílnou rozpustnost uhlíku v jednotlivých modifikacích železa.[3][2][5] Tuhý roztok uhlíku v železe α se nazývá ferit α nebo jenom ferit s maximální rozpustností 0,02 % uhlíku při teplotě 727 °C. Paramagnetická fáze feritu se označuje jako ferit β. Tuhý roztok uhlíku v železe γ se nazývá austenit s rozpustností až do 2,11 %. Uhlík v železe δ tvoří tzv. ferit δ, ve kterém je rozpustnost uhlíku maximálně 0,10 % při teplotě 1499 °C.[3][6]
Při obsahu uhlíku nad mezí rozpustnosti tvoří uhlík v železe samostatné fáze buď jako metastabilní soustava se železem, tzv. karbidem železa Fe3C – cementitem, nebo jako stabilní soustava s tzv. volným uhlíkem C – grafitem.[4][7][8]
V eutektoidních ocelích – s obsahem uhlíku právě 0,765 % – se při chladnutí z austenitu tvoří lamelární eutektoid tzv. perlit, což je směs 88,5 % feritu a 11,5 % cementitu.[9][10] Eutektikum, tj. eutektická litina nebo surové železo,[9] se při obsahu 4,3 % uhlíku nazývá ledeburit.[4] Je tvořen zrny austenitu o obsahu 2,11 % uhlíku a cementitu o obsahu 6,68 % uhlíku při teplotě 1148 °C. Při chladnutí se austenit rozpadá na perlit a cementit: tato směs perlitu v základním cementitu se často označuje jako tzv. rozpadlý ledeburit nebo transformovaný ledeburit.[11]
Grafitové eutektikum je směs krystalů austenitu s lupínkovým grafitem, která vzniká při teplotě 1154 °C a obsahu uhlíku 4,26 %. Grafitový eutektoid je směs feritu a grafitu, která vzniká při teplotě 738 °C s obsahem uhlíku 0,69 %.[4][12][13]
Slitina železa s uhlíkem se nazývá technickým železem.[4]
Binární diagramy
Rovnovážný diagram metastabilní soustavy Fe-Fe3C má technický smysl jen asi do 5 % obsahu uhlíku pro bílou litinu a pro oceli do 2,11 %. Pro vyšší koncentrace uhlíku v železe – u šedých litin – se používá diagram stabilní soustavy. Oba diagramy se často vykreslují přes sebe, přičemž metastabilní soustava se kreslí plně a stabilní čárkovaně.[7][14]

Poznámka: Některé hraniční linie a jejich významné body jsou uvedeny v odstavci kapitálkami s kurzivou, např. větev likvidu AB.
Metastabilní soustava Fe-Fe3C
Metastabilní soustava Fe–Fe3C (železo-cementit) je binární soustava s úplnou nerozpustností železa a omezenou rozpustností uhlíku. Na vodorovné ose rovnovážného diagramu jsou vyneseny koncentrace uhlíku zleva doprava. V hodnotě obsahu uhlíku 6,68 % je maximální (100%) obsah Fe3C. Na svislé ose je uvedena teplota ve stupních Celsia. Jako likvidus se označuje tavenina.[14][15]
Při hodnotách uhlíku do 0,765 % se oceli označují jako podeutektoidní, při hodnotě 0,765 % jako eutektoidní a od 0,765 % do 2,11 % jako nadeutektoidní. Slitina s obsahem uhlíku nad 2,11 % se nazývá buď jako surové železo nebo litina. Eutektikum se tvoří při obsahu uhlíku 4,3 %, od 2,11 % do 4,3 % obsahu uhlíku se jedná o podeutektické slitiny, při obsahu od 4,3 % do 6,68 % nadeutektické slitiny. Litina, která krystalizuje v souladu s diagramem metastabilní soustavy, se označuje jako bílá litina, protože obsahuje ve struktuře cementit. Výsledky krystalizace ocelí a bílé litiny jsou různé v závislosti na obsahu uhlíku.[4][9][16]
Krystalizace podeutektoidních ocelí
Při chladnutí oceli s obsahem uhlíku do 0,01 % z oblasti likvidu dochází po překročení tzv. větve likvidu AB ke krystalizaci feritu δ ve směsi s taveninou. Po překročení čáry AH bude ve směsi pouze ferit δ, který se přemění na směs s austenitem v oblasti mezi křivkami NH a NJ. Dalším ochlazováním roztoku se tvoří pouze zrna austenitu. Podobně krystalizuje i ocel s obsahem uhlíku od 0,01 % do 0,756 %. U slitiny s obsahem uhlíku 0,16 % však proběhne ještě peritektická reakce (na linii HB) při teplotě 1499 °C, při které se vyvíjejí pouze zrna austenitu. Při obsahu uhlíku mezi 0,10 a 0,16 %, vznikne směs krystalů feritu δ a austenitu. Při obsahu uhlíku od 0,16 % do 0,51 % se tvoří směs austenitu a likvidu. Při koncentraci uhlíku do 0,756 % probíhá krystalizace bez peritektické reakce na austenit podle větve JE.[17][18]

Překročením teploty A3 (větev GOS) roztok začne krystalizovat na ferit α, při dosažení teploty A2 (větev MO) se ferit stane feromagnetickým, po dosažení eutektoidní teploty A1 se začne austenit rozpadat na perlit. Struktura oceli je pak feriticko-perlitická. Při obsahu uhlíku do 0,02 % je ve struktuře obsažen terciární cementit s feritem.[4][19]
Krystalizace eutektoidní oceli
Ochlazováním z likvidu se nejprve tvoří směs zrn austenitu a taveniny mezi křivkami BC a JE až do úplné krystalizace taveniny na zrna austenitu. Při eutoktoidní reakci (bod S při teplotě 727 °C) se austenit přemění na směs feritu a eutektoidního cementitu – perlitu.[18][20] Slitina se nazývá perlitická ocel a obsah uhlíku je právě 0,765 %.[4]
Krystalizace nadeutektoidní oceli
Krystalizace austenitu z taveniny probíhá stejně jako u eutektoidních ocelí. Rozpad austenitu však začíná už na linii SE, která se označuje jako teplota Acm. V austenitu se tvoří sekundární cementit až do teploty 727 °C, pod kterou se austenit mění na perlit. Struktura nadeutektoidních ocelí s obsahem uhlíku od 0,765 % do 2,11 % je pak tvořena perlitem a sekundárním cementitem.[4][19][20]
Krystalizace podeutektické slitiny
Slitina s uhlíkem mezi 2,11 a 4,3 % krystalizuje v dendritické struktuře[pozn. 3] austenitických zrn při chladnutí likvidu mezi větvemi BC a EC, tzv. eutektiáklou. Chladnutím z eutektické teploty 1148 °C krystalizuje zbylá tavenina ve formě eutektického cementitu, tj. ledeburitu. S klesající teplotou klesá i rozpustnost uhlíku v austenitu až do eutektoidní teploty za vylučování uhlíku ve formě sekundárního cemenitu. Pod eutektoidní teplotou 727 °C se austenit rozpadá na perlit. Slitina pak obsahuje perlit, sekundární cementit a transformovaný (rozpadlý) ledeburit.[4][11][19]
Krystalizace eutektické slitiny
Eutektická slitina s obsahem uhlíku 4,3 % krystalizuje z taveniny při nejnižší tzv. eutektické teplotě 1148 °C přímo za vzniku ledeburitu.[4][11]
Krystalizace nadeutektické slitiny
Nadeutektická slitina s obsahem uhlíku od 4,3 do 6,68 % začíná tuhnout na křivce CD při tvorbě zrn primárního cementitu až do teploty eutektikály (1148 °C). Zbylá tavenina překročením eutektikály začne krystalizovat na zrna ledeburitu. Pod teplotou 727 °C se stejně jako u podeutektoidní slitiny ledeburit přemění na transformovaný ledeburit. Směs pak obsahuje ještě i primární cementit.[4][11]

Poznámka: Některé hraniční linie a jejich významné body jsou uvedeny v odstavci kapitálkami s kurzivou, např. větev A’C’.
Stabilní soustava železo-uhlík
Binární diagram stabilní soustavy má praktické využití jen pro slitiny s obsahem uhlíku vyšším než 2 %. Na vodorovné ose rovnovážného diagramu je vynesena koncentrace uhlíku, která vzrůstá zleva doprava. Eutektická krystalizace a eutektoidní rozpad stabilní soustavy probíhají při nižším obsahu uhlíku a při vyšších teplotách než u metastabilní soustavy. Litiny obsahující grafit se na lomu jeví jako šedé, proto jsou také označovány jako tzv. šedé litiny.[12][13]
Podeutektické slitiny obsahují od 2,08 %[12] (2,11 %[4]) do 4,26 % uhlíku. Obsah uhlíku nad 4,26 % tvoří nadeutektickou slitinu.[13]
Krystalizace podeutektické slitiny
Při chladnutí slitiny z likvidu nejdříve se začnou vytvářet krystaly austenitu v tavenině – pod větví A’C’. Překročením eutektické teploty 1154 °C (čára E’C’) se z taveniny vyloučí primární grafit a grafitové eutektikum k již vytvořeným krystalům austenitu. Pod eutektoidní teplotou 737 °C (čára O’K’) se austenit rozpadá na grafitový eutektoid, tj. směs feritu a lupínkového grafitu[4][12][13]
Krystalizace eutektické slitiny
Při koncentraci 4,26 % uhlíku vzniká při chladnutí přímo grafitické eutektikum (směs zrn austenitu a grafitu). Austenit se dále rozpadá na ferit a grafit, stejně jako u podeutektické slitiny.[4][12]
Krystalizace nadeutektické slitiny
Z likvidu se překročením větve C’D’ tvoří směs krystalů primárního grafitu a taveniny. Primární grafit má nižší objemovou hustotu než tavenina (asi třikrát) a vyplouvá na povrch. Tímto se v tavenině snižuje obsah uhlíku až do eutektické koncentrace 4,26 %, ze které se pod eutektickou teplotou (čára C’F’) krystalizuje grafitické eutektikum. Rozpad austenitu vytvoří směs feritu a grafitu.[4][12][13]
Význam binárních diagramů železo-uhlík
Nejvýhodnější teplota (nejnižší) pro odlévání litin je při koncentraci uhlíku 4,26 %. Tekutost eutektické litiny je dosažena již nad teplotou 1148 °C resp. 1154 °C, ale eutektoidní ocel je tekutá až při téměř 1495 °C a čisté železo až při 1538 °C.[15][12] |
Z binárních diagramů lze odvodit jednotlivé fáze a strukturu slitiny železo-uhlík na základě obsahu uhlíku a dosažené teploty.[21] Významné jsou především informace pro technologické zpracování a to zejména v oblasti teplotní: určení teplot tavení, lití, přehřátí taveniny, tváření (např. kování nebo válcování) nebo svařování a dalšího tepelného zpracování (např. žíhání, cementování, kalení a popouštění).[15][21][22]
Teplotní hranice označována jako A1 odpovídá přímce eutektoidní přímce PSK resp. P’S’K’, která prochází eutektoidním bodem S reps. S’ při eutektoidní koncentraci 0,765 % uhlíku. Teplota A2 je totožná s Curieovou teplotou. Teplotní hranice A3 určuje překrystalizaci tuhého roztoku austenitu podeutektoidního složení a je definována křivkami GOS resp. G’O’S’. Změnu rozpustnosti uhlíku v austenitu je pak určena křivkou SE resp. S’E’ označovanou Acm. Peritektická přeměna, která popisuje změnu alotropické modifikace železa δ – železo γ, se označuje A4 a je definována křivkami NJB resp. N’J’B’.[9][14]
Vliv dalších prvků na binární diagram železo-uhlík
Binární diagramy obou soustav popisují pouze slitinu železo–uhlík bez vlivů dalších prvků, které se ve slitině nacházejí. Prvky, které jsou v těchto slitinách přítomny z výroby, mohou být buď nežádoucí (např. síra, fosfor) nebo doprovodné (např. mangan, křemík, hliník). Prvky legující jsou prvky záměrně dodávané do slitiny v různých koncentracích (např. mangan, molybden, chrom, nikl, titan, vanad, wolfram, bor a další). Všechny prvky nějakým způsobem mění binární diagramy. Jednak to jsou feritotvorné prvky, které uzavírají (zmenšují) oblast austenitu takovým způsobem, že pro jistá složení ocelí není dosaženo austenitu při žádné teplotě. Takovými prvky jsou např. chrom, křemík, molybden, wolfram, vanad. Austenitotvorné prvky naopak otvírají (rozšiřují) oblast austenitu a je možné dosáhnout austenitické struktury i za normální teploty, takovými prvky jsou uhlík, nikl, mangan a měď. Karbidotvorné, nitridotvorné prvky a karbonitridové prvky se slučují s uhlíkem nebo dusíkem, případně oběma při vzniku precipitátů, které mají velký vliv na chemické (např. korozivzdornost) i fyzikální (např. pevnost či tažnost) vlastnosti ocelí. Takovými prvky bývají např. titan, hliník, vanad, wolfram, chrom atd. Pro litiny se používají přísady, kterými lze upravovat teplotu eutektika, tvar grafitu, vlastnosti perlitu i feritu.[22][23][24][25][26][27]
Odkazy
Poznámky
Reference
- ↑ a b c Foldyna et al., str. 71
- ↑ a b c Hluchý et al., str. 57
- ↑ a b c d Foldyna et al., str. 72
- ↑ a b c d e f g h i j k l m n o p Systém Fe-C [online]. VŠCHT, 2009-02-20 [cit. 2011-07-07]. Dostupné v archivu pořízeném dne 2011-08-08.
- ↑ Foldyna et al., str. 68
- ↑ Hluchý et al., str. 58
- ↑ a b Foldyna et al., str. 73
- ↑ Hluchý et al., str. 59
- ↑ a b c d Hluchý et al., str. 62
- ↑ Hluchý et al., str. 63
- ↑ a b c d Hluchý et al., str. 65
- ↑ a b c d e f g Hluchý et al., str. 66
- ↑ a b c d e Hluchý et al., str. 67
- ↑ a b c Hluchý et al., str. 60
- ↑ a b c Hluchý et al., str. 61
- ↑ Foldyna et al., str. 74
- ↑ Foldyna et al., str. 75
- ↑ a b Foldyna et al., str. 76
- ↑ a b c Hluchý et al., str. 64
- ↑ a b Foldyna et al., str. 77
- ↑ a b Hluchý et al., str. 71
- ↑ a b Foldyna et al., str. 79
- ↑ Foldyna et al., str. 80
- ↑ Foldyna et al., str. 81
- ↑ Hluchý et al., str. 68
- ↑ Hluchý et al., str. 69
- ↑ PODRÁBSKÝ, Tomáš; POSPÍŠILOVÁ, Simona. Struktura a vlastnosti grafitických litin [online]. Vysoké učení technické v Brně, Fakulta strojního inženýrství, Ústav materiálových věd a inženýrství, 2006-11-16 [cit. 2011-07-14]. Dostupné online.
Literatura
- FOLDYNA, Václav; HENNHOFER, Karel; OLŠAROVÁ, Věra, Hlavatý, Ivo; Koukal, Jaroslav; Kristofory, František; Ochodek, Václav; Pilous, Václav; Purmenský, Jaroslav; Schwarz, Drahomír; Veselko, Július., 2000. Materiály a jejich svařitelnost. Recenzent: Jaroslav Koukal. 1. vyd. Ostrava: Česká svářečská společnost ANB, ZEROSS, c2000. 216 s. ISBN 80-85771-85-3. [reference viz Foldyna et al.].
- HLUCHÝ, Miroslav; MODRÁČEK, Oldřich; PAŇÁK, Rudolf, 2002. Strojírenská technologie. Lektoři Dr. Otakar Bothe a Ing. Ladislav Němec. 3. vyd. Svazek 2. Praha: Scientia. 173 s. ISBN 80-7183-265-0. [reference viz Hluchý et al.].
- PACAL, Bohumil; DOLEŽAL, Pavel. Struktura slitin stabilní soustavy železo – uhlík (Fe – C) [online]. VUT, Fakulta strojního inženýrství, Ústav materiálových věd a inženýrství, 2006-11-20 [cit. 2011-07-15]. Dostupné online.
- 7. Slitiny železa a uhlíku [online]. VUT, Fakulta strojního inženýrství, Ústav materiálových věd a inženýrství, 2003-01-24 [cit. 2011-07-15]. Dostupné v archivu pořízeném dne 2009-02-06.
- Iron-Carbon Phase Diagram (a review) see Callister Chapter 9 [online]. University of Tennessee, Dept. of Materials Science and Engineering, 2004-05-28 [cit. 2011-07-15]. Dostupné v archivu. (angličtina)
Související články
- Alotropické modifikace železa
- Binární diagram
- TTT diagram
- Diagram izotermického rozpadu austenitu
- Diagram anizotermického rozpadu austenitu
- Shafflerův diagram
- Metalografie
Externí odkazy
 Obrázky, zvuky či videa k tématu binární diagram železo-uhlík na Wikimedia Commons
Obrázky, zvuky či videa k tématu binární diagram železo-uhlík na Wikimedia Commons - (anglicky) Iron-Iron Carbide Phase Diagram Example
- (anglicky) Iron-carbon phase diagram
Média použitá na této stránce
Autor:
- Trempe_acier_et_mouvements_atomes.svg: Cdang
- derivative work: Alu (talk)
atomová mřížka železa alfa a gama
Autor: Alu, Licence: CC BY 3.0
Schéma rovnovážného binárního diagramu metastabilní soustavy Fe-Fe3C
Ferrite (light gray) and perlite (dark gray) in carbon steel A285 (% wt.: 0.18 C, 0.43 Mn, 0.009 P, 0.026 S).