Boran
| Boran | |
|---|---|
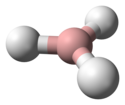
 kuličkový model molekuly | |
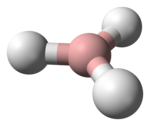
 kalotový model molekuly | |
| Obecné | |
| Systematický název | boran |
| Ostatní názvy | borovodík |
| Anglický název | borane |
| Německý název | Boran |
| Sumární vzorec | BH3 |
| Vzhled | bezbarvý plyn |
| Identifikace | |
| Registrační číslo CAS | 13283-31-3 |
| PubChem | 6331 |
| ChEBI | 30149 |
| SMILES | B |
| InChI | InChI=1S/BH3/h1H3 |
| Vlastnosti | |
| Molární hmotnost | 13,83 g/mol |
| Hustota | 0,57 kg/m3 |
| Rozpustnost ve vodě | rozkládá se |
| Rozpustnost v polárních rozpouštědlech | 4,4 g/100 ml (amoniak) |
| Struktura | |
| Tvar molekuly | trojúhelník |
| Dipólový moment | nulový |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | 106,69 kJ/mol |
| Standardní molární entropie S° | 187,88 kJ⋅K−1⋅mol−1 |
Některá data mohou pocházet z datové položky. | |
Boran je anorganická sloučenina se vzorcem BH3. Je to nejjednodušší z boranů, dvouprvkových sloučenin boru a vodíku, a základní molekula pro monoborany.
Historie
V roce 1937 byl objeven karbonyltrihydridobor, jehož objev hrál důležitou roli ve výzkumu chemie „normálních“ boranů v době, kdy ještě nebyla známa tricentrická dvouelektronová vazba.[1] Tento objev také existenci boranu, ovšem přímý důkaz byl proveden až o několik let později.
Chemické vlastnosti
Struktura
Molekuly BH3 mají trojúhelníkový tvar s atomy vodíku ve vrcholech a atomem boru uprostřed. Délka vazby B–H je 119 pm[2] stejně jako má koncová vazba B–H v diboranu. U boranu dochází k dimerizaci na diboran, reakce probíhá samovolně, jelikož její entalpie je kolem −40 kJ/mol.[3]: 2 BH3 → B2H6
Amfoterita
Přestože boran v základu působí jako Lewisova kyselina, neustále je vytvářeno mnoho 1:1 aduktů z diboranu nebo záměnou ligandů u existujících aduktů. B2H6 + 2 L → 2 LBH3
Odhadovaná řada stability je: PF3 < CO < Et2O < Me2O < C4H8O < C4H8S < Et2S < Me2S < Me3N < H−
BH3 má některé vlastnosti slabé kyseliny.
Borylová skupina (-BH2) ve sloučeninách, jako je diboran, se může napojit na další vodíkové centrum v molekule ionizací[4]: BH3 + H+ → BH2(H2)+
Protože zde přijímá proton, má boran vlastonsti zásady. Jeho konjugovaná kyselina je (η-dihydrogen)dihydridobor(1+) ([BH2(η-H2)]+)
Boran jako reaktivní meziprodukt
Příkladem reakce, u které se předpokládá, že je boran jejím meziproduktem, je pyrolýza diboranu za vzniku vyšších boranů: B2H6 ⇌ 2BH3
BH3 + B2H6 → B3H7 +H2
BH3 + B3H7 ⇌ B4H10
B2H6 + B3H7 → BH3 + B4H10
⇌ B5H11 + H2
Výroba
Existují dva hlavní způsoby výroby boranu. První z nich spočívá v reakci diboranu s dimethylsulfidem. Další metodou je částečná oxidace boranuidové soli v koordinujícím rozpouštědle jako je trimethylamin.
Použití
Boranové adukty se široce používají v organické syntéze na hydroboraci, kde adicí BH3 na vazbu C=C v alkenech vznikají trialkylborany: (THF)BH3 + 3 CH2=CHR → B(CH2CH2R)3 + THF Produkt této reakce lze převést na různé organické deriváty.
Reference
V tomto článku byl použit překlad textu z článku Borane na anglické Wikipedii.
- ↑ BURG, Anton B.; SCHLESINGER, H. I. Hydrides of boron. VII. Evidence of the transitory existence of borine: Borine carbonyl and borine trimethylammine. Journal of the American Chemical Society. May 1937, s. 780–787. doi:10.1021/ja01284a002.
- ↑ KAWAGUCHI, Kentarou. Fourier transform infrared spectroscopy of the BH3 ν3 band. The Journal of Chemical Physics. 1992, s. 3411. ISSN 0021-9606. doi:10.1063/1.461942.
- ↑ M. Page, G.F. Adams, J.S. Binkley, C.F. Melius "Dimerization energy of borane" J. Phys. Chem. 1987, vol. 91, pp 2675–2678. doi:10.1021/j100295a001
- ↑ RASUL, Golam; PRAKASH, Surya G. K.; OLAH, George A. Complexes of CO2, COS, and CS2 with the Super Lewis Acid BH4+ Contrasted with Extremely Weak Complexations with BH3: Theoretical Calculations and Experimental Relevance. Journal of the American Chemical Society. ACS Publications, 18 August 1999, s. 7401–7404. doi:10.1021/ja991171a.
Externí odkazy
 Obrázky, zvuky či videa k tématu boran na Wikimedia Commons
Obrázky, zvuky či videa k tématu boran na Wikimedia Commons
Média použitá na této stránce
Space-filling model of the borane molecule, BH3
Ball-and-stick model of the borane molecule, BH3