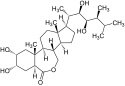
Brassinosteroidy

Brassinosteroidy (BR) jsou třída polyhydroxysteroidů, které byly zařazeny jako v pořadí již šestá skupina rostlinných hormonů. Byly objeveny roku 1970, když John W. Mitchell a jeho kolegové zjistili, že extrakt z pylu řepky (Brassica napus) má podpůrný vliv na elongaci stonku a dělení buněk rostlin.[1] V roce 1979 pak byla izolována biologicky aktivní molekula, odpovědná za výše jmenované působení řepkového pylu; látka byla nazvána brassinolid.[2][3]
Brassinosteroidy se vyskytují a působí ve velmi malých množstvích. Z 230 kg řepkového pylu je možné získat pouze 10 mg brassinolidu.[zdroj?] Od tohoto objevu bylo v rostlinách identifikováno celkem již více než 70 sloučenin s brassinosteroidním účinkem.[4]
Základní účinky
Brassinosteroidy mají několik objasněných základních účinků na rostliny:
- Podporují buněčný růst[5] (za současného působení auxinů).[6]
- Zatím nevyjasněná role v buněčném dělení a regeneraci buněčné stěny.[5]
- Podpora diferenciace cévních svazků.[7]
- Brassinosteroidy jsou nezbytné pro vytvoření a růst pylové láčky.[8]
- Částečně chrání rostliny před účinky stresu suchem a chladového stresu.[5]
Objev brassinosteroidů
Samotnému objevu v rostlinách předcházelo zjištění, že pylové extrakty stimulují růst rostlin. Mitchel et al., sebrali v roce 1970[1] pyl z asi 60 druhů rostlin a přibližně polovina těchto pylových extraktů podporovala růst fazolových semen. Látka v pylu zlepšující růst byla nazvána brassin. Později se ukázalo, že aktivní látky je v brassinu pouze nepatrné množství. Tato aktivní složka byla izolována vědci z Northern Regional Research Center – Peoria v roce 1979 v množství 4 mg ze 40 kg pylu řepky olejky (Brassica napus) a byla pojmenována brassinolid, podle zdroje pylu. Současně byla krystalografickou analýzou stanovena její struktura.[9]
V roce 1982 byl izolován jako druhý ze skupiny brassinosteroidů castasteron z hmyzích hálek kaštanovníku (Castanea crenata). Následoval objev dolicholidu a mnoha dalších.
V dnešní době je mimo přírodních brassinosteroidů, mnoho strukturních analogů brassinolidu připraveno chemicky. Od doby objevení brassinosteroidů se mnoho vědců zabývá jejich výzkumem, studují jejich chemickou strukturu, syntézu a biologickou aktivitu, molekulární mechanizmy účinku, vliv na rostliny, výskyt v rostlinách, transport a metabolismus v rostlinách a v neposlední řadě také praktické využití brassinosteroidů v zemědělství (přičemž v některých zemích už byly brassinosteroidy schváleny k polnímu použití.[poznámka 1][10]
Přirozený výskyt brassinosteroidů
Brassinosteroidy byly nalezeny ve všech druzích rostlin, u kterých byl proveden podrobnější výzkum (jednoděložných i dvouděložných), a jsou obsaženy ve všech rostlinných orgánech. Výskyt brassinosteroidů v kořenech byl potvrzen teprve nedávno.[11]
Brassinosteroidy jsou v rostlinách přítomny v extrémně nízkých koncentracích. Vnitrobuněčný obsah brassinosteroidů kolísá v závislosti na typu orgánu, stáří tkáně a druhu rostliny. Mladá pletiva jich obsahují větší množství než pletiva zralá. Pyl a semena jsou nejbohatšími zdroji. Dosud nejvyšší koncentrace byla zaznamenaná v pylu cypřiše (Cupressus arizonica) a dalším zajímavým místem výskytu jsou hmyzí hálky kaštanovníku nebo hálky v květech u Distylium racemosum a barvínku (Catharanthus roseus). Tyto hálky obsahují také vyšší koncentrace brassinosteroidů.[12]
Přítomnost brassinosteroidů v nižších rostlinách byla dokázána u zelené řasy (Hydrodictyon reticulatum), játrovky (Marchantia polymorfa) a přesličky (Equisetum arvense).
Mezi brassinosteroidy je u rostlin nejvíce rozšířen castasteron, následován brassinolidem a typhasterolem.
Přenos signálu
Signální dráhy brassinosteroidů nevyužívají cytoplazmatické steroidové receptory, tak jako je tomu u živočichů a člověka, ale jejich receptor je umístěn v plazmatické membráně, funguje na buněčném povrchu a převádí extracelulární signály do buňky (Li a Chory, 1997).
Hlavním brassinosteroidovým receptorem je serin/threonin kinasa BRI1, která je lokalizována v plazmatické membráně a je exprimována ve všech orgánech mladých rostlin huseníčku.[13]
Vliv brassinosteroidů na rostliny
Brassinosteroidy ovlivňují růstové i reprodukční procesy, stimulují růst i dělení buněk, růst mladých vegetativních pletiv (epikotylu, hypokotylu, koleoptile), indukují kvetení, zrání plodů, klíčení semen, tvorbu a růst kořenů, růst pylových láček, podílejí se na diferenciaci systému vodivých pletiv, hrají spolu s dalšími fytohormony zásadní roli při senescenci, aktivují protonové pumpy v buněčných membránách, ovlivňují fotosyntézu, asimilaci uhlíku a fixaci dusíku, podporují produkci etylenu, chrání rostlinu proti abiotickým i biotickým stresorům a podílejí se i na dalších procesech v rostlině.[14] Vývojové a růstové aktivity jsou hlavně spojeny s ATPázovou aktivitou, syntézou syntetasy 1-aminocyklopropan-1-karboxylové kyseliny změnu v orientaci mikrotubulů, a modifikaci buněčných stěn.[15]
Vliv brassinosteroidů na růst rostlin a diferenciaci pletiv
Od doby, kdy byl chemicky syntetizován brassinolid a jeho stereoizomer, 24-epibrassinolid (v roce 1981), mohly začít v širokém měřítku pokusy s aplikací brassinosteroidů na různé tkáně a orgány rostlin, a to ve skleníkových i polních podmínkách. První zpráva o vlivech brassinosteroidů na růst huseníčku se objevila v roce 1991, následována krátce nato popisem výběru mutantu u této rostliny (které jsou necitlivé k aplikovaným brassinosteroidům nebo jich syntetizují nedostatečné množství) a pozorováním, že brassinosteroidy u tohoto druhu regulují genovou expresi.[16]
Vliv brassinosteroidů na prodlužovací růst byl potvrzen mnoha pracemi. Velmi účinné jsou při stimulaci růstu mladých vegetativních tkání (obsah a tedy i citlivost je v těchto tkáních vyšší). Bylo pozorováno, že brassinosteroidy stimulovaly růst zelené řasy Chlorella vulgaris a mycelií Psilocybe cubensis a Gymnopilus purpuratous. Na druhou stranu však inhibovaly růst nádorových buněk vyvolaný Agrobacterium tumefaciens. Aplikace brassinosteroidů tedy většinou růst stimuluje, může ho ale i inhibovat. Studie na epikotylech soji odhalila schopnost brassinosteroidů stimulovat buněčný růst, a ten byl doprovázen výlevem protonů a hyperpolarizací buněčných membrán. V kultuře mrkvových (Daucus carota) buněk vyvolal 24-epibrassinolid pouze zvětšování buněk, aniž by měl jakýkoli vliv na jejich dělení.[16] Podélný prodlužovací růst buněk je v deficitních mutantech huseníčku (cbb, dwf4, cpd, dim) velmi snížen. Jak lze předpokládat, je u nich nižší i exprese genů spojených s prodlužovacím růstem buněk. Ukázalo se, že brassinosteroidy ovlivňují rekonfiguraci mikrotubulů do příčného uspořádání, které umožňuje podélný růst.
Brassinosteroidy mohou podpořit organizaci mikrotubulů a prodlužovací růst buněk přímo, aniž by vzrostla exprese genů tubulinu, nebo mohou ovlivnit transport vody aquaporiny a aktivitu vakuolární protonové (H+) ATPasy, což je oboje spojeno s prodlužovacím růstem buněk.[17][18] Brassinosteroidy ovlivňují zřejmě stejnou měrou růst i dělení buněk. Ovlivňují také kinetiku buněčného cyklu v synchronizovaných kulturách buněk tabáku (Nicotiana tabacum) a také regulují geny exprimující se v S fázi. Brassinosteroidy mají stimulující roli na dělení buněk.[17]
Regulace syntézy a aktivity enzymů účastnících se modifikace buněčné stěny (jako jsou xyloglukan, endotransglykosylasy, glukanasy, expansiny a další) se stala častým místem působení hormonů regulujících prodlužovací růst buněk. Nanomolární koncentrace brassinolidu stimuluje tvoření tracheid (xylogenezi) v izolovaných mezofylových buňkách ostálky (Zinnia elegans).[16] Brassinosteroidy regulují expresi mnoha genů, přispívajících k regulaci buněčného dělení a diferenciace, a pomáhají řídit celkové vývojové procesy vedoucí k morfogenezi rostliny. Podílejí se na regulaci fotomorfogeneze, skotomorfogeneze a buněčného růstu v přítomnosti buněčné stěny, která je potenciálním limitem růstu.[17]
Vliv brassinosteroidů na kořeny
V kořenech se nachází mnohem nižší množství brassinosteroidů než ve výhoncích a jiných částech rostliny.[19] I vzhledem k tomu, že brassinosteroidy byly v kořenech nalezeny,[20] jsou v kořenech také přítomny proteiny potřebné pro biosyntézu brassinosteroidů, stejně tak jako proteiny potřebné pro přenos brassinosteroidového signálu (BRI1 a BAK1). To naznačuje, že brassinosteroidy jsou důležité regulační sloučeniny také pro růst a vývoj kořenů. Pokusy, při kterých bylo studováno ovlivnění růstu kořenů brassinosteroidy, prokázaly inhibiční i stimulační účinky na růst kořenů.
Bohužel se při těchto pokusech pracovalo jen s kořenovými segmenty a byly tak přerušeny mnohé signalizační dráhy. 24-epibrassinolid měl inhibiční vliv na formaci kořenů u sazenic fazolu, pšenice (Triticum aestivum) a kukuřice (Zea mays).[14] Guan a Roddick (1988) zjistili inhibiční vliv 0,1 µM 24-epibrassinolidu na růst kořenů rajčete, také stejná koncentrace 24-epibrassinolidu silně inhibovala růst kořenů huseníčku. Ale inhibiční vliv brassinosteroidů na růst kořenů odporuje faktu, že mutanti mají redukovaný kořenový systém.[14]
V deficitních mutantech (zde byl použit cbb3) je na vyvolání inhibice růstu potřeba vyšší množství brassinosteroidů (>10 nM), nižší koncentrace růst kořenů stimulují. Lze říct, že nízké koncentrace brassinosteroidů podporují růst kořenů a brassinosteroidy přejdou na cestu inhibice pokud je překročena hraniční koncentrace brassinosteroidů. Tato hraniční koncentrace závisí na biologické aktivitě aplikovaného brassinosteroidu a genotypu rostliny.[14] Například je tato hranice nižší u 24-epibrassinolidu než u 24-epicastasteronu, a vyšší v mutantech necitlivých k brassinosteroidům.[14]
Doba ošetření, koncentrace a vývojové stádium rostliny má i zde velký vliv na působení brassinosteroidů na rostlinu.[21]
Brassinolid spolupracuje s auxinem při gravitropickém zakřivení primárních kořenů kukuřice. Aktivace gravitropického zakřivení pomocí brassinolidu byla plně anulována při aplikaci inhibitoru polárního transportu auxinu.[11] Exogenně aplikovaný brassinolid (10-9 M a 10-5 M) zvýšil gravitropické zakřivení v primárních kořenech kukuřice. Takto vyvolané zakřivení bylo velmi zvýrazněno přítomností auxinu (10-8 M a 10-10 M).
Vliv brassinosteroidů na květy a semena
Brasisinosteroidy pravděpodobně podporují růst pylové láčky při prorůstání bliznou.[14] Obsah brassinosteroidů v pylu je oproti jiným částem rostliny velmi vysoký, což naznačuje, že brassinosteroidy mohou mít významnou roli při regulaci reprodukce. Velmi vysoké koncentrace brassinosteroidů byly nalezeny také v semenech.[12] Aplikace brassinolidu zlepšila klíčení řeřichy či eukalyptu (Eucalyptus camaldulensis). Brassinolid, 24-epibrassinolid a 28-homobrassinolid podpořily klíčení semen podzemnice olejné (Arachis hypogaea). Obdobné výsledky byly získány při ošetření semen řepky, rajčete, tabáku, a dalších.[16] Snížená fertilita nebo samčí sterilita jsou běžné charakteristiky mutantů s nedostatkem brassinosteroidů nebo necitlivých k brassinosteroidům.[17] Ukázalo se, že v zásadě brassinosteroidy zlepšují klíčení semen a růst sazenic. Tento vliv může zvýšit výnos, zejména v suboptimálních růstových podmínkách.[22]
Vliv brassinosteroidů na výnos
Ihned po objevení brassinosteroidů byly iniciovány studie možnosti využití brassinosteroidů na zlepšení výnosu zemědělských plodin, a to jak v laboratorních, tak v polních podmínkách. Brassinosteroidy zvýšily výnos pšenice, ječmene, rýže, kukuřice, soji, fazolu, podzemnice olejné, hlávkového salátu, ředkviček, rajčat, mrkve, celeru, cibule, česneku, brambor, špenátu, papriky, bavlníku, čajovníku, kávovníku, jabloní, jahod, citrusů, vodního melounu, cukrové řepy, hořčice, řepky, tabáku, okurky, hroznů, a dalších.[14][16][23][24]
Brassinosteroidy zcela prokazatelně zvyšují výnos mnoha kulturních plodin, zvlášť v suboptimálních podmínkách, jsou pro rostliny zcela přirozené a neškodí životnímu prostředí. Jsou tedy vhodné k široké aplikaci v zemědělství pro zvýšení výnosů a ochranu rostlin[22]).
Vliv brassinosteroidů na stárnutí
Stárnutí rostlin je regulováno fytohormony a i zde hrají brassinosteroidy důležitou roli. Brassinolid zpožďuje odpadnutí listů citrusu.[16]
Mnoho brassinosteroidových mutantů má prodlouženou délku života a zpožděnou senescenci. Zpožděné stárnutí koreluje se sníženou fertilitou, sterilní mutanti jako je bri1 (brassinosteroidový insenzitivní) mají nejvíc zpožděný vývoj. Předpokládá se, že neschopnost vytvářet signály pro nástup senescence v neplodných mutantech vede k pozorovanému prodloužení délky života rostliny. Toto tvrzení také podpořilo domněnku o roli brassinosteroidů při navozování stárnutí u rostlin.[17]
Vliv brassinosteroidů na ostatní procesy v rostlinách
Postřik brassinolidem může hrát důležitou roli ve zvyšování komerční hodnoty ovoce (Litchi). Ošetření brassinoslidem také podpořilo růst, produkci plodů a zmírnilo jejich praskání. Postřik na listy tedy výrazně ovlivnil enzymové aktivity, obsah vápníku v perikarpu plodů a snížil praskání plodů.[24]
Ukázalo se, že 24-epibrassinolid přímo ovlivnil rychlost fotosyntézy.[25]
Brassinosteroidy stimulují růst hypokotylů na světle, ale inhibují jeho růst za tmy. Nicméně přiměřené koncentrace brassinosteroidů jsou potřebné jak pro růst na světle, tak i ve tmě. Je možné, že existuje optimální koncentrace brassinosteroidů v sazenicích. Nad tuto prahovou koncentraci, (která může záviset na vnějších podmínkách) brassinosteroidy růst inhibují. Interakce s ostatními fytohormony také může určit stupeň brassinosteroidové odpovědi.[14]
Brassinosteroidy ovlivňují mnoho procesů v rostlině. To, zda toto ovlivnění bude pozitivní nebo negativní velmi záleží na době aplikace brassinosteroidů, koncentraci, stáří a celkové kondici rostliny a na typu aplikovaného brassinosteroidu. Tyto procesy jsou ovlivněny hlavně přenosem signálu a expresí brassinosteroidy-indukovatelných genů. Přitom nelze zapomínat na interakce s ostatními fytohormony a vliv prostředí.
Protistresové účinky
Rostliny nemají motorický aparát, proto nemohou utéct před stresy z okolí. Brassinosteroidy zvyšují odolnost rostlin vůči různým abiotickým i biotickým stresům. Zvyšují odolnost rostlin k vysokým a nízkým teplotám, k vodnímu deficitu nebo zamokření substrátu, nadměrným koncentracím těžkých kovů nebo solí, pesticidům a herbicidům (abiotické stresy) a působení bakterií, virů či hub (biotické stresy). O mechanizmech těchto účinků je zatím známo pouze málo. Mechanizmem, který se může podílet na odolnosti k různým typům stresu je například zvýšená aktivita antioxidantů a jejich vysoký obsah při odpovědi na vysoké a nízké teploty, zasolení, sucho a zraňování a na oxidativní stres, a může hrát hlavní roli při získávání odolnosti rostlin na různé stresy z okolí.[26] Byla také zjištěna vyšší exprese heat shock proteinů nebo ATP[27][16])
Nízká teplota
Mnoho fyziologických procesů v rostlině je ovlivněno nízkou teplotou (fotosyntéza, klíčivost, zakořeňování, nasazování květů nebo plodů). Chladová tolerance může být indukována růstovými regulátory, je ale doprovázená zpožděním růstu po ošetření. Chladová tolerance je však v mnoha pokusech vyvolaná kyselinou abscisovou v relativně vysoké koncentraci, což inhibuje růst rostlin a buněk.[28]
Brassinosteroidy posilují toleranci rostlin k chladovému stresu, zvyšují účinnost a rychlost fotosyntézy, zvyšují obsah chlorofylu etiolovaných sazenic, podporují růst buněk a růst biomasy, urychlují a zlepšují růst mladých rostlin, působí na membránovou stabilitu, osmoregulaci a nasazování plodů, celkově tedy zmírňují poničení způsobená chladem a tento vliv je výraznější při nižších teplotách. Kombinované předošetření rostlin kyselinou abscisovou a 24-epibrassinolidem výrazně mírní poškození procesu fotosyntézy chladem,[28][29] brassinolid pravděpodobně zmírňuje snížení sušiny a rozklad chlorofylu po působení chladového stresu[30]
Vysoká teplota
Teplotní stres zvyšuje produkci kyslíkových radikálů v rostlinách. Superoxid dismutasa je klíčový enzym detoxifikace kyslíkových radikálů. Oba brassinosteroidy stimulovaly aktvivitu superoxid dismutasy při 25 i 40 °C a nebyl pozorován žádný významný rozdíl mezi použitými koncentracemi.[26] 24-epibrassinolidem vyvolaná zvýšená aktivita superoxid dismutasy při 40 °C může být cestou k odstranění přebytku vzniklých kyslíkových radikálů. Aktivita katalasy při vysoké teplotě poklesla, 24-epibrassinolid stimuloval její aktivitu při obou testovaných teplotách, ale jen v koncentraci 10,6 nM.[26] Tyto výsledky naznačují možnou roli obou sloučenin při snižování buněčného poškození vyvolaného teplotním stresem v závislosti na těchto enzymech. Ošetření sazenic řepky 24- epibrassinolidem (1 µM) vede k výraznému nárůstu jejich základní termotolerance. 24-epibrassinolid zvýšil akumulaci čtyř hlavních tříd heat-shock proteinů v porovnání s neošetřenými rostlinami během i po skončení působení stresu.[27][31] Syntéza heat-shock proteinů je řízena na posttranskripční úrovni. Ošetření 24-epibrassinolidem snižuje ztráty některých složek translačního aparátu během obnovy, což koreluje s rychlejším návratem buněčné protein-syntézy po teplotním šoku a vyšším poměrem rostlin, které přežijí[27] Ošetření brassinolidem zvyšuje odolnost k vysoušení a stresu z vysoké teploty. Rostliny ošetřené brassinolidy vykazovali menší ztrátu složek translačního aparátu díky, ke které by jinak došlo v důsledku teplotního stresu.[27][32][33]
Sucho a zamokření substrátu
Rostliny řepky byly ošetřeny syntetickými brassinosteroidy (4 varianty) postřikem na list. Jedna skupina byla ošetřena 7 dní před počátkem a druhá 5 dní po počátku stresu sucha a zamokření substrátu. Vliv stresu na rostliny byl sledován změnou sušiny, produkcí etylenu a hladinou kyseliny abscisové. Brassinosteroidy snížily hladinu kyseliny abscisové a produkci etylenu u rostlin stresovaných suchem při aplikaci 5 dní po počátku stresu. Výrazné snížení hladiny kyseliny abscisové bylo zaznamenáno již po 24 hodinách po postřiku, snížení produkce etylenu bylo pozorováno až po 48 hodinách. Tento efekt byl pozorován ještě 7 dní po aplikaci a po 2–3 týdnech vymizel. Vliv ošetření rostlin brassinosteroidy během stresu suchem byl výraznější než vliv ošetření před počátkem stresu. Aplikace brassinosteroidů jak před, tak během působením stresu mírně zvyšovala akumulaci sušiny. Produkce etylenu během stresu zamokřením substrátu u rostlin ošetřených před počátkem stresu nebyla ovlivněna. Při ošetření během stresu se produkce etylenu snížila oproti kontrole. Všechny použité brassinosteroidy měly pozitivní vliv na akumulaci sušiny, snížily na určitou dobu po aplikaci produkci etylenu a také endogenní hladinu kyseliny abscisové. Pozorované změny hladin kyseliny abscisové a etylenu jsou v souladu s předpokladem, že méně stresované rostliny mají nižší endogenní obsah kyseliny abscisové a uvolňují méně etylenu.
Bylo popsáno, že 24-epibrassinolid při aplikaci postřikem na vyvinuté rostliny zvyšuje růst rostlin a nárůst sušiny kořenů a výhonů při vodním stresu. Postřik na listy i ošetření obilek pšeničných odrůd citlivých nebo tolerantních k suchu 28-homobrassinolidem, mělo stimulační vliv na růst stresovaných rostlin. Přestože byl pozorován pouze malý rozdíl vlivu 28-homobrassinolidu na tyto dvě pšeničné odrůdy, tak celkově odrůda tolerantní k suchu měla silnější odpověď na ošetření 28-homobrassinolidem při působení vodního stresu. Stoupající příjem vody, membránová stabilita a vyšší asimilace CO2 a dusíku v ošetřených stresovaných rostlinách korelovaly se zvýšenou odolností k suchu vyvolanou 28-homobrassinolidem.[34] Aquaporiny jsou membránové vodní kanály, které hrají hlavní roli v kontrole obsahu vody v buňkách.
Brassinosteroidy mohou hrát roli v propustnosti pro vodu přes aquaporiny, a že brassinosteroidy neovlivňují přímo plazmatickou membránu v tomto procesu, protože zde nebyl pozorován žádný “rychlý“ vliv na osmotickou propustnost protoplastů způsobený brassinosteroidy. Změny v osmotické permeabilitě zde korelovaly s růstem hypokotylu.[35]
Patogeny
Brassinosteroidy indukují rezistenci k rostlinným patogenům. V některých výzkumech se brassinosteroidy ukázaly být efektivnější ochranou rostlin než standardní fungicidy.[33] Brassinolidem indukovaná odolnost nekorelovala se zvýšením obsahu kyseliny salicylové ani s indukcí „pathogenesis-related“ genové exprese (zraněním indukované odolnosti). Navíc se systémově získanou odolností (SAR) měla aditivní ochranné účinky proti patogenům, což naznačilo, že mechanizmus, kterým brassinolid vyvolá odolnost, je odlišný od jiných protistresových mechanizmů.[36] Rostliny brambor postříkané roztokem brassinosteroidu měly menší výskyt infekce Phytophthora infestans. Zlepšení odolnosti brassinosteroidem ošetřených hlíz bylo spojeno se zvýšením koncentrace kyseliny abscisové a etylenu a přítomnosti fenolických a terpenoidních sloučenin. Brassinosteroidy tedy působí i jako fungicidy. Ale některé koncentrace a aplikace brassinosteroidů v určitých stádiích vývoje mohou růst hub a rozvoj choroby stimulovat. Správná koncentrace, načasování a způsob aplikace jsou tedy důležité předpoklady pokud mají být brassinosteroidy vyvinuty a používány jako fungicidy.[33]
Stres zasolením a přítomností těžkých kovů v substrátu
Brassinosteroidy odvrací také negativní účinky zasolení na rostliny.
24 – epibrassinolid a 28 – homobrassinolid snížily inhibiční vliv soli na klíčení a na růst sazenic rýže.[16] Klíčení semen eukalyptu v roztoku 24-epibrassinolidu bylo zrychlené jen mírně, zatímco za přítomnosti soli bylo výrazně posíleno 24-epibrassinolidem.[37] Vliv brassinosteroidů na ultrastrukturu buněk listů ječmene byl zkoumán při stresu zasolením. Brassinosteroid neměl vliv na buněčnou ultrastrukturu listů v normálních podmínkách, ale výrazně snížil poškození jader a chloroplastů způsobené stresem zasolením.[33] Byla zaznamenána schopnost brassinosteroidů rušit inhibiční účinky zasolení na růst sazenic podzemnice olejné.[16]
Z předchozího textu je jasné, že pozitivní vliv brassinosteroidů na růst a výnos je nápadnější za stresových podmínek v porovnání s optimálními. Brassinosteroidy zlepšují fotosyntetické vlastnosti rostlin a i dalšími mechanizmy výrazně přispívají ke zvýšené odolnosti rostlin k různým stresům. Přitom také spolupracují s ostatními fytohormony a obrannými mechanizmy rostlin. Jak je vidět při odpovědi na patogeny, je i zde důležitá koncentrace a načasování při použití brassinosteroidů.
Závislost struktury a aktivity brassinosteroidů
Brassinolid je polyhydroxylovaný derivát 5α-cholestanu. Základní strukturou je podobný živočišným hormonům odvozených od cholesterolu (androgeny, estrogeny a kortikoidy obratlovců, ekdyson hmyzu a korýšů). Odlišnosti v aktivitě mezi různými brassinosteroidy vychází z rozdílů na C-2 a C-3 v A kruhu, přítomnosti laktonu, ketonu nebo oxo-skupiny na C-6 v B kruhu a prostorovém rozložení hydroxylových skupin na postranním řetězci, přítomnosti nebo nepřítomnosti metylové nebo etylové skupiny na C-24.
Optimální struktura pro nejvyšší biologickou aktivitu je struktura brassinolidu (laktonová funkční skupina na C-6/C-7, sousedící cis hydroxyly na C-2 a C-3, R konfigurace hydroxylů na C-22/C-23 a metyl jako substituent na C-24).[17]
Jedna z největších překážek používání brassinosteroidů v širokém měřítku na polích je jejich vyšší cena. Izolace brassinosteroidů z přírodních materiálů je kvůli jejich nepatrnému množství v nich obsažených velice pracná a nákladná a pro praktické účely nepřichází v úvahu. Syntetická příprava brassinolidu je také velmi nákladná, proto byla syntetizována řada analogů brassinosteroidů, které mají podobné účinky. Pokrok v chemické syntéze brassinosteroidů a jejich analogů vedl k ekonomicky použitelným postupům, které umožnily jejich praktickou aplikaci v zemědělství. Předpokládá se, že brassinosteroidy se budou stále častěji používat pro zvyšování výnosů.
Všechny brassinosteroidy ovšem nejsou biologicky aktivní, nejčastěji se ve fyziologických studiích používá brassinolid, 24-epibrassinolid a 28-homobrassinolid. Pro široké použití v zemědělství je potřeba najít kompromis mezi fyziologickou aktivitou a cenou, proto je vhodné studovat vliv různých brassinosteroidových analogů na růst a vývoj rostlin a to zejména kulturních plodin.[16]
Syntéza a degradace
Biosyntetická dráha syntézy brassinolidu může být rozdělena na syntézu základních sterolů (cycloartenol a z něj campesterol), a specifickou dráhu od campesterolu k brassinolidu. Rostlinné steroly jako např. campesterol jsou integrální složkou membrán, slouží jako regulátory tekutosti a propustnosti membrán a přímo ovlivňují aktivitu membránových proteinů včetně enzymů a složek signálních drah. Mutace v genech kódujících enzymy biosyntetické dráhy sterolů mohou také výrazně ovlivnit vývoj rostliny.[17] Biosyntetická dráha brassinolidu byla poprvé objasněna za použití kultury buněk barvínku (Catharanthus roseus).
Role mutantů
Mutanty můžeme rozdělit na mutanty s nedostatkem brassinosteroidů (deficitní) a mutanty necitlivé k působení brassinosteroidů, u kterých je ovlivněna signální dráha (insenzitivní mutanti). Brassinosteroidové deficitní a insenzitivní mutanti mají mnoho vývojových defektů, mají sníženou klíčivost semen, jsou zakrslí, mají tmavě zelené zakřivené listy, sníženou fertilitu, zpožděný reproduktivní vývoj a ve tmě rostou jako by rostly na světle (de-etiolovaní).[38][39] U deficitních mutantů mohou být tyto defekty kompenzovány přidáním brassinolidu[40] Tyto mutanti jsou důležitým předpokladem pro výzkum jednotlivých kroků biosyntézy.
Biosyntéza základních sterolů
Základní steroly pro biosyntézu brassinosteroidů jsou syntetizovány in vivo z cykloartenolu a ten vzniká ze squalenu. Cykloartenol je první cyklický prekurzor, který se pak postupně mění až na campesterol.
Mutanti huseníčku, jejichž biosyntetická dráha je přerušena v časné fázi syntézy sterolů, mají některé charakteristiky brassinosteroid-deficitních mutantů v dospělosti, ale mají i specifické defekty v embryogenezi.
Biosyntéza campesterolu prochází přes následující meziprodukty:
- squalen
- cykloartenol
- 24-metylen cykloartenol
- episterol
- 5-dehydroepisterol
- 24-metylencholesterol
- campesterol
Cesta od cykloartenolu k 24-metylen cykloartenol vede přes C-24 alkylaci postranního sterolového řetězce. Bylo prokázáno, že 5-dehydroepisterol vzniká v rámci kroku, který zahrnuje zavedení C-5 dvojné vazby do B-kruhu episterolu.[40] Dalším krokem biosyntetické dráhy je přeměna 5-dehydroepisterolu na 24-metylencholesterol pomocí 7 sterol reduktasy.[41] Na konci biosyntetické dráhy sterolů je izomerizace a redukce 24-metylencholesterolu na campesterol.[17]
Biosyntéza brassinolidu z campesterolu
V rostlinách byly zatím objeveny 3 dráhy biosyntézy brassinolidu. Je to biosyntetická dráha C27 brassinosteroidů a dráha syntézy C28 brassinosteroidů, která se dělí na časnou a pozdní C6 oxidační dráhu. Tyto dráhy mohou u některých rostlinných druhů fungovat všechny společně (např. u huseníčku, kde společný výskyt 6-deoxo a 6-oxo forem brassinolidových prekurzorů naznačil spolupůsobení obou drah), jinde je některá z nich převládající. Například cathasteron nebyl detekován v rajčeti a rýži, a proto se zdá, že u těchto rostlin je dominantní pozdní C6 oxidační dráha, zatímco v rajčeti byla zatím dokázána jen pozdní C-6 oxidační dráha (Kim et al., 2004, 2005). Navíc se předpokládá, že pozdní C6 oxidační dráha je hlavním zdrojem brassinolidu v sazenicích huseníčku rostoucích na světle, zatímco časná C6 oxidace může být dominantní ve tmě (Noguchi et al., 2000). Přeměna membránového sterolu campesterolu na brassinolid se děje přes sérii redukcí, hydroxylací, epimerizací a oxidací, které byly důkladně studovány u mnoha rostlinných druhů (Obr.1). První 4 reakce vedou k syntéze campestanolu přes redukci dvojné vazby v campesterolu. Mutant huseníčku det2 je mutantem pro tuto reakci. Gen DET2 má sekvenční identitu k savčím 5α-steroid reduktasám (Li et al., 1996). Aplikace brassinosteroidů může kompenzovat det2 mutanty a vnitrobuněčná koncentrace campestanolu je u nich snížena v porovnání s divokým typem (Fujioka et al., 1997). Det2 má i typický fenotyp brassinosteroidového mutanta, který ovšem oproti cpd a bri1 nemá tak výrazné defekty, což je zřejmě způsobeno zbytkovým campestanolem přítomným v det2. Ten může být vytvářen druhou reduktasou katalyzující stejnou reakci, podobně jako v případě DWF7 i DET2 katalyzuje krok přeměny (24R)-24-metylcholest-4-en-3-onu na (24R)-24-metyl-5α-cholestan-3-on (Noguchi et al., 1999). Mutant sax1 může také ovlivnit přeměnu campesterolu na campestanol. Sax1 má fenotyp brassinosteroidových deficitních mutantů a může být částečně kompenzován ošetřením brassinosteroidy. Nemá ale typický de-etiolovaný fenotyp ve tmě. Sax1 má blokovanou syntézu brassinolidu v kroku předcházejícím det2 a hraje roli v nějaké postranní syntetické dráze přeměny campesterolu na 6-deoxocathasteron přes 22-hydroxylované intermediáty (Ephritikhine et al., 1999). Role sax1 v biosyntéze není tedy jasná tak, jako u ostatních brassinosteroid-deficitních mutantů, kteří byli plně charakterizováni. Od campestanolu se dráha dělí na časnou a pozdní C-6 oxidační větev.
Reakce přeměny campestanolu na 6-deoxocathasteron (pozdní C-6 oxidační dráha) a 6-oxocampestanolu na cathasteron (časná C-6 oxidační dráha) jsou obě katalyzované produktem DWF4 genu, který kóduje cytochrom P450 se sekvenční homologií k savčím steroid hydroxylasám (Choe et al., 1998). Dwf4 mutant může být kompenzován pouze 22α-hydroxylovanými meziprodukty biosyntézy brassinolidů a syntetickými sloučeninami, jako je 22-hydroxycampesterol. Toto dokazuje, že DWF4 funguje jako C-22 steroid hydroxylasa (Clouse, 2002). Nadměrná exprese DWF4 genu způsobí nárůst délky hypokotylu.[14] Další krok obou větví dráhy také zahrnuje postranní hydroxylaci a je katalyzován produktem CPD genu (alelický k CBB3 a DWF3), který kóduje cytochrom P450, který je podobný DWF4. Cpd mutant je extrémně zakrslý a může být kompenzován pouze 23α-hydroxylovanými brassinosteroidy, což dokazuje, že CPD účinkuje jako C-23 steroid hydroxylasa (Szekeres et al., 1996). Tedy C-22 a C-23 pozice brassinosteroidů jsou úspěšně hydroxylovány cytochromy P450, kódovanými geny DWF4 a CPD. Jejich funkce a i jejich DNA sekvence jsou podobné (Asami et al., 2000).
Mutanti, kteří mají blokované kroky biosyntézy za enzymem CPD a mutanti v biosyntéze C27 brassinosteroidů nebyli zatím důkladněji identifikováni (Clouse a Feldmann, 1999). Biosyntéza brassinolidu u huseníčku je pravděpodobně spíš síť než nezávislé lineární dráhy. Je zajímavé, že většina sterol a brassinosteroid-deficitních mutantů byla izolována při výběru mutant, které měly defekty ve fyziologických procesech (zakrslost, konstitutivní fotomorfogeneze ve tmě) nebo defekty embryogeneze. Teprve po klonování jejich genů se ukázalo, že mají defekt v biosyntéze sterolů nebo brassinosteroidů. Pochopení, jak je vnitrobuněčná koncentrace brassinosteroidů regulována přes syntézu a metabolizmus je důležitou součástí mnoha modelů působení brassinosteroidů.[17]
Regulace
Regulace se může vyskytnout na úrovni transkripce, stability mRNA, translace, enzymové aktivity a dostupnosti substrátu. Může být ovlivňována i vnějšími signály a vývojovými podněty jako je světlo a ostatní hormony. Transkripce CPD genu je specificky regulovaná brassinolidem a citlivost k cykloheximidu naznačuje potřebu de novo syntézy regulačního faktoru (Mathur et al., 1998). Množství transkriptů DWF4 je alostericky regulováno vnitrobuněčným obsahem brassinosteroidů. Jeho exprese je velmi nízká v divokém typu huseníčku, ale výrazně stoupá v deficitních mutantech dwf1, bri1 a cpd. To naznačuje, že brassinosteroidové signály jsou potřebné pro snížení exprese DWF4 genu v divokém typu. Reakce katalyzované produkty genu CPD a DWF4 genů pravděpodobně limitují rychlost biosyntézy brassinolidu. Dalším limitujícím krokem je reakce přeměny 6-deoxocastasteronu na castasteron. Ve všech případech je substrát přítomen v buňkách v mnohonásobně větším množství než produkt (Nomura et al., 2001).
Jiný možný mechanizmus regulace je transport brassinosteroidů v rostlinách, který je nejspíš bazipetální, jak je ukázáno ve studiích s brassinosteroidy aplikovanými exogenně (Li a Chory, 1999). Také se spekuluje o tom, ve kterých částech rostliny jsou takto hormony syntetizovány. Například exprese CPD genu byla detekována pouze v kotyledonech rostoucích listů huseníčku. Na druhé straně DET2 je exprimován ve všech orgánech a nezávisle na vývojovém stádiu. Je možné, že exprese může probíhat ve všech orgánech a uplatňují se alosterické regulace závisející na metabolizmu. Brassinosteroidy jsou zřejmě rychleji metabolizovány v listech a pomaleji v kořenech nebo hypokotylech, kde mohou alostericky inhibovat svou biosyntetickou dráhu (Shimada et al., 2003).
Inhibitory biosyntézy
KM-01 byl první známý selektivní brassinosteroidový inhibitor, má však zatím omezené použití.[40]
Dalším nalezeným brassinosteroidovým inhibitorem byl brassinazol (v současné době nejznámější a nejpoužívanější). Jeho struktura je podobná struktuře pacrobutrazolu a uniconazolu (inhibitory biosyntézy gibberelinu) a jedním z cílových míst inhibice je 22-hydroxylační krok přeměny 6-oxocampestanolu na cathasteron a nebo oxidační krok přeměny cathasteronu na teasteron.
Morfologické změny brassinazolem ošetřených rostlin se podobají změnám u det2 mutantů. Rostliny ošetřené brassinazolem jsou zakrslé s kadeřavými, tmavě zelenými listy, mají změněnou fotomorfogenezi (exprimují větší množství fotosyntetických proteinů) a ve tmě vyvíjí pravé listy.
Brassinazol nemá žádný postranní vliv kromě inhibice biosyntézy brassinosteroidů. Limity v použití brassinazolu však jsou. Například při koncentraci 10 µM nebo větší nemůže být morfologie ošetřených rostlin úplně kompenzována pomocí brassinolidu. Také rostliny větší než huseníček (rajče nebo okurka) potřebují vyšší množství brassinazolu, což může být způsobeno problémy se vstřebáváním brassinazolu nebo s jeho pohybem v rostlině.[40][42][43]
Brassinazol 2001 a brassinazol 220, jsou další triazolové inhibitory brassinosteroidové biosyntézy, s podobnými, ale silnějšími a specifičtějšími účinky než má brassinazol. Imazalil (fungicid) by mohl být také jedním z brassinosteroidových inhibitorů, ale imazalilem inhibovaný růst hypokotylu je možno plně obnovit pouze aplikací kombinace 24-epibrassinolidu a gibberelinu a je také pětkrát méně aktivní než brassinazol.[44]
Degradace brassinosteroidů v rostlinách
Metabolizmus brassinosteroidů byl studován na různých rostlinných druzích a mnoho typů metabolitů bylo již bylo identifikováno jako produkty degradace nebo inaktivace (hydroxylací, oxidací, glykosylací, acylací, nebo degradací postranního řetězce). Nejčastějším produktem 24-epibrassinolidu byl 25-hydroxy-24-epibrassinolid a 25-β-D-glukosyloxy-24-epibrassinolid.[17]
Brassinolid ve fazolových explantátech byl metabolizován na jeho 23-O-β-glukosid. V rýžových explantátech a sazenicích byl exogenně aplikovaný brassinolid metabolizován na neznámé polární ale neglykosidické metabolity. 24-epimery brassinolidu a castasteronu jsou přeměňovány na různé metabolity a jejich konjugáty v suspenzní kultuře buněk rajčete. Mezi metabolity fazolu byl brassinolid bez 26- a 28-metylových skupin, který byl identifikován jako 26-norbrassinolid. Vzniká pomocí brassinolid demetylasy. U mnohých podobných experimentů ani produkty metabolizmu nebyly přesně určeny (Kim et al., 2000b).
Interakce brassinosteoidů s ostatními fytohormony
Dříve byly brassinosteroidy považovány pouze za růstové regulátory spolu s polyaminy, kyselinou jasmonovou, oligosacharidy nebo některými fenolickými látkami, ale díky objevení brassinosteroidových mutantů huseníčku a hrachu byly na konferenci v Japonsku v roce 1998 zařazeny mezi fytohormony, vedle již uznávaných pěti skupin hormonů (auxiny, gibberelliny, cytokininy, kyselina abscisová a etylen).
Mechanizmus jejich působení se od účinku ostatních fytohormonů liší a není na nich závislý.[16] Interakce mezi hormony je však základem pro koordinaci rostlinného vývoje.
Mnoho vývojových procesů, které jsou ovlivněny brassinosteroidy, je zároveň řízeno i dalším hormonem – auxinem (prodlužování stonku a kořenů, klíčení semen, apikální dominance aj.). Brassinosteroidové a auxinové signální dráhy se sbíhají na úrovni transkripčních regulací cílových genů.
Oba hormony mají ale jinou kinetiku působení. U soji (Glycine max) např. brassinolid stimuloval prodlužování epikotylu 45 min po aplikaci a tato stimulace dosáhla vrcholu po několika hodinách. Odpověď rostliny na auxin byla naopak relativně rychlá, začala po 10–15 min a gradovala po 30–45min. Podobná kinetika byla také nalezena na úrovni genové regulace u huseníčku.
Brassinosteroidy jsou závislé na změnách poměru auxinu/cytokininu v rostlinných tkáních. Vzrůst obsahu auxinu v rostlinných buňkách po exogenní aplikaci brassinosteroidů a biosyntetické expresi genů byl následován významným poklesem koncentrace cytokininu nebo zvýšením degradace cytokininu v transformovaných rostlinách tabáku.[15] Většina prací popisuje stimulaci syntézy etylenu po aplikaci brassinosteroidů, např. u etiolovaných rostlin vigny (Vigna radiata). Bylo popsáno i snížení hladiny kyseliny abscisové po aplikaci 24-epibrassinolidu v etiolovaných hypokotylech tykve (http://chemicke-listy.vscht.cz).
Vliv aplikace exogenních brassinosteroidů na endogenní hladiny kyseliny abscisové je velmi různorodý, na jedné straně po aplikaci 24-epibrassinolidu dochází ke zvýšení hladiny kyseliny abscisové v rostlinách bavlníku (Gossypium hirsutum) a v hypokotylech okurky (Cucumis sativus), na druhé straně bylo popsáno snížení hladiny kyseliny abscisové po aplikaci 24-epibrassinolidu v etiolovaných hypokotylech tykve (Cucurbita pepo).[15]
Dormance semen a jejich klíčení jsou regulovány kyselinou abscisovou a gibbereliny. Tyto dva hormony spolu účinkují antagonisticky. Kyselina abscisová indukuje dormanci semen a inhibuje jejich klíčení. Gibberelliny tuto dormanci přerušují. V práci Stebera a Mc Courta (2001)[45] je dokázáno, že 24-epibrassinolid obnoví klíčení mnoha gibberelinových biosyntetických mutantů a gibberelinového insenzitivního mutanta sly1. Autoři také zjistili, že klíčení brassinosteroidového deficitního mutanta huseníčku det2-1 a brassinosteroidového insenzitivního mutanta bri1-1 je silněji inhibováno kyselinou abscisovou, než klíčení divokého typu. Brassinosteroidy stimulují klíčení a jejich signál je nejspíš potřebný při překonávání inhibice, která je vyvolaná kyselinou abscisovou. Částečná kompenzace klíčení v gibberelinových mutantech pomocí 24-epibrassinolidu může být ale způsobena stimulací růstu hypokotylu, a tím i růstu embrya v klíčícím semeni. Stále tedy není zodpovězena otázka, zda mají brassinosteroidy esenciální roli při klíčení semen. Pokud ano, tak můžeme očekávat, že bude získán neklíčící fenotyp i mezi brassinosteroidovými mutanty.[45] Společná aplikace gibberelinu a brassinolidu na rostliny begónie (Tabebuia alba) snížila koncentraci kyseliny abscisové v postranních pupenech, což vedlo k jejich vývoji. Ošetření begónie gibberelinem a následně brassinolidem působilo výrazně pozitivně na růst stonku sazenic, ale ošetření samotným brassinolidem velký vliv nemělo. Aplikace brassinolidu samotného nebo v kombinaci s gibberelinem způsobila nárůst tloušťky listové čepele. Gibberelin a brassinosteroidy působí na stejné růstové a vývojové procesy, a to zřejmě aditivně.[15]
Brassinosteroidy a gibbereliny působily aditivně také na růst epikotylů fazolu. Jejich růstově regulační vliv byl pozorován také na odříznutých segmentech hypokotylu okurky, obě látky aditivně podpořily růst[14] Aplikace 24-epibrassinolidu obnovila citlivost huseníčkových hypokotylových buněk ke gibberelinu. Nedávné zprávy o deficitních mutantech dwf4 a sax1 podaly důkaz, že plně aktivní brassinosteroidová biosyntetická dráha je potřebná pro plnohodnotnou gibberelinovou odpověď[44]
Testovací systémy (biotesty)
Počáteční studie brassinosteroidů byly zaměřeny na jejich schopnost stimulovat růst. Byly vyvinuty dva testovací specifické systémy a citlivé k brassinosteroidům. Jsou to test druhého fazolového internodia (second bean internode test) a test odchylky jazýčku rýže (rice lamina inclination test).
Test druhého fazolového internodia byl vyvinut při první izolaci brassinolidu z pylu řepky. Yopp et al., (1979) zjistili, že účinky brassinolidu jsou odlišné od účinků jiných hormonů při testech využívajících hákovité stáčení a prodlužovací růst hypokotylů fazolu v testu druhého fazolového internodia. Uřízlá druhá internodia ze sazenic fazolu (Phaseolus vulgaris), které byly ošetřeny brassinolidem v lanolinové pastě, se prodlužovala, zakřivovala, bobtnala nebo se rozdělovala. Síla těchto jevů závisela na množství brassinolidu. Při nižších koncentracích brassinolid vyvolal prodlužovací růst, zakřivování a bobtnání internodií a při vyšších koncentracích vyvolával rozdělování internodií (Yokota, 1999). Při tomto testu jsou pouze brassinosteroidy schopné vyvolat rozdělení internodia, ostatní rostlinné hormony ho nevyvolají. Další zkoušky citlivosti k brassinosteroidům také využívají růstu internodií.[46]
Test odchylky jazýčku rýže byl původně vyvinut při testování auxinu. Je při něm zjišťováno odklonění čepele listu rýže. Ta se odklání proto, že buňky na adaxiální straně jazýčku se selektivně prodlužují jako odpověď na auxin, zatímco ty na abaxiální straně jsou k němu méně citlivé. Použitím této metody testování byl zkoumán rozdíl biologické aktivity brassinolidu a auxinu. Úhel odchýlení vyvolaný 5,7×10−5 M auxinem byl shodný s úhlem vyvolaným 2×10−9 M brassinolidem, což dokazuje, že brassinolid je v tomto testu aktivní v koncentracích 1000krát menších než auxin (Fuji and Saka, 2001).
Další vysoce citlivé testy jsou založeny např. na inhibici růstu etiolovaných sazenic hrachu (Pisum sativum).[46]
Odkazy
Poznámky
- ↑ v Číně byl 28-homobrassinolid registrován jako růstový regulátor pro tabák, cukrovou třtinu, čajovník, ovocné stromy a řepku, v Rusku byl 24-epibrassinolid registrován jako růstový regulátor brambor, rajčat, okurek, pepře a ječmene a i v dalších zemích jsou brassinosteroidy využívány v zemědělství)
Reference
V tomto článku byl použit překlad textu z článku Brassinosteroid na anglické Wikipedii.
- ↑ a b Mitchell JW, Mandava NB, Worley JF, Plimmer JR, Smith MV. 1970 "Nature" 281: 216–217
- ↑ Grove, M.D., Spencer, G.F., Rohwedder, W.K., Mandava, N., Worley, J.F., Warthen, J.D., Ste€ens, G. L., Flippen-Anderson, J.L. and Cook, J.C. 1979. Brassins:a new family of plant hormones from rape pollen Nature 225:1065–66
- ↑ GROVE, Michael D.; SPENCER, Gayland F.; ROHWEDDER, William K.; MANDAVA, Nagabhushanam; WORLEY, Joseph F.; WARTHEN, J. David; STEFFENS, George L. Brassinolide, a plant growth-promoting steroid isolated from Brassica napus pollen. Nature. 1979, roč. 281, s. 216–217. DOI 10.1038/281216a0.
- ↑ Bajguz, A. 2007. Metabolism of brassinosteroids in plants. Plant Physiology and Biochemistry 45: 95-107
- ↑ a b c Clouse SD, Sasse JM. 1998. Brassinosteroids: Essential regulators of plant growth and development. Annu. Rev. Plant Physiol. Plant Mol. Biol. 49:427–51
- ↑ Nemhauser et al. 2004. Interdependency of Brassinosteroid and Auxin Signaling in Arabidopsis. PLoS Biology
- ↑ Cano-Delgado A, 2004. BRL1 and BRL3 are novel brassinosteroid receptors that function in vascular differentiation in Arabidopsis. Development 131 :5341-5351
- ↑ Hewitt FR, et al. 1985. Effect of brassinolide and other growth regulators on the germination and growth of pollen tubes of "Prunus avium" using a multiple hanging drop assay. Aust. J. Plant Physiol. 12:201–11
- ↑ Yokota, 1999
- ↑ Khripach et al., 1997
- ↑ a b Kim et al., 2000a
- ↑ a b Bajguz a Tretyn, 2003
- ↑ Friedrichsen et al., 2000
- ↑ a b c d e f g h i j Müssig, 2005
- ↑ a b c d Ono et al., 2000
- ↑ a b c d e f g h i j k Rao et al., 2002
- ↑ a b c d e f g h i j Clouse, 2002
- ↑ Morillon et al., 2000
- ↑ Kim et al., 2000b
- ↑ Yokota et al., (2001)
- ↑ Fujii a Saka 2001
- ↑ a b Khripach et al., 2000
- ↑ Hayat et al., 2000
- ↑ a b Peng et al., 2003
- ↑ Yu et al., 2004
- ↑ a b c (Mazorra et al., 2002)
- ↑ a b c d Dhaubhadel et al., 2002
- ↑ a b Yu et al., 2002
- ↑ He et al., 1991
- ↑ Katsumi et al., 1991
- ↑ Dhaubhadel et al., 1999
- ↑ Kulaeva et al., 1991
- ↑ a b c d Krishna, 2003
- ↑ Sairam 1994
- ↑ Morillon et al., 2001
- ↑ Nakashita et al., 2003
- ↑ Sasse, 1999
- ↑ Wang a He, 2004
- ↑ Bishop a Koncz, 2002
- ↑ a b c d Asami a Yoshida, 1999
- ↑ Choe et al., 2000
- ↑ Asami et al., 2000
- ↑ Nagata et al., 2000
- ↑ a b Werbrouck et al., 2003
- ↑ a b Steber a Mc Court, 2001
- ↑ a b Kohout et al., 1991
Externí odkazy
Média použitá na této stránce
Brassinolide