Bromid vápenatý
| Bromid vápenatý | |
|---|---|
 | |
| Obecné | |
| Systematický název | Bromid vápenatý |
| Anglický název | Calcium bromide |
| Německý název | Calciumbromid |
| Sumární vzorec | CaBr2 |
| Vzhled | Bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 7789-41-5 |
| 22208-73-7 (dihydrát) 13477-28-6 (hexahydrát) | |
| PubChem | 24608 |
| Číslo RTECS | EV9328000 |
| Vlastnosti | |
| Molární hmotnost | 199,89 g/mol 307,98 g/mol (hexahydrát) |
| Teplota tání | 730 °C 38,2 °C (hexahydrát) |
| Teplota varu | 810 °C |
| Teplota rozkladu | 149 °C (hexahydrát, dehydratace -6 H2O) |
| Hustota | 3,353 g/cm3 2,295 g/cm3 (hexahydrát) |
| Rozpustnost ve vodě | 125,2 g/100 g (0 °C) 132 g/100 g (10 °C) 143 g/100 g (20 °C) 153 g/100 g (25 °C) 213 g/100 g (40 °C) 278 g/100 g (60 °C) 295 g/100 g (80 °C) 312 g/100 g (105 °C) Hexahydrát 593,2 g/100 g (0 °C) 1 003,6 g/100 g (20 °C) |
| Rozpustnost v polárních rozpouštědlech | Methanol 50,4 g/100 g (0 °C) 56,2 g/100 g (20 °C) 97,8 g/100 g (60 °C) Aceton 2,72 g/100 g (20 °C) Glycerol Ethanol |
| Relativní permitivita εr | 6,15 |
| Měrná magnetická susceptibilita | −4,51·10−6 cm3g−1 −5,69×10−6 cm3g−1 (hexahydrát) |
| Struktura | |
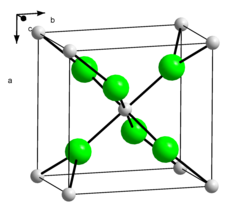
| Krystalová struktura | kosočtverečná šesterečná (hexahydrát) |
| Hrana krystalové mřížky | a= 655 pm b= 688 pm c= 434 pm Hexahydrát a= 797 pm b= 397 pm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −674,9 kJ/mol −2 500 kJ/mol (hexahydrát) |
| Entalpie rozpouštění ΔHrozp | −520,3 J/g −14,9 J/g (hexahydrát) |
| Standardní molární entropie S° | 130 JK−1mol−1 304,7 JK−1mol−1 (hexahydrát) |
| Standardní slučovací Gibbsova energie ΔGf° | −656,5 kJ/mol −2 118,9 kJ/mol (hexahydrát) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R36/37/38 |
| S-věty | S26, S36 |
| NFPA 704 | |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Bromid vápenatý je vápenatá sůl kyseliny bromovodíkové, chemický vzorec má CaBr2. V tuhém stavu se jedná o bílé, silně hygroskopické krystalky. Je velmi dobře rozpustná ve vodě a o hodně lépe je rozpustný její hexahydrát. Dobře rozpustná je také v methanolu a poměrně málo i v acetonu.
Používá se v řezných kapalinách, léčivech, mrazicích směsích, potravinářských konzervantech, ve zpomalovačích hoření a v oblasti fotografie.[2]
CaBr2 lze připravit například reakcí oxidu vápenatého s kyselinou bromovodíkovou nebo reakcí kovového vápníku s elementárním bromem.
Při silném zahřívání CaBr2 na vzduchu vzniká oxid vápenatý a brom:
- 2 CaBr2 + O2 → 2 CaO + 2 Br2
V této reakci dochází k oxidaci bromidu na brom.
Reference
V tomto článku byl použit překlad textu z článku Calcium bromide na anglické Wikipedii.
- ↑ a b Calcium bromide. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Chemical Land 21 [online]. [cit. 2008-12-25]. Dostupné online. (anglicky)
Externí odkazy
- MSDS - Calcium bromide hydrate Archivováno 4. 3. 2016 na Wayback Machine
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.
Autor: Orci, data source: American-Mineralogist-Crystal-Structure-Database - Hydrophilit, Licence: CC BY-SA 3.0
Crystal structure of en:Calcium choride






