Chimerní antigenní receptor
Arteficiální T buněčné receptory (známé také jako chimerní T buněčné receptory, dimerní T receptory, chimerní antigenní receptory - CARs) jsou receptory, které jsou navrženy tak, aby přenesly libovolnou antigenní specifičnost na imunní efektorovou buňku. Tyto receptory jsou užity k přenosu specificity monoklonální protilátky na T buňku, s přenosem jeho kódovací sekvence napomáhá retrovirový vektor. Tímto způsobem můžeme vytvořit velký počet nádorově specifických T buněk.[1] Již během první fáze klinických studií CARs se ukázala účinnost těchto přístupů.
Anatomie CARů
Nejčastější formou těchto molekul jsou splynuté jednoduché řetězce variabilních fragmentů (scFV), odvozených od monoklonálních protilátek, připojené k CD3-zeta transmembránové části a endodoméně. Tyto molekuly přenášejí signál zeta, jako odpověď na rozpoznání cílové molekuly pomocí scFV. Příkladem takového konstruktu je 14g2a-Zeta, kde jsou připojeny scFV odvozené od hybridomu 14g2a (který rozpoznává disialogangliosid GD2). Když T buňky exprimují tuto molekulu (obvykle v důsledku transdukce onkoretrovirovým vektorem) rozpoznává a zabijí cílovou buňku, která exprimuje GD2 (např. neuroblastomové buňky). K zacílení maligních B buněk je využíváno CAR-modifikovaných T buněk, které rozpoznávají specifické molekuly pro B buněčné linie, např. CD 19.
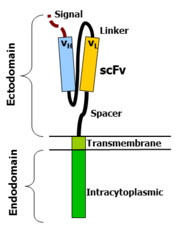
Variabilní části na těžkém a lehkém řetězci imunologlobinu jsou spojeny pomocí flexibilního linkeru do formy scFV. scFV má k sobě připojen signální peptid k řízení vznikajícího peptidu do endoplazmatického retikula a jeho následné expresi (je štěpen). Flexibilní spacer umožňuje scFV orientovat se v různých směrech, což umožňuje vazbu k antigenu. Transmembránová doména je typicky hydrofobní alfa-helix struktura, odvozena z původní molekuly signální endodomény, která vyčnívá do buňky a přenáší požadovaný signál.
Skutečnost, že tyto molekuly skutečně fungují, je na první pohled překvapující. Na druhý pohled si uvědomíme, že bílkovina typu I jsou de facto dvě bílkovinné domény spojeny transmembránovým alfa-helixem. Lipidovou dvouvrstvou prochází transmembránová doména, která od sebe izoluje vnější část (ektodoména, z ang.: ectodomain) od vnější části (endodoména, z ang.: endodomain). Není tedy už překvapením, že propojením ektodomény z jednoho proteinu k endodoméně druhého proteinu vznikne molekula, která je schopna rozpoznat svůj cíl a následně přenést signál do buňky.
Pro lepší pochopení dané problematiky, budou jednotlivé složky tohoto systému probrány jednotlivě:
Ektodoména – signální peptid
Signální peptid řídí vznikající protein v endoplasmatickém retikulu. Je to důležité, jestliže má být receptor glykosilovaný a ukotvený v buněčné membráně. Eukaryotické signální peptidy obvykle dobře fungují. Obecně platí, že ve většině případů je signální peptid přirozeně připojen k NH2 konci (např. u scFV se orientuje: lehký řetězec – linker – těžký řetězec).
Ektodoména – rozpoznání
Jako antigen rozpoznávající doména slouží obvykle scFV, ale existuje však mnoho alternativ. Například u nativního TCR alfa a beta řetězce byla antigen rozpoznávací doména popsána jako jednoduchá ektodoména (např. CD 4 ektodoména k rozpoznání buňky nakažené HIV), ale bylo též popsáno mnoho dalších, více exotických rozpoznávajících komponentů, jako je např. navázaný cytokin (které rozpoznávají buňky, které nesou receptor pro daný cytokin). Jako antigen rozponávající region můžeme použít cokoli, co váže cílovou molekulu s dostatečnou afinitou.
Ektodoména – spacer
Spacer váže antigen-vázající doménu k transmembránové doméně. Měla by být dostatečně flexibilní, aby zaručila, že se antigen-vazebná doména může orientovat v různých směrech a tím usnadnit rozpoznání antigenu. Nejjednodušší formou je tzv. hinge region z IgG1. Alternativou je CH2CH3 region z imunoglobulinu, nebo části z molekuly CD3. Pro většinu scFV konstruktů je tzv. hinge region z molekuly IgG1 dostatečný. Nicméně nejlepší spacer musí být stanoven empiricky.
Transmembránová doména
jedná se o hydrofobní alfa-helix, který prochází buněčnou membránou. Obecně se používají transmembránové domény z nejproximálnějších membránových částí endodomén. Zajímavé je, že užití CD3-zeta transmembránové domény má za následek inkorporaci artificiálního TCR do nativního TCR, faktoru, který je dependentní na přítomnosti nabitého zbytku kyseliny aspartamové transmembránového nativního CD3-zeta.[2] Rozdílné transmembránové domény mají za následek rozdílnou receptorovou stabilitu. CD28 transmembránová doména má za následek jasnou expresi a stabilní receptor.
Endodoména
Jedná se o koncovou část. Po rozpoznání antigenu se receptory shlukují a přenášejí signál do vnitra buňky. Nejčastěji používanou endodoménou je CD3-zeta, která obsahuje tři molekuly ITAM. Slouží jako přenašeč signálu T buňkám po navázání antigenu. CD3-zeta však nemusí vždy poskytovat zcela dostačující signál k aktivaci, a je nutné přidat ještě další kostimulační signály. Například je možné použít chimerní CD28 nebo OX40 společně s CD3-zeta k přenosu signálu k proliferaci, či k přežití buňky. V některých případech lze kombinovat všechny tři molekuly dohromady.
Evoluce v projektování T buněčných CARů
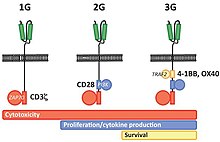
První generace CARů zpravidla měla intracelulární doménu z CD3ξ řetězce, který sloužil jako primární vysílač signálů z endogenních TCR. U Druhé generace CARů byly přidány do cytoplazmatických částí CARů intracelulární signální domény z různých kostimulačních receptorů (např. CD28, 41BB, ICOS), které poskytovali další signály T buňkám. V případě Druhé generace CARů, předklinické studie poukázaly na to, že dochází u T buněk k posílení protinádorové imunity. Novější Třetí generace CARů již kombinuje různé signalizační domény, jako je CD3-zeta – CD28 – 41BB nebo CD3-zeta – CD28 – OX40.
Klinické studie testující Chimérní antigenní receptory
Tato metoda je založena na reprogramování T buněk vektorem (např. virovým). Buňky následně exprimují chimerické antigenní receptory, které jsou cíleny proti nádorovým buňkám a jejím rozeznáním umožňují jejich následné zničení. Díky tomuto poznatku, se CARs-modifikované T buňky staly středem zájmu vědců z celého světa, kteří se v pre-klinické fázi zajímají o jejich optimalizaci v oblasti struktury a signalizace. V současné době již probíhají klinické studie, které naznačují jisté budoucí využití této metody v léčbě maligních stavů.
První generace CARs-modifikovaných T buněk zaznamenala úspěch během preklinických testů a následně vstoupila do první fáze klinických studií. CARs-modifikované T buňky byly cíleny na ovariální karcinom, neuroblastom a různé typy leukemií a lymfomů (viz tab.). Klinické studie neprokázaly významný klinický přínos a upozornily na nedostatečnou anti-nádorovou aktivitu, poruchu aktivace, nedostatečnou perzistenci a homing do místa nádoru. Jen v několika případech u pacientů s B-lymfomem (léčených αCD20-CD3ζ CAR-modifikovanými T-buňkami) a neuroblastomem (léčených ScFv-CD3ζ CAR-modifikovanými T buňkami), byla pozorována částečná odpověď - stabilizace stavu, nebo došlo k remisi onemocnění. Druhá a třetí generace CARs-modifikovaných T buněk vedla ke zlepšení aktivačního signálu, zvýšení proliferace, zvýšení produkce cytokinů a celkovému zlepšení efektorových funkcí CAR-modifikovaných T buněk v pre-klinických modelech. Obě dvě tyto generace CARs-modifikovaných T buněk vstoupily do klinických testů. Již první klinické testy naznačují velmi slibné výsledky. Ve studii s αCD19.4-1BB-CD3ζ T buněk u pacientů s chronickou lymfatickou leukemií došlo ke kompletní remisi a u jednoho pacienta k dílčí reakci, která probíhala 10 měsíců po léčbě. Navíc bylo nalezeno zvýšení CAR-modifikovaných buněk o tři řády, které infiltrovali a lyzovali nádorovou tkáň. Zajímavostí je, že některé CARs-modifikované T buňky vykazovaly fenotyp paměťových buněk, což může sloužit jako prevence relapsů onemocnění. Ačkoli tyto modifikované T buňky vykazovaly výrazný terapeutický efekt, jejich cytotoxická činnost vedla k nebezpečnému syndromu z lýzy nádoru, který se vyvinul 3 týdny po podání první infuze CARs-modifikovaných T buněk.
Nedávno zveřejněné vedlejší účinky poukazují na fakt, jak je důležité dbát na opatrnost, při použití CARs-modifikovaných T buněk druhé a třetí generace. Pacient zemřel 5 dnů po cyklofosfamidové chemoterapii, která zahrnovala infuzi modifikovaných T buněk, obsahující část z CD28. Toxicita vedla k nárůstu prozánětlivých cytokinů, plicní toxicitu, multiorgánové selhání a eventuální smrt pacienta. Dalším problémem je tzv. off target cytotoxicita, která vede k autoimunním reakcím, kvůli tomu, že většina tumor-asociovaných antigenů se vyskytuje i na normální tkáni.
Velkým slibem do budoucna je imunoterapie rakoviny, bez toxicity konvenční léčby. Podle pre-klinický a klinických studií CAR-modifikované buňky dávají naději. Léčba touto metodou má několik výhod: rozpoznání cíle nezávislé na HLA antigenech, použitelnost pro většinu pacientů a rychlé dodání buněk. Pro úspěšnou aplikaci těchto buněk bude však nutné identifikovat cílové antigeny vyjádřené na nádorových buňkách, čímž se značně sníží riziko cytotoxicity.[4],[5]
Aktuální seznam tumorových antigenů a CARs uplatněných v in-vitro a in-vivo trudiích [6],[7]:
| Cílový antigen | Související malignita | Typ receptoru | CARs generace |
|---|---|---|---|
| α-Folátový receptor | Nádor vaječníků | ScFv-FcεRIγCAIX | První |
| CAIX | Karcinom renálních buněk | ScFv-FcεRIγ | První |
| CAIX | Karcinom renálních buněk | ScFv-FcεRIγ | Druhá |
| CD19 | B-buněčné malignity | ScFv-CD3ζ (EBV) | První |
| CD19 | B-buněčné malignity, CLL | ScFv-CD3ζ | První |
| CD19 | B-ALL | ScFv-CD28-CD3ζ | Druhá |
| CD19 | ALL | CD3ζ(EBV) | První |
| CD19 | ALL post-HSCT | ScFv-CD28-CD3ζ | Druhá |
| CD19 | Leukemie, lymfom, CLL | ScFv-CD28-CD3ζ vs. CD3ζ | První and Druhá |
| CD19 | B-buněčné malignity | ScFv-CD28-CD3ζ | Druhá |
| CD19 | B-buněčné malignity post-HSCT | ScFv-CD28-CD3ζ | Druhá |
| CD19 | Refractorní folikulární lymfom | ScFv-CD3ζ | První |
| CD19 | B-NHL | ScFv -CD3ζ | První |
| CD19 | B-liniová lymfoidní malignity post-UCBT | ScFv-CD28-CD3ζ | Druhá |
| CD19 | CLL, B-NHL | ScFv-CD28-CD3ζ | Druhá |
| CD19 | B buněčné malignity, CLL, B-NHL | ScFv-CD28-CD3ζ | Druhá |
| CD19 | ALL, lymfom | ScFv-41BB-CD3ζ vs CD3ζ | První and Druhá |
| CD19 | ALL | ScFv-41BB-CD3ζ | Druhá |
| CD19 | B-buněčné malignity | ScFv-CD3ζ (Influenza MP-1) | První |
| CD19 | B-buněčné malignity | ScFv-CD3ζ (VZV) | První |
| CD20 | Lymfomy | ScFv-CD28-CD3ζ | Druhá |
| CD20 | B-buněčné malignity | ScFv-CD4-CD3ζ | Druhá |
| CD20 | B-buněčné lymfomy | ScFv-CD3ζ | První |
| CD20 | Mantle cell lymfom | ScFv-CD3ζ | První |
| CD20 | Mantle cell lymfom, indolent B-NHL | CD3 ζ /CD137/CD28 | Třetí |
| CD20 | indolent B-cell lymphomas | ScFv-CD28-CD3ζ | Druhá |
| CD20 | Indolentní B-buněčný lymfomy | ScFv-CD28-41BB-CD3ζ | Třetí |
| CD22 | B-buněčné malignity | ScFV-CD4-CD3ζ | Druhá |
| CD30 | Lymfomy | ScFv-FcεRIγ | První |
| CD30 | Hodgkinův lymfom | ScFv-CD3ζ (EBV) | První |
| CD33 | AML | ScFv-CD28-CD3ζ | Druhá |
| CD33 | AML | ScFv-41BB-CD3ζ | Druhá |
| CD44v7/8 | Cervikální karcinom | ScFv-CD8-CD3ζ | Druhá |
| CEA | Breast cancer | ScFv-CD28-CD3ζ | Druhá |
| CEA | Kolorektální karcinom | ScFv-CD3ζ | První |
| CEA | Kolorektální karcinom | ScFv-FceRIγ | První |
| CEA | Kolorektální karcinom | ScFv-CD3ζ | První |
| CEA | Kolorektální karcinom | ScFv-CD28-CD3ζ | Druhá |
| CEA | Kolorektální karcinom | ScFv-CD28-CD3ζ | Druhá |
| EGP-2 | Mnohočetné malignity | scFv-CD3ζ | První |
| EGP-2 | Mnohočetné malignity | scFv-FcεRIγ | První |
| EGP-40 | Kolorektální karcinom | scFv-FcεRIγ | První |
| erb-B2 | Kolorektální karcinom | CD28/4-1BB-CD3ζ | Třetí |
| erb-B2 | Karcinom prsu | ScFv-CD28-CD3ζ | Druhá |
| erb-B2 | Karcinom prsu | ScFv-CD28-CD3ζ (Influenza) | Druhá |
| erb-B2 | Karcinom prsu | ScFv-CD28mut-CD3ζ | Druhá |
| erb-B2 | Nádor prostaty | ScFv-FcεRIγ | První |
| erb-B 2,3,4 | Karcinom prsu | Heregulin-CD3ζ | Druhá |
| erb-B 2,3,4 | Karcinom prsu | ScFv-CD3ζ | První |
| FBP | Nádor vaječníků | ScFv-FcεRIγ | První |
| FBP | Nádor vaječníků | ScFv-FcεRIγ (alloantigen) | První |
| Fetalní acethylcholinový receptor | Rhabdomyosarkom | ScFv-CD3ζ | První |
| GD2 | Neuroblastom | ScFv-CD28 | První |
| GD2 | Neuroblastom | ScFv-CD3ζ | První |
| GD2 | Neuroblastom | ScFv-CD3ζ | První |
| GD2 | Neuroblastom | ScFv-CD28-OX40-CD3ζ | Third |
| GD2 | Neuroblastom | ScFv-CD3ζ (VZV) | První |
| GD3 | Melanom | ScFv-CD3ξ | První |
| GD3 | Melanom | ScFv-CD3ξ | První |
| Her2/neu | Medulloblastom | ScFv-CD3ξ | První |
| Her2/neu | Plicní malignity | ScFv-CD28-CD3ζ | Druhá |
| Her2/neu | Pokročilý osteosarkom | ScFv-CD28-CD3ζ | Druhá |
| Her2/neu | Glioblastom | ScFv-CD28-CD3ζ | Druhá |
| IL-13R-a2 | Gliom | IL-13-CD28-4-1BB-CD3ζ | Třetí |
| IL-13R-a2 | Glioblastom | IL-13-CD3ζ | Druhá |
| IL-13R-a2 | Medulloblastom | IL-13-CD3ζ | Druhá |
| KDR | Vaskulární tumory | ScFv-FcεRIγ | First |
| k-light chain | B-buněčné malignity | ScFv-CD3ζ | První |
| k-light chain | (B-NHL, CLL) | ScFv-CD28-CD3ζ vs CD3ζ | Druhá |
| LeY | Karcinomy | ScFv-FcεRIγ | První |
| LeY | Epiteliální tumory | ScFv-CD28-CD3ζ | Druhá |
| L1 cell adhesion molecule | Neuroblastom | ScFv-CD3ζ | First |
| MAGE-A1 | Melanom | ScFV-CD4-FcεRIγ | Druhá |
| MAGE-A1 | Melanom | ScFV-CD28-FcεRIγ | Druhá |
| Murine CMV infected cells | Murine CMV | Ly49H-CD3ζ | Druhá |
| MUC1 | Nádory prsu a vaječníků | ScFV-CD28-OX40-CD3ζ | Třetí |
| NKG2D ligands | Různé tumory | NKG2D-CD3ζ | First |
| Oncofetal antigen (h5T4) | Různé tumory | ScFV-CD3ζ (vaccination) | První |
| PSCA | Prostate carcinoma | ScFv-b2c-CD3ζ | Druhá |
| PSMA | Prostatické a cévní tumory | ScFv-CD3ζ | První |
| PSMA | Prostatické a cévní tumory | ScFv-CD28-CD3ζ | Druhá |
| PSMA | Prostatické a cévní tumory | ScFv-CD3ζ | První |
| TAA targeted by mAb IgE | Různé tumory | FceRI-CD28-CD3ζ (+ a-TAA IgE mAb) | Třetí |
| TAG-72 | Adenocarcinom | scFv-CD3ζ | První |
| VEGF-R2 | Vaskulární tumory | scFv-CD3ζ | První |
Zlepšení bezpečnosti adoptivního přenosu CAR-modifikovaných buněk jako terapie rakoviny
Adoptivní přenos buněk, které exprimují chimerní antigenní receptory, jsou považovány za slibné protirakovinné terapeutikum. CAR-modifikované buňky mohou být navrženy tak, aby byly cíleny proti některým tumor-asociovaných antigenům a díky tomu mohou být specificky cíleny individuálně pro každého pacienta. Díky tomu se jedná se o slibnou terapeutickou metodu léčby rakoviny.
Poté, co jsou pacientovi odebrány T-buňky, jsou geneticky upraveny k expresi CARů, konkrétně zaměřených proti pacientovým nádorovým antigenům. Následně jsou připraveny k infúzi zpět do těla pacienta.[8] Ačkoli adoptivní přenos CAR-modifikovaných buněk je jedinečným a perspektivním léčebným prostředkem rakoviny, existují významné obavy o bezpečnost této metody. Klinické studie této terapie ukázaly potenciální toxické účinky CARů, když zdravé tkáně exprimují stejné cílové antigeny jako jsou obsaženy v nádorových buňkách, což vede ke stavům podobným graft-versus-host disease(GvHD). Potenciálním řešením tohoto problému je sestrojení sebevražedného genu, který by byl vložen do modifikovaných T-buněk. Touto cestou by došlo ke spuštění sebevražedných genů v aktivovaných CAR-modifikovaných T-buněk. Tato metoda byla již bezpečně a efektivně při transplantaci hematopoetických kmenových buněk (HSCT). V současné době jsou sebevražedné geny podrobeny klinickým testum, pro svůj potenciál zmírnění těchto vedlejších účinků při současném zvýšení protinádorových účinků.[3]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Chimeric antigen receptor na anglické Wikipedii.
- ↑ PULE, M, Finney H, Lawson A. Artificial T-cell receptors. Cytotherapy. 2003, s. 211–26. DOI 10.1080/14653240310001488. PMID 12850789. (anglicky)
- ↑ BRIDGEMAN, JS, Hawkins RE, Bagley S, Blaylock M, Holland M, Gilham DE. The Optimal Antigen Response of Chimeric Antigen Receptors Harbouring the CD3zeta Transmembrane Domain Is Dependent Upon Incorporation of the Receptor Into the Endogenous TCR/CD3 Complex. Journal of Immunology. 2010, s. 6938–49. DOI 10.4049/jimmunol.0901766. PMID 20483753. (anglicky)
- ↑ a b CASUCCI, Monica, Attilio Bondanza. Suicide Gene Therapy to Increase the Safety of Chimeric Antigen Receptor-Redirected T Lymphocytes. Journal of Cancer. 2011, s. 378-382. Dostupné online [cit. 30 April 2012]. PMID 21750689. (anglicky)
- ↑ CURRAN, Kevin J., Pengram Hollie J, Brentjens Renier J. The promise and potential. J Gene Med. 2012, s. 405–415. Dostupné online [cit. 5 January 2012]. DOI 10.1002/jgm.2604. PMID 22262649. (anglicky)
- ↑ LIPOVSKA-BHALLA, Grazyna, Gilham David E., Hawkins Robert E., Rothwell Dominic G. Target immunotherapy of cancer with CAR T cell: achievements and challenges. Cancer Immunol Immunother. 2012, s. 953–962. Dostupné online [cit. 25 March 2012]. DOI 10.1007/s00262-012-1254-0. PMID 22527245. (anglicky)[nedostupný zdroj]
- ↑ LIPOWSKA-BHALLA, Grazina, Gilham David E., Hawkins Robert E., Rothwell Dominic G. Target immunotherapy of cancer with CAR T cell: achievements and challenges. Cancer Immunol Immunother. 2012, s. 953–962. Dostupné online [cit. 25 March 2012]. DOI 10.1007/s00262-012-1254-0. PMID 22527245. (anglicky)[nedostupný zdroj]
- ↑ SADELAIN, M., Gilham David E., Hawkins Robert E., Rothwell Dominic G. The promise and potential pitfalls of chimeric antigen receptor. Curr Opin Immunol. 2009, s. 215–223. Dostupné online [cit. April 2009]. DOI 10.1016/j.bbr.2011.03.031. PMID 19327974. (anglicky)
- ↑ JACOBSON, Caron, Jerome Ritz. Time to put the CAR-T before the horse. Blood. 3, s. 4761-4762. Dostupné online [cit. 7 May 2012]. DOI 10.1182/blood-2011-09-376137. PMID 22053170. (anglicky) Archivovaná kopie. bloodjournal.hematologylibrary.org [online]. [cit. 2012-09-12]. Dostupné v archivu pořízeném z originálu.
Externí odkazy
- (anglicky) Historie chimerních antigenních receptorů
Média použitá na této stránce
Depiction of 3 generations of CARs from http://www.jcancer.org/v02p0378.htm
Depiction of adoptive cell therapy using CAR-modified T Cells.