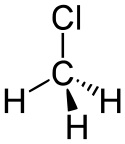
Chlormethan
| Chlormethan | |
|---|---|
 Vzorec | |
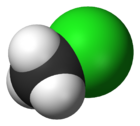 Model molekuly | |
| Obecné | |
| Systematický název | chlormethan |
| Ostatní názvy | monochlormethan, methylchlorid, Freon 40, R-40, UN 1063 |
| Anglický název | Chloromethane |
| Německý název | Chlormethan |
| Sumární vzorec | CH3Cl |
| Vzhled | bezbarvý plyn |
| Identifikace | |
| Registrační číslo CAS | 74-87-3 |
| EC-no (EINECS/ELINCS/NLP) | 200-817-4 |
| PubChem | 6327 |
| ChEBI | 36014 |
| SMILES | CCl |
| InChI | 1/CH3Cl/c1-2/h1H3 |
| Číslo RTECS | PA6300000 |
| Vlastnosti | |
| Molární hmotnost | 50,49 g/mol |
| Teplota tání | −97,7 °C |
| Teplota varu | −24,2 °C |
| Hustota | 2,22 kg/m3 (plyn, 0 °C) |
| Rozpustnost ve vodě | 5,325 g/l |
| Tlak páry | 490 kPa (20 °C) |
| Struktura | |
| Tvar molekuly | čtyřstěnný |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R12 R40 R48/20 |
| S-věty | (S2) S9 S16 S33 |
| NFPA 704 | |
| Teplota vznícení | 625 °C |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Chlormethan (též monochlormethan nebo methylchlorid) je organická sloučenina (nejjednodušší chlorovaný uhlovodík). Používal se jako chladivo známé pod označením R-40 nebo HCC 40. Je to bezbarvý, velmi hořlavý plyn s mírně nasládlou vůní, která je však cítit až při úrovních, které již mohou být toxické. Kvůli obavám z jeho toxicity se již ve výrobcích pro spotřebitele nepoužívá.
Chlormethan poprvé (v roce 1835) syntetizovali francouzští chemici Jean-Baptiste Dumas a Eugene Peligot, když vařili směs methanolu, kyseliny sírové a chloridu sodného. Tato metoda je podobná té dnes používané.
Použití
Chlormethan se široce používal jako chladivo, toto použití však je již minulostí kvůli toxicitě a hořlavosti plynu. Používal se i při výrobě olovnatých aditiv (tetramethylolova) do automobilového benzinu, ve většině průmyslového světa se však již olovnaté benziny nepoužívají (významnou výjimkou jsou však některé státy bývalého Sovětského svazu).
Nejdůležitější dnešní oblastí použití je jako surovina pro výrobu silikonových polymerů. Malá množství se používají jako rozpouštědlo butylové pryže a při rafinaci ropy.
Chlormethan se využívá jako methylační a chlorační činidlo v organické chemii. Používá se i na řadě dalších míst – při extrakci vazelin, olejů a pryskyřic, jako propelent a nadouvadlo při výrobě pěnového polystyrenu, jako lokální anestetikum, při výrobě léčiv, jako nosič katalyzátorů při nízkoteplotní polymeraci, jako tekutina pro měření a regulaci teploty nebo jako herbicid.
Bezpečnost
Vdechování plynného chlormethanu má na centrální nervový systém podobné účinky jako při opilosti. Postižený může cítit ospalost, závratě a otupělost, ztížené dýchání s dušením a lapáním po dechu, motorický neklid a hovornost. Při vyšších koncentracích může nastat paralýza, křeče a kóma.
Při požití se může objevit nausea a zvracení. Kontakt kůže se zkapalněným plynem může způsobit omrzliny. Kontakt s očima může způsobovat zhoršené vidění a široce roztaženou duhovku, která jen pomalu reaguje na změnu světla.
Chronická expozice chlormethanu je spojována s vrozenými poruchami u myší. U člověka může expozice chlormethanu v těhotenství způsobit, že se u plodu nesprávně vyvíjí dolní část páteře, pánev a nohy, ale nebylo to dostatečně prokázáno.
Při opětovném vyšetřování (1997) tragického požáru v bostonském nočním klubu Cocoanut Grove (492 mrtvých, stovky zraněných) byl za hlavní příčinu neštěstí označen únik chlormethanu z chladicího zařízení.
Externí odkazy
 Obrázky, zvuky či videa k tématu chlormethan na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlormethan na Wikimedia Commons - MSDS at Oxford University
- Data sheet at inchem.org
- Toxicological information
- Information about chloromethane
- Silicone manufacturing
- Concise International Chemical Assessment Document 28 on chloromethane
- IARC Summaries & Evaluations Vol. 71 (1999)
Reference
V tomto článku byl použit překlad textu z článku Chloromethane na anglické Wikipedii.
- ↑ a b Chloromethane. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Média použitá na této stránce
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
Chloromethane; methyl chloride
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances