Chlorochroman pyridinia
| Chlorochroman pyridinia | |
|---|---|
 Strukturní vzorec | |
| Obecné | |
| Systematický název | chlorochroman pyridinia |
| Ostatní názvy | Coreyovo–Suggsovo činidlo |
| Funkční vzorec | (C5H6N+)CrO3Cl− |
| Sumární vzorec | C5H6NCrO3Cl |
| Vzhled | žlutooranžová pevná látka[1] |
| Identifikace | |
| Registrační číslo CAS | 26299-14-9 |
| EC-no (EINECS/ELINCS/NLP) | 247-595-5 |
| PubChem | 129695875 |
| ChEBI | 176795 |
| SMILES | C1=CC=[NH+]C=C1.[O-][Cr](=O)(=O)Cl |
| InChI | 1S/C5H5N.ClH.Cr.3O/c1-2-4-6-5-3-1;;;;;/h1-5H;1H;;;;/q;;+1;;;-1 |
| Vlastnosti | |
| Molární hmotnost | 201,55 g/mol |
| Teplota tání | 205 °C (478 K) |
| Rozpustnost v polárních rozpouštědlech | rozpustný v acetonu, acetonitrilu a tetrahydrofuranu |
| Bezpečnost | |
| H-věty | H272 H317 H350 H410 |
| P-věty | P201 P221 P273 P280 P302+352 P308+313 |
Některá data mohou pocházet z datové položky. | |
Chlorochroman pyridinia (zkráceně PCC) je organická sloučenina se vzorcem [C5H5NH]+[CrO3Cl]−. Používá se v organické syntéze na oxidace alkoholů na karbonylové sloučeniny. Jsou známy i jiné obdobné sloučeniny s podobnou reaktivitou;. PCC má výhodu ve větší selektivitě oxidací.[1]
Struktura a příprava
Molekula PCC se skládá z pyridiniového kationtu, [C5H5NH]+, a chlorochromanového aniontu, [CrO3Cl]−. Bylo popsáno i několik podobných solí, například chlorochroman 1-butylpyridinia, [C5H5N(C4H9)][CrO3Cl], a chlorochroman draselný.
PCC je možné zakoupit nebo připravit přidáním pyridinu do chladného roztoku oxidu chromového v koncentrované kyselině chlorovodíkové:[2][3]
- C5H5N + HCl + CrO3 → [C5H5NH][CrO3Cl]
Tvorbu par chromylchloridu (CrO2Cl2) během přípravy uvedeného roztoku lze omezit změnou pořadí přidávání reaktantů, kdy se roztok pyridinu v koncentrované kyselině chlorovodíkové přilévá k pevnému oxidu chromovému za současného míchání.[4]
Použití
Oxidace alkoholů
PCC se používá jako oxidační činidlo, vysoce účinné při oxidacích alkoholů, primárních na aldehydy a sekundárních na ketony. Vykazuje větší selektivitu než podobné Jonesovo činidlo, takže málokdy dochází k oxidaci až na karboxylové kyseliny, pokud se v reakční směsi nenachází voda. Při oxidaci pomocí PCC se alkohol přidává k suspenzi PCC v dichlormethanu.[5][6][7] Obecná rovnice reakce vypadá takto:
- 2 [C5H5NH][CrO3Cl] + 3 R2CHOH → 2 [C5H5NH]Cl + Cr2O3 + 3 R2C=O + 3 H2O
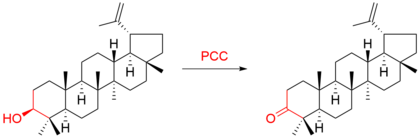
Například triterpen lupeol se oxiduje na lupenon:[8]
Bablerova oxidace
Za přítomnosti terciárního alkoholu se chromátový ester vzniklý z chlorochromanu pyridinia může izomerizovat [3,3]-sigmatropní reakcí a následnou oxidací se vytvořit enon; tato reakce se nazývá Bablerova oxidace:

Tento druh reakce byl například využit při syntéze morfinu.[9]
U jiných běžných oxidačních činidel se často objevují dehydratace, protože tyto alkoholy nelze oxidovat přímo.
Ostatní reakce
PCC také může přeměňovat některé nenasycené alkoholy a aldehydy na cyklohexenony. Tato oxidační kationtová cyklizace může být například využita k přeměně (−)-citronellolu na (−)-pulegon.
PCC také zvyšuje účinnost allylových oxidací, například oxidací dihydrofuranů na furanony.[1]
Podobná činidla
K oxidaci alkoholů se dají použít i dimethylsulfoxid (ve Swernově a Pfitznerově–Moffattově oxidaci) a Dessův–Martinův perjodinan.
Bezpečnost
PCC je, podobně jako další sloučeniny šestimocného chromu, toxický.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Pyridinium chlorochromate na anglické Wikipedii.
- ↑ a b c PIANCATELLI, G.; LUZZIO, F. A. e-EROS Encyclopedia of Reagents for Organic Synthesis. Pyridinium Chlorochromate. [s.l.]: John Wiley & Sons, 2007. ISBN 978-0471936237. DOI 10.1002/9780470842898.rp288.pub2. (anglicky)
- ↑ E. J. Corey; J. W. Suggs. Pyridinium Chlorochromate. An Efficient Reagent for Oxidation of Primary and Secondary Alcohols to Carbonyl Compounds. Tetrahedron Letters. 1975, s. 2647–2650. DOI 10.1016/S0040-4039(00)75204-X.
- ↑ Derek Lowe. The Old Stuff [online]. Science [cit. 2015-11-21]. Dostupné v archivu pořízeném dne 2015-11-21.
- ↑ S. Agarwal; H. P. Tiwari; J. P. Sharma. Pyridinium Chlorochromate: An Improved Method for Its Synthesis and Use of Anhydrous Acetic Acid as Catalyst for Oxidation Reactions. Tetrahedron. 1990, s. 4417–4420. DOI 10.1016/S0040-4020(01)86776-4.
- ↑ PAQUETTE, L. A.; EARLE, M. J.; SMITH, G. F. (4R)-(+)-tert-Butyldimethylsiloxy-2-cyclopenten-1-one. Org. Synth.. 1996, s. 36. Dostupné online. (anglicky); Coll. Vol.. S. 132. (anglicky)
- ↑ TU, Y.; FROHN, M.; WANG, Z.-X.; SHI, Y. Synthesis of 1,2:4,5-Di-O-isopropylidene-D-erythro-2,3-hexodiulo-2,6-pyranose. A Highly Enantioselective Ketone Catalyst for Epoxidation. Org. Synth.. 2003, s. 1. Dostupné online. (anglicky)
- ↑ WHITE, J. D.; GRETHER, U. M.; LEE, C.-S. (R)-(+)-3,4-Dimethylcyclohex-2-en-1-one. Org. Synth.. 2005, s. 108. Dostupné online. (anglicky); Coll. Vol.. S. 100. (anglicky)
- ↑ A. Lao; Y. Fujimoto; T. Tatsuno. Studies on the Constituents of Artemisia argyi Lévl & Vant. Chemical and Pharmaceutical Bulletin. 1984, s. 723–727. Dostupné online [cit. 2016-06-05]. DOI 10.1248/cpb.32.723.
- ↑ =Patrick M. Killoran; Steven B. Rossington; James A. Wilkinson; John A. Hadfield. Expanding the scope of the Babler–Dauben oxidation: 1,3-oxidative transposition of secondary allylic alcohols. Tetrahedron Letters. 2016, s. 3954–3957. Dostupné online. DOI 10.1016/j.tetlet.2016.07.076.
Literatura
- TOJO, G.; FERNÁNDEZ, M. Oxidation of Alcohols to Aldehydes and Ketones: A Guide to Current Common Practice. Redakce Tojo G.. New York: Springer, 2006. (Basic Reactions in Organic Synthesis). ISBN 978-0-387-23607-0. (anglicky)
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Chlorchroman pyridinia na Wikimedia Commons
Obrázky, zvuky či videa k tématu Chlorchroman pyridinia na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for oxidizing substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
Autor: Georginho, Licence: CC BY-SA 4.0
Example of oxidation of a secondary alcohol with pyridinium chlorochromate (PCC). The file was made with ChemBioDraw Ultra 14. The example is taken from the work of Yasuo Fujimoto et al. in 1984: https://dx.doi.org/10.1248/cpb.32.723 (open access). A more modern picture depicting the stereochemistry of lupeol and lupenone can be seen in the work of Chaturvedula Prakash and Indra Prakash in 2012: http://www.isca.in/IJPS/Archive/v1/i1/5.ISCA-RJPcS-2012-009.php (open access).
Structure of pyridinium chlorochromate
Autor: A. T. Galenitis, Licence: CC BY-SA 4.0
The Babler-Dauben oxidation of cyclic tertiary allylic alcohols to cyclic enones using PCC.