1,4-diazabicyklo(2.2.2)oktan
| 1,4-diazabicyklo[2.2.2]oktan | |
|---|---|
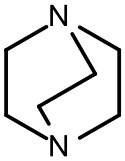 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | 1,4-diazabicyklo[2.2.2]oktan |
| Ostatní názvy | DABCO, triethylendiamin, TEDA |
| Sumární vzorec | C6H12N2 |
| Vzhled | bezbarvé krystaly[1] |
| Identifikace | |
| Registrační číslo CAS | 280-57-9 |
| EC-no (EINECS/ELINCS/NLP) | 205-999-9 |
| PubChem | 9237 |
| ChEBI | 151129 |
| SMILES | C1CN2CCN1CC2 |
| InChI | 1S/C6H12N2/c1-2-8-5-3-7(1)4-6-8/h1-6H2 |
| Vlastnosti | |
| Molární hmotnost | 112,17 g/mol |
| Teplota tání | 158 °C (431 K)[1] |
| Teplota varu | 174 °C (447 K)[1] |
| Hustota | 1,14 g/cm3 (28 °C)[1] |
| Rozpustnost ve vodě | 45 g/100 ml[1] |
| Rozpustnost v polárních rozpouštědlech | 13 g/100 g (aceton) 77 g/100 g (ethanol) 26,1 g/100 g (ethylmethylketon); rozpustný v chloroformu[1] |
| Rozpustnost v nepolárních rozpouštědlech | 51 g/100 g (benzen)[1] |
| Tlak páry | 99 Pa[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H228 H302 H315 H318 H319 H335 H412[1] |
| P-věty | P210 P240 P241 P261 P264 P270 P271 P272 P273 P280 P301+312 P302+352 P304+340 P305+351+338 P310 P312 P321 P330 P332+313 P337+313 P362 P370+378 P403+233 P405 P501[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
1,4-Diazabicyklo[2.2.2]oktan, zkráceně DABCO, je bicyklická organická sloučenina se vzorcem N2(C2H4)3. Jedná se o silně nukleofilní terciární amin, používaný jako katalyzátor a reaktant při polymerizacích a v organické syntéze.[2]
Chinuklidin má podobnou strukturu, která se liší pouze náhradou jednoho dusíkového atomu uhlíkem.
Reakce
pKa iontu [HDABCO]+ (protonované formy) je 8,8, což je podobná hodnota jako u běžných alkylaminů. Aminová skupina je silným nukleofilem, protože aminová centra nejsou stericky narušována. Zásaditost této sloučeniny dostačuje ke spouštění C–C párování koncových alkynů, například fenylacetylen reaguje s jodareny chudými na elektrony.
Katalyzátor
DABCO se používá jako zásaditý katalyzátor při:
- tvorbě polyuretanu z alkoholů a izokyanátových funkcionalizovaných monomerů.[3]
- Baylisových–Hillmanových reakcích aldehydů s nenasycenými aldehydy a ketony.[4]
Lewisovy zásady
DABCO je silným ligandem a Lewisovou zásadou. Vytváří krystalický 2:1 adukt s peroxidem vodíku[5] a s oxidem siřičitým.[6]
Tvorba iontových monomerů
DABCO lze použít k přípravě dvojnásobně nabitých styrenových monomerů. Tyto monomery umožňují tvorbu polyelektrolytů a ionomerů s dvěma cyklickými kvartérními amoniovými kationty na každé molekule.[7]
Zachytávání singletového kyslíku
DABCO a podobné aminy mohou zachytávat singletový kyslík, jsou tak účinnými antioxidanty[8] a lze je použít k prodloužení životnosti barviv. Díky tomu nachází DABCO využití v barvivových laserech a ve fluorescenčních mikroskopech.[9]
DABCO může též být použit při demethylacích kvartérních amoniových solí zahříváním v dimethylformamidu (DMF).[10]
Výroba
Dabco se vyrábí tepelnými reakcemi sloučenin typu H2NCH2CH2X (X = OH, NH2 nebo NHR) za katalýzy zeolity. Níže je uvedena rovnice přípravy z ethanolaminu:[11]
- 3 H2NCH2CH2OH → N(CH2CH2)3N + NH3 + 3 H2O
Odkazy
Literatura
- Cecchi, L.; DESARLO, F.; MACHETTI, F. 1,4-Diazabicyclo[2.2.2]octane (DABCO) as an Efficient Reagent for the Synthesis of Isoxazole Derivatives from Primary Nitro Compounds and Dipolarophiles: The Role of the Base. European Journal of Organic Chemistry. 2006, s. 4852–4860. DOI 10.1002/ejoc.200600475. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu 1,4-diazabicyklo(2.2.2)oktan na Wikimedia Commons
Obrázky, zvuky či videa k tématu 1,4-diazabicyklo(2.2.2)oktan na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku DABCO na anglické Wikipedii.
- ↑ a b c d e f g h i j k https://pubchem.ncbi.nlm.nih.gov/compound/9237
- ↑ Uppuluri V. Mallavadhani, Nicolas Fleury-Bregeot. „1,4-Diazabicyclo [2.2.2]octane“. In Encyclopedia of Reagents for Organic Synthesis, 2010, John Wiley & Sons, Ltd. DOI:10.1002/047084289X.rd010m.pub2
- ↑ Polyurethane additives guide [online]. Air Products & Chemicals. Dostupné v archivu pořízeném z originálu dne 2016-03-06.
- ↑ Baylis, A. B.; Hillman, M. E. D. German Patent 2155113, 1972
- ↑ P. Dembech, A. Ricci, G. Seconi, and M. Taddei „Bis(trimethylsilyl) Peroxide“ Organic Syntheses 1997, volume 74, pp. 84. DOI:10.15227/orgsyn.074.0084
- ↑ Ludovic Martial and Laurent Bischoff „Preparation of DABSO from Karl-Fischer Reagent“ Organic Syntheses 2013, volume 90, pp. 301. DOI:10.15227/orgsyn.090.0301
- ↑ K. Zhang; K. J. Drummey; N. G. Moon; W. D. Chiang; T. E. Long. Styrenic DABCO salt-containing monomers for the synthesis of novel charged polymers. Polymer Chemistry. 2016, s. 3370–3374. Dostupné online. DOI 10.1039/C6PY00426A.
- ↑ C. Ouannes; T. Wilson. Quenching of singlet oxygen by tertiary aliphatic amines. Effect of DABCO (1,4-diazabicyclo[2.2.2]octan). Journal of the American Chemical Society. 1968, s. 6527–6528. Dostupné online. DOI 10.1021/ja01025a059.
- ↑ K. Valnes; P. Brandtzaeg. Retardation of immunofluorescence fading during microscopy. Journal of Histochemistry and Cytochemistry. 1985, s. 755–761. Dostupné v archivu pořízeném dne 2015-05-13. DOI 10.1177/33.8.3926864. PMID 3926864. Archivováno 13. 5. 2015 na Wayback Machine.
- ↑ T. L. Ho. Dealkylation of Quaternary Ammonium Salts with 1,4-Diazabicyclo[2.2.2]octane. Synthesis. 1985, s. 755–761. Dostupné v archivu pořízeném dne 2015-05-13. DOI 10.1055/s-1972-21977. Archivováno 13. 5. 2015 na Wayback Machine.
- ↑ Karsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke „Amines, Aliphatic“ in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005. DOI:10.1002/14356007.a02_001
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
A metal-free Sonogashira coupling using DABCO as catalyst. Example gives a 77% yield, with 95% selectivity. Information from: Luque R, Macquarrie DJ. "Efficient solvent- and metal-free Sonogashira protocol catalysed by 1,4-diazabicyclo(2.2.2) octane (DABCO)", Organic and Biomolecular Chemistry, 2009, 7, 1627 – 1632. doi:10.1039/b821134p
Ball-and-stick model of the 1,4-diazabicyclo[2.2.2]octane (DABCO) molecule
Skeletal formula of DABCO, 1,4-diazabicyclo[2.2.2]octane



![Příklad reakce katalyzované 1,4-diazabicyklo[2.2.2]oktanem](http://upload.wikimedia.org/wikipedia/commons/thumb/c/ca/DABCO_Sonogashira.png/500px-DABCO_Sonogashira.png)







