Difosfiny

Difosfiny, neboli bisfosfany, jsou organické sloučeniny fosforu, obsahující dvě fosfinové skupiny propojené organickými řetězci. Používají se jako bidentátní fosfinové ligandy, často chelatující, v homogenních katalyzátorech.[1] Změnami funkčních skupin navázaných na fosfanové jednotky i propojujících skupin lze upravovat elektronové a sterické vlastnosti ligandů, které mohou vést k odlišným koordinačním geometriím a katalytickým vlastnostem.
Příprava

Z fosfidů

Řada běžně používaných difosfinů odpovídá obecnému vzorci Ar2P(CH2)nPAr2. Tyto sloučeniny se připravují reakcí X(CH2)nX (X = halogen) a MPPh2 (M = alkalický kov):[2]
- Cl(CH2)nCl + 2 NaPPh2 → Ph2P(CH2)nPPh2 + 2 NaCl
Difosfiny je možné připravit také z dilithiovaných sloučenin a chlorfosfinů:[3]
- XLi2 + 2 ClPAr2 → X(PAr2)2 + 2 LiCl (X = uhlovodíkový řetězec)
Tento postup je vhodný k zavádění dvou dialkylfosfinových skupin pomocí činidel jako je chlordiisopropylfosfin.
Nesymetrické difosfiny lze výhodně získat navázáním sekundárních fosfinů na vinylfosfiny, jako je například vinyldifenylfosfin:
- Ph2PH + 2 CH2=CHPAr2 → Ph2PCH2-CH2PAr2
Na přípravu nesymetrických difosfinů lze použít i (2-lithiofenyl)difenylfosfin, získatelný z (2-bromfenyl)difenylfosfinu:
- Ph2P(C6H4Br) + BuLi → Ph2P(C6H4Li) + BuBr
- Ph2P(C6H4Li) + R2PCli → Ph2P(C6H4PR2) + LiCl
Z bis(dichlorfosfinů)
Mnoho difosfinů se připravuje ze sloučenin typu X(PCl2)2, kde X = (CH2)n nebo C6H4 pomocí 1,2-bis(dichlorfosfino)ethanu nebo 1,2-bis(dichlorfosfino)benzenu.

Délka řetězce a koordinační vlastnosti
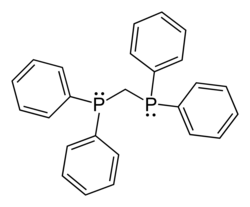
Difosfiny s krátkým řetězcem, jako je 1,1-bis(difenylfosfino)methan (dppm) vytvářejí interakce mezi atomy kovů. Pokud jsou fosfinové jednotky spojeny dvou- až čtyřuhlíkatým řetězcem, tak vzniklé ligandy vytvářejí chelátové kruhy s jedním atomem kovu. Patří sem také 1,2-bis(difenylfosfino)ethan (dppe), vytvářející s většinou kovů pětičlenné chelátové kruhy.
Některé difosfiny, například tBu2P(CH2)10PtBu2, vytváří makrocyklické komplexy obsahující až 72atomové kruhy.[6]
K tomu, aby byla fosfinová donorová skupina v koordinační sféře v poloze trans je třeba, aby se na donorová centra navázalo několik atomů; difosfiny s dlouhými řetězci jsou často „měkké“ a nejsou tak dobrými chelatačními činidly. Tento nedostatek lze překonat použitím dlouhých, ale pevných, difosfinů SPANphos.[7] Úhel skusu fosfinu ovlivňuje reaktivitu kovu.[8]
Jsou známy i nechelatující difosfiny, u kterých v důsledku sterických efektů atomy fosforu mohou reagovat pouze s protony.[9] Na chelatující je lze přeměnit úpravou délky organických můstků.[10]
Příklady ligandů
Níže jsou zobrazeny některé běžnější difosfiny:[11]
| Zkratka | Běžný název (z nějž je odvozena zkratka) | Struktura | Úhel skusu[12], pokud není uvedeno jinak |
|---|---|---|---|
| dppm | 1,1-bis(difenylfosfino)methan | 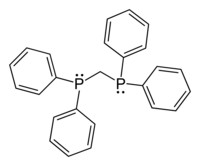 | 73 |
| dmpe | 1,2-bis(dimethylfosfino)ethan | 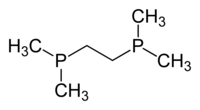 | |
| dippe | 1,2-bis(diisopropylfosfino)ethan | 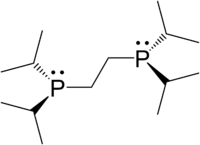 | |
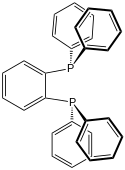
| dppbz | 1,2-bis(difenylfosfino)benzen |  | |
| dppe | 1,2-bis(difenylfosfino)ethan |  | 86 |
| DIPAMP | derivát fenylanisylmethylfosfinu |  | |
| dcpe | bis(dicyklohexylfosfino)ethan | 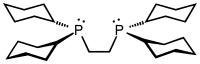 | |
| dppp | 1,3-bis(difenylfosfino)propan | 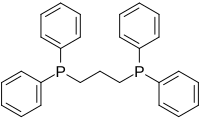 | 91 |
| dppb | 1,4-Bis(difenylfosfino)butan |  | 94 |
| DIOP | (S,S)-DIOP (O-isopropyliden-2,3-dihydroxy-1,4-bis(difenylfosfino)butan) |  | |
| Chiraphos | 2,3-bis(difenylfosfino)butan |  | |
| BINAP | 2,2'-bis(difenylfosfino)-1,1'-binaftyl |  | 93 |
| Xantphos | 4,5-bis(difenylfosfino)-9,9-dimethylxanthen |  | 108 |
| DPEphos | bis[(2-difenylfosfino)fenyl]ether | 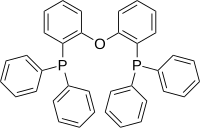 | 104 |
| SPANphos | 4,4,4',4',6,6'-hexamethyl-2,2'-spirobichroman-8,8'-diylbis(difenylfosfan) | 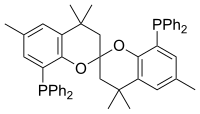 | |
| SEGPHOS | 4,4'-bi-1,3-benzodioxol-5,5'-diylbis(difenylfosfan) |  | |
| dppf | 1,1'-bis(difenylfosfino)ferrocen |  | 99 |
| Me-DuPhos | 1,2-bis(2,5-dimethylfosfolano)benzen |  | |
| Josiphos | (difenylfosfino)ferrocenyl-ethyldicyklohexylfosfin | ![Josiphos[3]](http://upload.wikimedia.org/wikipedia/commons/thumb/6/63/Josiphos.png/200px-Josiphos.png) | |
| P2N2 | 1,5-diaza-3,7-difosfacyklooktany | 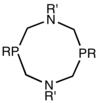 |
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Diphosphines na anglické Wikipedii.
- ↑ Hartwig, J. F. Organotransition Metal Chemistry, from Bonding to Catalysis; University Science Books: New York, 2010 ISBN 189138953X
- ↑ Wilkinson, G.; Gillard, R.; McCleverty, J. Comprehensive Coordination Chemistry: The synthesis, reactions, properties & applications of coordination compounds, vol. 2; Pergamon Press: Oxford, UK, 1987; 993 ISBN 0-08-035945-0
- ↑ Gareth J. Rowlands Planar Chiral Phosphines Derived from [2.2]Paracyclophane Israel Journal of Chemistry 2012, volume 52, issue 1-2, pages 60–75DOI:10.1002/ijch.201100098
- ↑ Roger J. Burt; Joseph Chatt; Wasif Hussain; G.Jeffery Leigh. A convenient synthesis of 1,2-bis(dichlorophosphino)ethane, 1,2-bis(dimethylphosphino)ethane and 1,2-bis(diethylphosphino)ethane. Journal of Organometallic Chemistry. 1979, s. 203–206. DOI 10.1016/S0022-328X(00)94383-3.
- ↑ Kenneth G. Moloy; Jeffrey L. Petersen. N-Pyrrolyl Phosphines: An Unexploited Class of Phosphine Ligands with Exceptional .pi.-Acceptor Character. Journal of the American Chemical Society. 1995, s. 7696–7710. DOI 10.1021/ja00134a014.
- ↑ Cotton, F. A.; Wilkinson, G. Advanced Inorganic Chemistry: A Comprehensive Text, 4th ed.; Wiley-Interscience Publications: New York, NY, 1980; 246 ISBN 0-471-02775-8
- ↑ Z. Freixa, M. S. Beentjes, G. D. Batema, C. B. Dieleman, G. P. F. v. Strijdonck, J. N. H. Reek, P. C. J. Kamer, J. Fraanje, K. Goubitz, P. W. N. M. Van Leeuwen. SPANphos: A C2-Symmetric trans-Coordinating Diphosphane Ligand. Angewandte Chemie. 2003, s. 1322–1325. DOI 10.1002/anie.200390330. PMID 12645065.
- ↑ Birkholz, M.-N., Freixa, Z., van Leeuwen, P. W. N. M., „Bite angle effects of diphosphines in C-C and C-X bond forming cross coupling reactions“, Chemical Society Reviews 2009, vol. 38, 1099
- ↑ Zong, J., J. T. Mague, C. M. Kraml, and R. A. Pascal, Jr., A Congested in,in-Diphosphine, Organic Letters 2013, 15, 2179-2181
- ↑ Zong, J., J. T. Mague, and R. A. Pascal, „Encapsulation of non-hydrogen atoms by in, in-bis (triarylelement)-containing cyclophanes“ Tetrahedron, 2017, 73, 455-460
- ↑ http://old.iupac.org/reports/provisional/abstract04/RB-prs310804/TableVII-3.04.pdf
- ↑ van Leeuwen Chemical Society Reviews 2009
Související články
- Dialkylbiarylfosfinové ligandy
Média použitá na této stránce
Skeletal formula of 1,2-bis(dimethylphosphino)ethane, dmpe, Me2PCH2CH2PMe2.
Structure drawn in ChemDraw Ultra 11.0.Autor: Smokefoot, Licence: CC BY-SA 4.0
chemical structure of chlorodiisopropylphosphine
structure of 1,2-bis(diphenylphosphino)benzene
Autor: Amir.ahrls, Licence: CC0
1,2-Bis(diisopropylphosphino)ethane 2D molecular structure
Autor: Smokefoot, Licence: CC BY-SA 4.0
chemical structure of (2-bromophenyl)diphenylphosphine
Autor: Organometallics, Licence: CC BY-SA 3.0
H-U. Blaser, W. Brieden, B. Pugin, F. Spindler, M. Studer and A. Togni, Top. Catal., 2002, 19, 3.
Skeletal formula of the 1,1-bis(diphenylphosphino)methane or dppm molecule, C25H22P2 or H2C(PPh2)2.
X-ray structure from Acta Cryst. (2007). E63, o2559.
Model constructed in CrystalMaker 8.1.
Image generated in Accelrys DS Visualizer.structure of 1,2-C2H4(PCl2)2 (1,2-bis(dichlorophosphino)ethane)
Autor: Smokefoot, Licence: CC BY-SA 3.0
improved image of the ligand dppf as a chelating rotamer
Struktur von DIPAMP
BINAP_Enantiomers
Chemical structure of bis(2-diphenylphosphinophenyl)ether (DPEphos)
Autor: Pelirojopajaro, Licence: CC BY-SA 4.0
The diphoshine ligand diphenylphosphinobutane AKA dppb
Structure of (S,S)-DIOP (O-isopropylidene-2,3-dihydroxy-1,4-bis(diphenylphosphino)butane)
Chemical structure of dppp (1,3-bis(diphenylphosphino)propane)
Skeletal formula of a generic diphosphine ligand.
Image generated in ChemBioDraw Ultra 12.0.