Elektronová ionizace

Elektronová ionizace (zkráceně EI) je způsob ionizace, který spočívá v srážkách elektronů s vysokými energiemi s atomy nebo molekulami vedoucími k tvorbě iontů.[1] Jde o jeden z prvních způsobů ionizace používaný v hmotnostní spektrometrii,[2] stále však patří k často využívaným postupům. Patří mezi tvrdé ionizační metody (vytvářející velký počet fragmentů), protože se k ionizaci používají elektrony o vysokých energiích a tvoří se velký počet fragmentů, což umožňuje určení struktury neznámých látek. Nejčastěji se používá u organických sloučenin s relativní molekulovou hmotností do 600. Kombinacemi s různými separačními metodami je možné elektronovou ionizaci využít na analýzu některých těkavých a teplotně nestabilních sloučenin.[3]
Historie

Elektronovou ionizaci poprvé popsal roku 1918 kanadskoamerický fyzik Arthur J. Dempster.[4] Jako zdroj iontů se při této metodě používá proud elektronů pohybující se k pevnému povrchu. Anoda měla válcovitý tvar a byla vyrobena z kovu, který měl být zkoumán; byla zahřívána a poté ostřelována elektrony. Byly identifikovány dva izotopy lithia a tři izotopy hořčíku.[5] Od té doby bylo uskutečněno několik vylepšení. Používání soustředěného jednoelektronového paprsku k ionizaci atomů a molekul v plynném skupenství zavedl Walker Bleakney v roce 1929.[6][7]
Podstata účinku

Při elektronové ionizaci dochází k vytržení elektronu z molekuly analytu (M) při srážce s elektronem, čímž dojde ke vzniku kladně nabitého iontu s lichým počtem elektronů. Průběh elektronové ionizace plynné látky lze popsat takto: [8]
kde M je molekula analytu, která je ionizována, e− je elektron anM+• je vzniklý molekulový ion.
V elektronově ionizačních zdrojích iontů se elektrony vytvářejí zahříváním tenkého drátu, kterým prochází elektrický proud. Kinetická energie uvolněných elektronů by měla být vyšší než ionizační energie zkoumané molekuly. Mezi drátem a zdrojem iontů získávají elektrony energii okolo 70 eV. Vzorek se do zdroje iontů dostane kolmo vůči elektronovému paprsku. Vysokoenergetické elektrony v prostředí s nízkým tlakem (10−3 až 10−4 Pa) vyvolají fluktuace v elektrickém poli okolo molekul a způsobí jejich ionizaci a fragmentaci.[9] Fragmentaci při elektronové ionizaci je možné popsat pomocí Bornových-Oppenheimerových potenciálových křivek, jak je znázorněno výše; červená šipka označuje energii potřebnou k nedisociativní ionizaci, zatímco modrá označuje disociativní procesy, kterými vznikají sekundární ionty. Vytvořené radikálové kationty putují do hmotnostního analyzátoru. Fragmentaci často lze předvídat, což umožňuje získat údaje o struktuře analytu.
Účinnost
Účinnost elektronové ionizace lze zlepšit úpravou vláknového, emisního a ionizačního proudu; vláknový proud je proud dodávaný do vlákna za účelem jeho zahřátí, emisní proud je proud naměřitelný mezi vláknem a místem vstupu elektronů a ionizační proud odpovídá rychlosti průchodu elektronů do iontové pasti a počtu elektronů využitelných k ionizaci.
Úroveň ionizace lze uvádět jako iontový proud vzorku (I+). Lze jej upravit změnou účinnosti extrakce iontů (β), účinného průřezu ionizace (Qi), účinné délky ionizační dráhy (L), koncentrace molekul ve vzorku ([N]) a ionizačního proudu (Ie). Celý proces popisuje tato rovnice:
Účinnost extrakce iontů (β) může být zvýšena zvýšením napětí. Účinný průřez ionizace závisí na chemických vlastnostech vzorku a na energii elektronů, obvykle se udává pro energii 70 eV. Při nízkých energiích (kolem 20 eV) interakce mezi elektrony a analytem nejsou dostatečné silné na to, aby vyvolávaly ionizaci. Při 70 eV je de Broglieova vlnová délka elektronů podobná délce běžných vazeb v organických molekulách (kolem 0,14 nm) a energie předaná molekulám analytu maximální, takže dochází k největší možné ionizaci a fragmentaci, kdy se ionizuje přibližně 1 z 1000 molekul ve vzorku. U vyšších energií je de Broglieova vlnová délka elektronů kratší než délka vazeb v obvyklých analytech a molekuly jsou tak pro elektrony „průhledné“, což vede ke snížení účinnosti ionizace. Účinnou délku ionizační dráhy (L) je možné zvýšit použitím slabého magnetického pole, nejčastějším způsobem zvyšování proudu ve vzorku je ovšem navýšení ionizačního proudu (Ie).[3]
Součásti přístroje
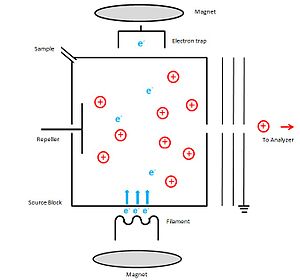
Na obrázku výše je zobrazeno schéma přístroje pro elektronovou ionizaci. Zdrojem iontů je kovová katoda, nejčastěji ve formě vlákna tvořeného wolframem nebo rheniem, která se zahřívá. Mezi katodou a zdrojem iontů je napětí 70 V, které dodává elektronům kinetickou energii 70 eV. Potenciál anody (elektronové pasti) je mírně kladný a umístěn mimo ionizační komoru naproti katodě. Tato elektronová past vychytává nevyužité elektrony. Vzorek je aplikován do příslušné díry. Ke zvýšení míry ionizace se rovnoběžně se směrem pohybu elektronů vkládá slabé magnetické pole; elektrony se tak pohybují po úzké šroubovicové dráze, díky tomuto tvaru je jejich dráha delší. Vznikající kationty se urychlují odpuzovací elektrodou. S využitím potenciálu vzhledem ke zdroji iontů a udržování základního potenciálu u místa odchodu elektronů ionty vstupují do hmotnostního analyzátoru s konkrétní hodnotou kinetické energie. Kondenzaci vzorku se zabrání zahříváním na přibližně 300 °C.[3]
Využití
Od začátku 20. století je elektronová ionizace jedním z nejčastěji využívaných způsobů ionizace, protože má mnoho využití, které lze rozdělit podle způsobu, kterým se vzorek dostává do ionizační komory. U plynných a velmi těkavých vzorků se používá vakuová komora, u pevných látek a méně těkavých kapalin dochází k přímému aplikování vzorku a v případě složitějších směsí se kombinuje s kapalinovou nebo plynovou chromatografií.
Vakuová komora
V tomto případě se vzorek nejprve dostane do vakuové komory, kde je zahříván, a následně přechází malým otvorem do ionizační komory. Tento způsob se používá u značně těkavých vzorků, u nichž nelze použít jiné postupy.[10]
Přímý vstup vzorku
Při přímém vstupu vzorku se používá sonda tvořená dlouhým kusem kovu, který obsahuje kapiláru se vzorkem. Vzorek je vpraven do ionizační komory pomocí skleněné kapiláry. Následně se sonda rychle zahřívá na teplotu potřebnou k odpaření vzorku. Tímto způsobem se vzorek může dostat velice blízko k místu, kde probíhá ionizace.[3]
Analýza archeologických materiálů
Hmotnostní spektrometrie s elektronovou ionizací s přímým vstupem vzorku má využití v archeologii při zkoumání vzorků obsahujících materiály jako jsou dehty, pryskyřice a vosky. Nejčastější metodou analýzy je zde plynová chromatografie s hmotnostní spektroskopií. Jelikož tyto vzorky často pocházejí z pravěku, tak jsou často použitelná jen jejich malá množství. Pomocí EI–MS s přímým vstupem vzorku je možné analyzovat zbytky organických látek a směsí jako jsou pryskyřice, dehty, včelí vosk a rostlinné oleje z doby bronzové a železné. Výhodou tohoto postupu je malé množství vzorku potřebné k analýze a minimální potřeba přípravy vzorku.[11]
Srovnání EI-MS s přímým vstupem vzorku a plynové chromatografie bylo provedeno při zkoumání organických látek v nátěrech na amforách z doby starověkého Říma. Bylo zjištěno, že analýza s přímým vstupem vzorku je rychlá a přímá metoda použitelná k analýze organických archeologických materiálů, která umožňuje určit hlavní složky vzorku; pomocí ní lze zjistit míru oxidace přítomných látek. Nevýhodou je, že méně zastoupené složky nemusí být určeny.[12]
Analýza látek v životním prostředí
Plynová chromatografie s elektronově ionizační hmotnostní spektroskopií (GC-EI-MS) může být použita k detekci pozůstatků pesticidů v potravinách; například v zelenině bylo takto nalezeno 81 různých pesticidů. Ke zkoumání těchto pesticidů byla využita extrakce dichlormethanem a následně plynová chromatografie s tandemovou hmotnostní spektroskopií (GC-MS-MS). Jako nejvhodnější způsoby ionizace byly určeny elektronová a chemická ionizace. Jedná se o metodu, která je rychlá, jednoduchá a z jednoho nástřiku vzorku lze určit velké množství různých pesticidů, čímž se zkracuje doba analýzy.[13]
Analýza biokapalin
Plynovou chromatografii s elektronově ionizační hmotnostní spektroskopií je možné analyzovat biokapaliny; příkladem je identifikace syntetických pyrethroidových insekticidů v krvi s využitím selektivního sledování iontů pomocí plynové chromatografie s hmotnostní spektrometrií s jediným nástřikem vzorku. Jednotlivé pyrethroidy byly odděleny pomocí GC-MS s využitím elektronové ionizace a jejich množství byla určena selektivním sledováním iontů. Detekování zbytků jednotlivých insekticidů je obtížné, protože jejich koncentrace jsou velmi nízké, jelikož jsou brzy po vstupu do organismu vyloučeny. Touto metodou lze však zachytit různé pyrethroidy již při koncentracích kolem 0,05 až 2 ng/ml. Jejich zachycení v krvi má velký význam, protože i takováto množství mohou ovlivňovat lidské zdraví, obzvláště u dětí. GC-EI-MS je možné upravit tak, aby byly vyloučeny rušivé vlivy matrice. Selektivní sledování iontů umožňuje snížit mez detekce až na 0,05 ng/ml.[14] GC-EI-MS je také možné použít například k měření velmi nízkých koncentrací D-fenylalaninu při výzkumu lidské proteosyntézy. Lze přitom měřit koncentrace volného i vázaného D-fenylalaninu stejným hmotnostním spektrometrem a k analýze stačí velmi malé množství bílkoviny (okolo 1 mg).[15]
Forenzní vědy
GC-EI-MS má také využití ve forenzních vědách; příkladem může být analýza pěti lokálních anestetik v krvi pomocí plynové chromatografie pro měření rozpuštěných plynů s mikroextrakcí pevné fáze (HS-SPME) a plynové chromatografie s hmotnostní spektrometrií s elektronovou ionizací a selektivního sledování iontů (GC–MS–EI-SIM). Lokální anestezie se provádí velmi často, ovšem použité látky ojediněle mívají vedlejší účinky. V některých případech je potřeba rychlá a jednoduchá metoda analýzy lokálních anestetik. GC-EI-MS byla použita při době analýzy okolo 65 minut a hmotnostech vzorků přibližně 0,2 g.[16]
Kapalinová chromatografie s EI-MS
Byly popsány dva způsoby využití uplatnění kapilární kapalinové chromatografie a hmotnostní spektrometrie s elektronovou ionizací (LC-EI-MS), používají se při nich buď kapilární EI rozhraní mezi LC a MS, nebo přímá EI rozhraní. U kapilární EI je rozprašovač optimalizován tak, aby bylo dosaženo co možná nejlepší linearity a citlivosti. Přímá EI rozhraní jsou miniaturizovaná rozhraní pro nano- a mikro-vysokoúčinnou kapalinovou chromatografii (HPLC), která obsahují vhodně pozměněné zdroje iontů. Vyšší citlivost a lepší linearita a reprodukovatelnost může být dosažena díky tomu, že eluce vzorku z chromatografu do iontového zdroje má téměř 100procentní účinnost. Pomocí těchto dvou rozhraní může být elektronová ionizace využita k analýze malých a středně velkých molekul s rozdílnými mírami polarity. Jejich nejběžnějšími způsoby využití v LC-MS je při zkoumání životního prostředí, například jde o gradientovou separaci pesticidů, jako jsou karbaryl, propanil a chlorprofam, chromatografií s obrácenými fázemi, a farmaceutická využití, jako oddělování protizánětlivých léčiv difenyldraminu, amitryptylinu, naproxenu a ibuprofenu.[17]
Jiným způsobem klasifikace metod založených na elektronové ionizaci je založeno na způsobu oddělování složek směsi. Z takto určených druhů jsou nejčastěji používány TOF a ortogonální TOF hmotnostní spektrometrie (OA-TOF MS), Cyklotronová iontová rezonance s Fourierovou transformací (FT-ICR MS) a kvadrupólová hmotnostní spektrometrie.
TOF hmotnostní spektrometrie
TOF hmotnostní spektrometrie s elektronovou ionizací (EI-TOF MS) je metoda využívající elektronovou ionizaci v hmotnostní spektrometrii doby letu (TOF MS), jedná se o vhodnou metodu pro analytickou i fyzikální chemii. EI-TOF MS se používá ke zjišťování ionizačních potenciálů molekul a radikálů a také vazebných energií iontů i neutrálních molekul. Lze ji použít i při výzkumu chemických a fyzikálních vlastností aniontů (záporně nabitých iontů). Při této metodě tvorba oblasti volné ionizace umožňuje dosažení velké přesnosti a rozlišení, co se energie elektronů týče.
Elektronová ionizace s ortogonálním-urychlováním spojená TOF MS (EI oa-TOFMS) byla poprvé popsána v roce 1989. Pomocí ní bylo dosaženo lepších rozlišení. Jedna z hlavních výhod oa-TOFMS s elektronovou ionizací se projevuje při spojení s plynovými chromatografy , kde je díky ní možné velmi rychle oddělovat organické sloučeniny.[18]
Cyklotronová iontová rezonance s Fourierovou transformací
Cyklotronovou iontová rezonanci s Fourierovou transformací byla použita k analýze tří frakcí z motorové nafty, s teplotami varu 295-319 °C, 319-456 °C a 456-543 °C. Využívá se zde,EI s energií elektronů 10 eV, čímž dochází k „měkké“ ionizaci aromatických sloučenin. Odchylky ve složení na molekulární úrovni lze určit pomocí stanovení prvkového složení. U této metody je dosahováno velmi vysokého rozlišení, dobré reprodukovatelnosti a přesnosti (<0,4 ppm) i při malém objemu vzorku. Hlavními složkami všech tří uvedených frakcí jsou aromatické uhlovodíky, navíc lze odhalit přítomnost mnoha sloučenin síry, dusíku a kyslíku. Analýzou získaných dat lze zjistit údaje o struktuře těchto látek, jako jsou aromatické kruhy a dvojné vazby, počet uhlíkových atomů a průměrná molární hmotnost.[19]
Hmotnostní spektrometrie s iontovou pastí
Hmotnostní spektrometrii s +iontovou pastí je možné použít na identifikaci a stanovení pozůstatků nonylfenolpolyethoxylátu (NPEO) a produktů jeho rozkladu, jako jsou například nonylfenolpolyethoxykarboxyláty a karboxyalkylfenolethoxykarboxyláty, v pitné i odpadní vodě. Plynová chromatografie s hmotnostní spektrometrií s iontovou pastí je vhodnou metodou analýzy, kombinovatelnou s několika různými způsoby ionizace, jako je i EI, při určování složení vzorků pocházejících ze životního prostředí.[20]
Výhody a nevýhody
Použití elektronové ionizace v hmotnostní spektrometrii má několik výhod i nevýhod.
| Výhody | Nevýhody |
|---|---|
| Jednoduché provedení | Molekuly musejí být těkavé |
| Velká citlivost | molekuly musí být odolné vůči vysokým teplotám |
| Fragmentace usnadňuje určení struktury molekul | Vysoká míra fragmentace ztěžuje vyhodnocování údajů |
| Možnost vyhledávat spektra v databázích | Metodu lze použít pouze pro sloučeniny s molekulovými hmotnostmi pod 1000 Da |
Odkazy
Související články
- Chemická ionizace
- Tepelná ionizace
Reference
V tomto článku byl použit překlad textu z článku Electron ionization na anglické Wikipedii.
- ↑ The IUPAC Compendium of Chemical Terminology: The Gold Book. Příprava vydání Victor Gold. 4. vyd. Research Triangle Park, NC: International Union of Pure and Applied Chemistry (IUPAC) Dostupné online. DOI 10.1351/goldbook.e01999. (anglicky) DOI: 10.1351/goldbook.
- ↑ Jennifer Griffiths. A Brief History of Mass Spectrometry. Analytical Chemistry. 2008, s. 5678–5683. ISSN 0003-2700. DOI 10.1021/ac8013065.
- ↑ a b c d Chhabil Dass. Fundamentals of Contemporary Mass Spectrometry - Dass - Wiley Online Library. [s.l.]: [s.n.], 2007. ISBN 9780470118498. DOI 10.1002/0470118490.
- ↑ A. J. Dempster. A new Method of Positive Ray Analysis. Physical Review. 1918-04-01, s. 316–325. Dostupné online. DOI 10.1103/PhysRev.11.316. Bibcode 1918PhRv...11..316D.
- ↑ A. J. Dempster. Positive Ray Analysis of Lithium and Magnesium. Physical Review. 1921-01-01, s. 415–422. DOI 10.1103/PhysRev.18.415. Bibcode 1921PhRv...18..415D.
- ↑ Walker Bleakney. A New Method of Positive Ray Analysis and Its Application to the Measurement of Ionization Potentials in Mercury Vapor. Physical Review. 1929, s. 157–160. ISSN 0031-899X. DOI 10.1103/PhysRev.34.157. Bibcode 1929PhRv...34..157B.
- ↑ Mark Gordon Inghram; Richard J. Hayden. Mass Spectroscopy. [s.l.]: National Academies, 1954. S. 32–34.
- ↑ R. Davis, M. Frearson, (1987). Mass Spectrometry – Analytical Chemistry by Open Learning, John Wiley & Sons, London.
- ↑ K. Robinson et al. Undergraduate Instrumental Analysis, 6th ed. Marcel Drekker, New York, 2005
- ↑ Chhabil Dass. Fundamentals of Contemporary Mass Spectrometry. Příprava vydání Dominic Desiderio, Nico Nibbering. Hoboken: John Wiley & Sons, Inc., 2007. Dostupné online. S. 19.
- ↑ Martine Regert; Christian Rolando. Identification of Archaeological Adhesives Using Direct Inlet Electron Ionization Mass Spectrometry. Analytical Chemistry. 2002-02-02, s. 965–975. DOI 10.1021/ac0155862. PMID 11924999.
- ↑ Maria Colombini; Francesca Modugno; Erika Ribechini. Direct exposure electron ionization mass spectrometry and gas chromatography/mass spectrometry techniques to study organic coatings on archaeological amphorae. Journal of Mass Spectrometry. 2005-05-01, s. 675–687. ISSN 1096-9888. DOI 10.1002/jms.841. PMID 15739159. Bibcode 2005JMSp...40..675C.
- ↑ F. J. Arrebola; J. L. Martı́nez Vidal; M. Mateu-Sánchez; F. J. Álvarez-Castellón. Determination of 81 multiclass pesticides in fresh foodstuffs by a single injection analysis using gas chromatography–chemical ionization and electron ionization tandem mass spectrometry. Analytica Chimica Acta. 2003-05-19, s. 167–180. DOI 10.1016/S0003-2670(03)00332-5.
- ↑ Atmakuru Ramesh; Perumal Elumalai Ravi. Electron ionization gas chromatography–mass spectrometric determination of residues of thirteen pyrethroid insecticides in whole blood. Journal of Chromatography B. 2004-04-05, s. 371–376. DOI 10.1016/j.jchromb.2003.12.016. PMID 15018801.
- ↑ A. G. Calder; S. E. Anderson; I. Grant; M. A. McNurlan; P. J. Garlick. The determination of low d5-phenylalanine enrichment (0.002–0.09 atom percent excess), after conversion to phenylethylamine, in relation to protein turnover studies by gass chromatography/electron ionization mass spectrometry. Rapid Communications in Mass Spectrometry. 1992-07-01, s. 421–424. ISSN 1097-0231. DOI 10.1002/rcm.1290060704. PMID 1638043. Bibcode 1992RCMS....6..421C.
- ↑ Tomohiko Watanabe; Akira Namera; Mikio Yashiki; Yasumasa Iwasaki; Tohru Kojima. Simple analysis of local anaesthetics in human blood using headspace solid-phase microextraction and gas chromatography–mass spectrometry–electron impact ionization selected ion monitoring. Journal of Chromatography B. 1998-05-29, s. 225–232. DOI 10.1016/S0378-4347(98)00081-4. PMID 9657219.
- ↑ Achille Cappiello; Giorgio Famiglini; Filippo Mangani; Pierangela Palma. New trends in the application of electron ionization to liquid chromatography—mass spectrometry interfacing. Mass Spectrometry Reviews. 2001-01-01, s. 88–104. ISSN 1098-2787. DOI 10.1002/mas.1004. PMID 11455563. Bibcode 2001MSRv...20...88C.
- ↑ M. Guilhaus; D. Selby; V. Mlynski. Orthogonal acceleration time-of-flight mass spectrometry. Mass Spectrometry Reviews. 2000-01-01, s. 65–107. ISSN 1098-2787. DOI 10.1002/(SICI)1098-2787(2000)19:2<65::AID-MAS1>3.0.CO;2-E. PMID 10795088. Bibcode 2000MSRv...19...65G.
- ↑ Jinmei Fu; Sunghwan Kim; Ryan P. Rodgers; Christopher L. Hendrickson; Alan G. Marshall; Kuangnan Qian. Nonpolar Compositional Analysis of Vacuum Gas Oil Distillation Fractions by Electron Ionization Fourier Transform Ion Cyclotron Resonance Mass Spectrometry. Energy & Fuels. 2006-02-08, s. 661–667. DOI 10.1021/ef0503515.
- ↑ Wang-Hsien Ding; Shin-Haw Tzing. Analysis of nonylphenol polyethoxylates and their degradation products in river water and sewage effluent by gas chromatography–ion trap (tandem) mass spectrometry with electron impact and chemical ionization. Journal of Chromatography A. 1998-10-16, s. 79–90. DOI 10.1016/S0021-9673(98)00593-7. PMID 9818430.
Média použitá na této stránce
Portrait of Arthur Jeffrey Dempster
Autor: Evan Mason, Licence: CC BY-SA 4.0
Diagram of Electron Ionization, prepared with reference to Wikipedia article and http://schwinger.caltech.edu/~carl/ionization.html
Autor: Thilini ukwaththage, Licence: CC BY-SA 4.0
Schematic Diagram of Electron Ionization Instrumentation
Autor: Thilini ukwaththage, Licence: CC BY-SA 4.0
Electron Ionization of Methanol - Born Oppenheimer Potential Curves



