Elektronový obal

Elektronový obal je systém elektronů vázaných k jádru atomu, které obklopuje a zaujímá většinu prostoru atomu. Poloměr elektronového obalu (a tedy celého atomu) se pohybuje kolem 10−10 m a jeho hmotnost tvoří okolo 0,01 % celkové hmotnosti atomu. Prostor, ve kterém se nachází elektron s určitou mírou pravděpodobnosti (většinou 95%), se nazývá orbital.
Elektronový obal je tvořen pouze elektrony a proto má záporný elektrický náboj, který je v atomu neutralizovaný kladným nábojem jádra atomu. Proto je atom jako celek elektricky neutrální. Neutrální atomy obsahují v elektronovém obalu stejný počet elektronů, jako je počet protonů v jádře. U kladně nabitých iontů je počet elektronů v elektronovém obalu menší, u záporně nabitých iontů je počet elektronů v obalu větší.
Vlastnosti elektronů v obalu lze charakterizovat čtyřmi kvantovými čísly: hlavní, vedlejší, magnetické a spinové číslo. Energie elektronu je závislá na hlavním kvantovém čísle n, velikost momentu hybnosti elektronu závisí na vedlejším kvantovém čísle l, směr momentu hybnosti je určen magnetickým kvantovým číslem m, spin elektronu určuje směr jeho otáčivost kolem své osy a může nabývat pouze dvou hodnot +1/2 nebo -1/2.
Vlastnosti elektronů v atomu
Elektrony jsou, společně s protony a neutrony tvořícími atomová jádra, základními stavebními částicemi hmoty. V každém atomu se vyskytuje stejný počet elektronů, jako je počet protonů v jádře. Dojde-li k odtržení nebo přidání elektronu, stává se z atomu iont.
Chování elektronů mimo jiné popisuje teorie dualismu. Podle ní lze elektrony považovat za částici a vlnění současně. Některé jeho vlastnosti jsou vysvětlitelné, pouze pokud ho považujeme za částici, jiné jeho vlastnosti jsou vysvětlitelné, pouze pokud ho považujeme za vlnění. Stejně jako u ostatních elementárních částic v atomu popisuje chování elektronů kvantová teorie. Podle Schrödingerovy rovnice kvantové mechaniky (tzv. vlnové mechaniky) se elektrony vyskytují v různých orbitalech daných jejich
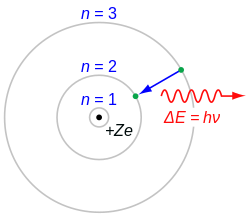
elektronovou konfigurací. Jednotlivé orbitaly neurčují přesně polohu elektronu, ale pouze největší pravděpodobnost jeho výskytu a pohybu v elektronovém obalu. Přechody elektronů mezi jednotlivými energetickými hladinami v elektronovém obalu jsou doprovázeny emisí nebo absorpcí fotonů elektromagnetického záření.
K vysvětlení základních spektrálních charakteristik vodíku postačuje zjednodušený Bohrův model atomu. K vysvětlení vlastností spekter atomů se složitějším obalem a změny spekter v magnetickém poli je již potřeba Schrödingerova kvantově-mechanického popisu a započtení vzájemné kvantové interakce spinů elektronů. Jemná a hyperjemná struktura spektra již vyžadují relativistický Diracův popis a započtení kvantové interakce se spinem atomového jádra.
Vlastnosti elektronů v elektronovém obalu


Elektronu se kolem jádra nepohybuje po přesně daných drahách, jeho umístění v atomovém obalu tak lze udat jen s určitou mírou pravděpodobností. Prostor, ve kterém se nachází elektron s určitou mírou pravděpodobnosti (většinou 95 %), se nazývá orbital. Pro popis orbitalu a pohybu konkrétního elektronu v atomovém obalu se využívají čtyři kvantová čísla - hlavní (n), vedlejší (l), magnetické (m) a spinové (s).
Hlavní kvantové číslo (n)
Hlavní kvantové číslo (n) udává pořadové číslo slupky (vrstvy), na které se daný elektron v atomovém obalu nachází a je určen jeho energií. Hlavní kvantové číslo nabývá hodnot 1-7 (také písmena K-Q). Nejblíže jádru je slupka 1 (K), nejvzdálenější je slupka 7 (Q).
Ve slupce nejblíž jádru, má elektron nejnižší energii. Se zvyšující se hodnotou hlavního kvantového čísla se zvyšuje energie daného elektronu, neboť mezi ním a kladně nabitým jádrem jsou slabší přitažlivé síly.
| n | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
|---|---|---|---|---|---|---|---|
| slupka | K | L | M | N | O | P | Q |
Vedlejší kvantové číslo (l)

Vedlejší kvantové číslo (l) udává tvar orbitalu (podslupky, oblasti), ve kterém se konkrétní elektron nachází. Orbital s hodnotou 0 se nazývá orbital s, s hodnotou 1 orbital p, s hodnotou 2 orbital d, s hodnotou 3 orbital f. V závislosti na tvaru daného orbitalu má elektron různou energií. Toto číslo nabývá hodnot od 0 do n-1, kde n je hlavní kvantové číslo. Pro konkrétní hodnoty vedlejšího kvantového čísla je jednoznačně určen typ daného orbitalu.
Magnetické kvantové číslo (m)
Magnetické kvantové číslo (m) určuje orientaci daného orbitalu v prostoru. Toto číslo je závislé na hodnotě vedlejšího kvantového čísla l, neboť samo nabývá hodnot od –l po +l. Magnetické kvantové číslo se tak nazývá proto, že po vložení atomu do magnetického pole je možné změnit prostorovou orientaci daného orbitalu.
| Podslupka | s | p | d | f |
|---|---|---|---|---|
| Hodnota vedlejšího čísla | 0 | 1 | 2 | 3 |
| Hodnota magnetického čísla | 0 | -1,0,1 | -2,-1,0,1,2 | -3,-2,-1,0,1,2,3 |
Spinové kvantové číslo (s)
Spinové kvantové číslo (s) udává vnitřní moment hybnosti konkrétního elektronu. Má pouze dvě hodnoty –1/2 nebo +1/2. Zjednodušeně udává směr rotace daného elektronu.
Počty elektronů ve slupkách
| Název slupky | Název podslupky | Maximální počet elektronů v podslupce | Maximální počet elektronů ve slupce |
|---|---|---|---|
| K | 1s | 2 | 2 |
| L | 2s | 2 | 2 + 6 = 8 |
| 2p | 6 | ||
| M | 3s | 2 | 2 + 6 + 10 = 18 |
| 3p | 6 | ||
| 3d | 10 | ||
| N | 4s | 2 | 2 + 6 + 10 + 14 = 32 |
| 4p | 6 | ||
| 4d | 10 | ||
| 4f | 14 | ||
| O | 5s | 2 | 2 + 6 + 10 + 14 + 18 = 50 |
| 5p | 6 | ||
| 5d | 10 | ||
| 5f | 14 | ||
| 5 g | 18 |
Pravidla výstavby elektronového obalu

Obsazování orbitalů jednotlivými elektrony není zcela náhodné a řídí se třemi základními zákonitostmi: Pauliho principem výlučnosti, Hundovým pravidlem a Výstavbovým principem.
Pauliho princip výlučnosti
Orbitaly se stejnou hodnotou hlavního (n) a vedlejšího kvantového čísla (l), které se liší v hodnotě magnetického kvantového čísla (m), mají stejnou hodnotu energie a nazývají se energeticky degenerované. Pauliho princip výlučnosti nebo Pauliho vylučovací princip říká, že v každém degenerovaném orbitalu se mohou nacházet nejvýše 2 elektrony, které se však musí lišit ve svém spinovém kvantovém čísle. Elektrony se graficky znázorňují jako šipky, které se vpisují do rámečků (orbitalů), přičemž odlišná orientace těchto šipek značí rozdílné spinové kvantové číslo. Podle Pauliho principu výlučnosti tak v každém atomu nemohou existovat dva elektrony, které by se současně shodovaly v hodnotách hlavního, vedlejšího, magnetického a spinového kvantového čísla.
Hundovo pravidlo
Hundovo pravidlo říká, že konkrétní orbital se zaplní dvěma elektrony, až ve chvíli, kdy každý degenerovaný orbital obsahuje alespoň 1 elektron.
Výstavbový princip

Výstavbový princip (též pravidlo n+l) říká, že elektrony nejprve obsadí orbitaly s nejnižší hodnotou energie, která je jednoznačně určena jeho hlavním a vedlejším kvantovým číslem. Proto se nejprve zaplňují elektrony právě ty orbitaly, které mají nižší součet hodnot hlavního a vedlejšího kvantového čísla. Dříve se zaplní tedy například orbital 4s (4+0=4), než orbital 3d (3+2=5). Jestliže jsou tyto součty u dvou různých orbitalů shodné, zaplní se elektrony nejprve orbital, který má nižší hodnotu hlavního kvantového čísla. Orbital 2p (2+1=3) se zaplní elektrony dříve, než orbital 3s (3+0=3). Orbitaly se tedy zaplňují v pořadí: 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s ...
Z uvedených poznatků je možné zapsat elektronovou konfiguraci libovolného chemického prvku či iontu. Počty elektronů v daném orbitalu se zapisují do pravého horního indexu. Například elektronová konfigurace atomu síry je 1s2 2s2 2p6 3s2 3p4. Uvedený zápis lze zjednodušit odkazem na předcházející vzácný plyn, kterým je v tomto případě neon. V případě atomu síry by zjednodušený zápis byl [Ne] 3s2 3p4, kde jsou 3s2 3p4 elektrony poslední slupky a říká se jim valenční elektrony.
Elektronová konfigurace
Elektronová konfigurace atomu má rozhodující vliv na jeho chemické a optické vlastnosti (vyzařované i absorpční spektrum). Elektrony nacházející se ve vnější slupce elektronového obalu se nazývají valenční. Především valenční elektrony jsou odpovědné za chemické vlastnosti atomu nebo molekuly, jejich chemické reakce a chemické vazby.
Pro konkrétní atom se číslo jeho valenční vrstvy shoduje s číslem periody (řádku), ve které se atom nachází v periodické tabulce objevené D. I. Mendělejevem. V tabulce jsou uvedeny prvky periodické tabulky podle jejich pořadí, které zároveň udává počet elektronů v jejich elektronovém obalu.
| Pořadí v periodické tabulce | Prvek | Elektrony v podslupkách (s, p, d, f) |
|---|---|---|
| 1 | vodík | 1 |
| 2 | helium | 2 |
| 3 | lithium | 2, 1 |
| 4 | berylium | 2, 2 |
| 5 | bór | 2, 3 |
| 6 | uhlík | 2, 4 |
| 7 | dusík | 2, 5 |
| 8 | kyslík | 2, 6 |
| 9 | fluor | 2, 7 |
| 10 | neon | 2, 8 |
| 11 | sodík | 2, 8, 1 |
| 12 | hořčík | 2, 8, 2 |
| 13 | hliník | 2, 8, 3 |
| 14 | křemík | 2, 8, 4 |
| 15 | fosfor | 2, 8, 5 |
| 16 | síra | 2, 8, 6 |
| 17 | chlor | 2, 8, 7 |
| 18 | argon | 2, 8, 8 |
| 19 | draslík | 2, 8, 8, 1 |
| 20 | vápník | 2, 8, 8, 2 |
| 21 | skandium | 2, 8, 9, 2 |
| 22 | titan | 2, 8, 10, 2 |
| 23 | vanad | 2, 8, 11, 2 |
| 24 | chrom | 2, 8, 13, 1 |
| 25 | mangan | 2, 8, 13, 2 |
| 26 | železo | 2, 8, 14, 2 |
| 27 | kobalt | 2, 8, 15, 2 |
| 28 | nikl | 2, 8, 16, 2 |
| 29 | měď | 2, 8, 18, 1 |
| 30 | zinek | 2, 8, 18, 2 |
| 31 | gallium | 2, 8, 18, 3 |
| 32 | germanium | 2, 8, 18, 4 |
| 33 | arsen | 2, 8, 18, 5 |
| 34 | selen | 2, 8, 18, 6 |
| 35 | brom | 2, 8, 18, 7 |
| 36 | krypton | 2, 8, 18, 8 |
| 37 | rubidium | 2, 8, 18, 8, 1 |
| 38 | stroncium | 2, 8, 18, 8, 2 |
| 39 | yttrium | 2, 8, 18, 9, 2 |
| 40 | zirkonium | 2, 8, 18, 10, 2 |
| 41 | niob | 2, 8, 18, 12, 1 |
| 42 | molybden | 2, 8, 18, 13, 1 |
| 43 | technecium | 2, 8, 18, 13, 2 |
| 44 | ruthenium | 2, 8, 18, 15, 1 |
| 45 | rhodium | 2, 8, 18, 16, 1 |
| 46 | palladium | 2, 8, 18, 18 |
| 47 | stříbro | 2, 8, 18, 18, 1 |
| 48 | kadmium | 2, 8, 18, 18, 2 |
| 49 | indium | 2, 8, 18, 18, 3 |
| 50 | cín | 2, 8, 18, 18, 4 |
| 51 | antimon | 2, 8, 18, 18, 5 |
| 52 | tellur | 2, 8, 18, 18, 6 |
| 53 | jód | 2, 8, 18, 18, 7 |
| 54 | xenon | 2, 8, 18, 18, 8 |
| 55 | cesium | 2, 8, 18, 18, 8, 1 |
| 56 | baryum | 2, 8, 18, 18, 8, 2 |
| 57 | lanthan | 2, 8, 18, 18, 9, 2 |
| 58 | cer | 2, 8, 18, 19, 9, 2 |
| 59 | praseodym | 2, 8, 18, 21, 8, 2 |
| 60 | neodym | 2, 8, 18, 22, 8, 2 |
| 61 | promethium | 2, 8, 18, 23, 8, 2 |
| 62 | samarium | 2, 8, 18, 24, 8, 2 |
| 63 | europium | 2, 8, 18, 25, 8, 2 |
| 64 | gadolinium | 2, 8, 18, 25, 9, 2 |
| 65 | terbium | 2, 8, 18, 27, 8, 2 |
| 66 | dysprosium | 2, 8, 18, 28, 8, 2 |
| 67 | holmium | 2, 8, 18, 29, 8, 2 |
| 68 | erbium | 2, 8, 18, 30, 8, 2 |
| 69 | thulium | 2, 8, 18, 31, 8, 2 |
| 70 | ytterbium | 2, 8, 18, 32, 8, 2 |
| 71 | lutecium | 2, 8, 18, 32, 9, 2 |
| 72 | hafnium | 2, 8, 18, 32, 10, 2 |
| 73 | tantal | 2, 8, 18, 32, 11, 2 |
| 74 | wolfram | 2, 8, 18, 32, 12, 2 |
| 75 | rhenium | 2, 8, 18, 32, 13, 2 |
| 76 | osmium | 2, 8, 18, 32, 14, 2 |
| 77 | iridium | 2, 8, 18, 32, 15, 2 |
| 78 | platina | 2, 8, 18, 32, 17, 1 |
| 79 | zlato | 2, 8, 18, 32, 18, 1 |
| 80 | rtuť | 2, 8, 18, 32, 18, 2 |
| 81 | thallium | 2, 8, 18, 32, 18, 3 |
| 82 | olovo | 2, 8, 18, 32, 18, 4 |
| 83 | bismut | 2, 8, 18, 32, 18, 5 |
| 84 | polonium | 2, 8, 18, 32, 18, 6 |
| 85 | astat | 2, 8, 18, 32, 18, 7 |
| 86 | radon | 2, 8, 18, 32, 18, 8 |
| 87 | francium | 2, 8, 18, 32, 18, 8, 1 |
| 88 | radium | 2, 8, 18, 32, 18, 8, 2 |
| 89 | aktinium | 2, 8, 18, 32, 18, 9, 2 |
| 90 | thorium | 2, 8, 18, 32, 18, 10, 2 |
| 91 | protaktinium | 2, 8, 18, 32, 20, 9, 2 |
| 92 | uran | 2, 8, 18, 32, 21, 9, 2 |
| 93 | neptunium | 2, 8, 18, 32, 22, 9, 2 |
| 94 | plutonium | 2, 8, 18, 32, 24, 8, 2 |
| 95 | americium | 2, 8, 18, 32, 25, 8, 2 |
| 96 | curium | 2, 8, 18, 32, 25, 9, 2 |
| 97 | berkelium | 2, 8, 18, 32, 27, 8, 2 |
| 98 | kalifornium | 2, 8, 18, 32, 28, 8, 2 |
| 99 | einsteinium | 2, 8, 18, 32, 29, 8, 2 |
| 100 | fermium | 2, 8, 18, 32, 30, 8, 2 |
| 101 | mendelevium | 2, 8, 18, 32, 31, 8, 2 |
| 102 | nobelium | 2, 8, 18, 32, 32, 8, 2 |
| 103 | lawrencium | 2, 8, 18, 32, 32, 8, 3 |
| 104 | rutherfordium | 2, 8, 18, 32, 32, 10, 2 |
| 105 | dubnium | 2, 8, 18, 32, 32, 11, 2 |
| 106 | Seaborgium | 2, 8, 18, 32, 32, 12, 2 |
| 107 | bohrium | 2, 8, 18, 32, 32, 13, 2 |
| 108 | hassium | 2, 8, 18, 32, 32, 14, 2 |
| 109 | meitnerium | 2, 8, 18, 32, 32, 15, 2 (?) |
| 110 | darmstadtium | 2, 8, 18, 32, 32, 16, 2 (?) |
| 111 | roentgenium | 2, 8, 18, 32, 32, 17, 2 (?) |
| 112 | Copernicium | 2, 8, 18, 32, 32, 18, 2 (?) |
| 113 | Nihonium | 2, 8, 18, 32, 32, 18, 3 (?) |
| 114 | Flerovium | 2, 8, 18, 32, 32, 18, 4 (?) |
| 115 | Moscovium | 2, 8, 18, 32, 32, 18, 5 (?) |
| 116 | Livermorium | 2, 8, 18, 32, 32, 18, 6 (?) |
| 117 | Tennessin | 2, 8, 18, 32, 32, 18, 7 (?) |
| 118 | Oganesson | 2, 8, 18, 32, 32, 18, 8 (?) |
Související články
Literatura
- Zdeněk Opava: Chemie kolem nás. Praha: Albatros, 1986, 13-751-86
Externí odkazy
 Obrázky, zvuky či videa k tématu Elektronový obal na Wikimedia Commons
Obrázky, zvuky či videa k tématu Elektronový obal na Wikimedia Commons
Reference
V tomto článku byly použity překlady textů z článků Electron na anglické Wikipedii a Elektron na německé Wikipedii.
Média použitá na této stránce
(c) JabberWok, CC BY-SA 3.0
A vector graphic similar of an image originally created by User:PAR, of the Bohr model.
Autor: Geek3, Licence: CC BY-SA 4.0
Collection of 16 atomic single-electron orbitals for the lowest four n quantum numbers. Only the cases with one radial node are shown. Each row shows one l-quantum number l=0 (s), l=1 (p), l=2 (d) and l=3 (f). The color depicts the complex-valued phase of the wavefunction. The right half depicts mz-eigenstates with m quantum numbers in ascending order showing complex phases and probability densities which are symmetric around the z-axis. The left half shows real-valued superpositions of ±m, which break the rotational symmetry and are often used in chemistry. The solid bodies enclose the volume where the continuous probability density exceeds a well-chosen threshold. The formulas that describe the orbitals can be found at Hydrogen atom.
The labels in the image show the quantum numbers nlm with l encoded as letter and m replaced by the spatial alignment for the real-valued superpositions.
Autor: Mets501, Licence: CC BY-SA 3.0
Hydrogen molecule showing proton and electron cloud
Autor: Naďa Čel, Licence: CC BY-SA 4.0
Znázornění zaplňování orbitalů na základě Pauliho principu výlučnosti a Hundova pravidla
Schematicke znazorneni prostoroveho rozlozeni pravdepodobnosti vyskytu elektronu v atomu vodiku pro nektera vlastni cisla
Autor: Naďa Čel, Licence: CC BY-SA 4.0
Grafické znázornění orbitalů s,p,d,f pomocí rámečků
Autor: Pellegatta Simone, Licence: CC BY-SA 4.0
Energetic levels and sublevels of polyelectronic atoms.