Ethylenaminy

Ethylenaminy jsou aminy, u kterých jsou aminové skupiny propojeny ethylenovými (-CH2CH2-) skupinami. Obvykle jsou to bezbarvé kapaliny s nízkou viskozitou a typickým aminovým zápachem. Nejčastěji se používají jako základní stavební prvky při přípravě složitějších molekul a při úpravách epoxidových pryskyřic.[1]
Výroba
Existují dva hlavní způsoby výroby ethylenaminů, reakce 1,2-dichlorethanu (ethylendichloridu) s amoniakem a reduktivní aminace monoethanolaminu. V roce 2001 se vyrobilo asi 385 000 tun ethylenaminů, většina z ethylendichloridu.[2]
Při výrobě z ethylendichloridu jako základní produkt vzniká ethylendiamin.[3] V přebytku ethylendichloridu se původní ethylenaminový řetězec rozšiřuje o jednu ethylenovou jednotku. Koncový alkylchlorid reaguje s amoniakem za tvorby aminu a polyaminový řetězec tak lze dále rozšiřovat. Přidáním polyaminu k původní reakční směsi se navyšuje tvorba polyaminů s delšími řetězci.[4] U této metody je k přeměně aminhydrochloridů na aminy potřeba stechiometrické množství zásady.
V monoethanolaminovém postupu reaguje ethanolamin s amoniakem za přítomnosti katalyzátoru obsahujícího přechodný kov. Tímto procesem vzniká více cyklických produktů než ethylendichloridovým postupem.[2]
U obou metod se vytváří směs několika produktů. Složení této směsi závisí na složení výchozího materiálu; jednotlivé produkty se oddělují destilací. Přidáním polyaminů s kratšími řetězci nebo jejich derivátů mohou být vytvořeny produkty s delšími řetězci.[5]
Vedlejší produkty
Kromě homologů ethylenaminu se vytváří také vedlejší produkty; například cyklizací chlorethylaminu se tvoří aziridiny a cyklizací sloučenin s dvěma ethylenovými jednotkami vznikají piperaziny.
Příklady
| Počet atomů dusíku | Název | Struktura | Teplota varu (°C, 100 kPa)[6] |
|---|---|---|---|
| 2 | Ethylendiamin (EDA) | 116,9 | |
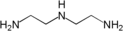
| 3 | Diethylentriamin (DETA) | 206,7 | |
| 3 | Aminoethylpiperazin (AEP) |  | 222,1 |
| 4 | Triethylentetraamin (lineární TETA) | 276,5 | |
| 4 | Tris(2-aminoethyl)amin (rozvětvený TETA) |  | |
| 4 | N,N'-Bis-(2-aminoethyl)piperazin) (bis-AEP) | ||
| 4 | N-[(2-Aminoethyl)2-aminoethyl]piperazin)/piperazinoethylethylendiamin (PEEDA) | ||
| 5 | Tetraethylenpentamin | Více sloučenin | ~200 |
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Ethyleneamine na anglické Wikipedii.
- ↑ Epoxy Curing Agents [online]. [cit. 2021-03-02]. Dostupné v archivu pořízeném dne 2018-04-17.
- ↑ a b Srivasan Sridhar; Richard G. Carter. Kirk-Othmer Encyclopedia of Chemical Technology. New York: John Wiley, 2001. doi:10.1002/0471238961.0409011303011820.a01.pub2. Kapitola Diamines and Higher Amines, Aliphatic.
- ↑ Production of aliphatic polyamines. Původce vynálezu: Nathan M. MNOOKIN. US. Patentový spis US2049467A. 1936-08-04. Dostupné: <online> [cit. 2024-09-24].
- ↑ Production of ethylene polyamines. Původci vynálezu: Stanley W. DYLEWSKI, Harvey G. DULUDE, Glenn W. WARREN. US. Patentový spis US2769841A. 1956-11-06. Dostupné: <online> [cit. 2024-09-24].
- ↑ Controlled production of ethylene amines. Původci vynálezu: Myrl LICHTENWALTER, Thomas H. COUR. US. Patentový spis US3484488A. 1969-12-16. Dostupné: <online> [cit. 2024-09-24].
- ↑ Ethyleneamines [online]. Huntsman, 2007 [cit. 2021-03-02]. Dostupné v archivu pořízeném dne 2019-03-06.
Externí odkazy
- Ethyleneamines Technical Manual. Dow [online]. 2019 [cit. 2024-09-24]. Dostupné online. (anglicky)
- Bezpečnostní list. Dow [online]. 2023-01-10 [cit. 2024-09-24]. Dostupné online.
Média použitá na této stránce
chemical structure of diethylene triamine
Structure of N1,N1'-(ethane-1,2-diyl)bis(ethane-1,2-diamine)
Skeletal formula of tris(2-aminoethyl)amine. Created using ACD/ChemSketch 10.0, Inkscape, and vim.
Ethylenediamine structural formula
Autor: W. Oelen, Licence: CC BY-SA 3.0
Ethylene diamine, reagent grade, 2 ml