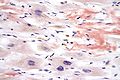
Fibróza

Barvení dle Movata (jádra a elastická vlákna černě; kolagen a retikulární vlákna žlutě; základní hmota a mucin modře; fibrin světle červeně; sval červeně)
Fibróza je stav zmnožení vaziva, typu pojivové tkáně, jakožto důsledku hojivého procesu po zánětu, zranění či reparativní reakce na různé typy podnětů, včetně příčin nejasné etiologie.[1] Byla nalezena souvislost s akumulací železa.[2]
Fibrotickým procesem se u parenchymatózních orgánů zvyšuje poměr vaziva na úkor funkční tkáně, dochází ke snížení fyziologické funkčnosti a jejich ztuhnutí.[3] Při hojení rány dochází ke vzniku fibrotické jizvy. Proliferativní zánět způsobuje přeměnu fibrinového exsudátu, organizaci fibrinu a novotvorbu cév s vazivem – granulační tkáně či hyperplazii. Dochází k pučení fibroblastů a tvorbě buněk endotelu. Proliferaci lze tlumit kortizonem.[4]
Typ nezhoubného mezenchymového nádoru fibrom vychází z fibrocytů produkujících kolagenní vlákna.[4]
Fyziologie
Při fibrotickém procesu je stimulována činnost fibroblastů produkujících kolagen a glykosaminoglykany. Proces je iniciován imunitními buňkami, včetně makrofágů, které uvolňují rozpustné faktory stimulující fibroblasty. Nejvíce charakteristickým profibrotickým mediátorem je skupina cytokinů TGF-β, sekretovaná makrofágy stejně tak i poškozenou tkání. Mezi další rozpustné mediátory fibrózy patří CTGF, růstový faktor PDGF a interleukin 4 (IL-4). Tyto molekuly aktivují dráhy signální transdukce AKT/mTOR[5] a SMAD do jádra,[6] což vyvolá aktivaci a proliferaci fibroblastů. Jejich činnost následně vede k ukládání extracelulární matrix a výstavbě pojivové tkáně. Tento komplexní proces tkáňové obnovy je regulován ve smyslu rovnováhy syntézy a degradace tak, aby byla zajištěna obnova architektury tkáně. Za patologických podmínek jako jsou vážná, dlouhodobá, opakovaná poškození tkáně či poruchy regulace v procesu hojení, může docházet k progresivním změnám s ireverzibilním fibrotickým poškozením.[3]
Příklady fibrotických procesů
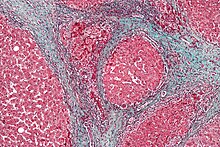
Fibrotický proces postihuje řadu tkání, typicky v důsledku zánětu či poškození:
- Plíce
- Plicní fibróza – skupina plicních chorob
- Cystická fibróza
- Idiopatická plicní fibróza
- Plicní fibróza – skupina plicních chorob
- Srdce
- Endomyokardiální fibróza
- Mozek
- Gliová jizva
- Další
- Artrofibróza (klouby)
- Dupuytrenova kontraktura (ruka)
- Morbus Peyronie (penis)
- Mediastinální fibróza (mediastinum)
- Myelofibróza (kostní dřeň)
- Retroperitoneální fibróza (retroperitoneum)
- Systémová nefrogenní fibróza (více orgánů)
- Systémová sklerodermie (více orgánů)
Reference
V tomto článku byl použit překlad textu z článku Fibrosis na anglické Wikipedii.
- ↑ BIRBRAIR, Alexander; ZHANG, Tan; FILES, Daniel C.; MANNAVA, Sandeep; SMITH, Thomas; WANG, Zhong-Min; MESSI, Maria L. Type-1 pericytes accumulate after tissue injury and produce collagen in an organ-dependent manner. Stem Cell Research & Therapy. 2014-11-06, s. 122. Dostupné online. ISSN 1757-6512. DOI 10.1186/scrt512. PMID 25376879. (anglicky)
- ↑ Iron accumulation: A new insight into fibrotic diseases. medicalxpress.com [online]. [cit. 2023-12-15]. Dostupné online.
- ↑ a b Neary; WATSON; BAUGH. Epigenetics and the overhealing wound: the role of DNA methylation in fibrosis. Fibrogenesis & Tissue Repair. 01/10/2015. Dostupné online [cit. 2016-04-13]. DOI 10.1186/s13069-015-0035-8. (anglicky)
- ↑ a b Josef Stejskal. Obecná patologie v poznámkách. Jinočany: 2. lékařská fakulta Univerzity Karlovy, 1992. S. 49–50, 78.
- ↑ Mitra A, Luna JI, Marusina AI, Merleev A, Kundu-Raychaudhuri S, Fiorentino D, Raychaudhuri SP, Maverakis E. Dual mTOR Inhibition Is Required to Prevent TGF-β-Mediated Fibrosis: Implications for Scleroderma.. J Invest Dermatol. 2015, s. 2873–6. DOI 10.1038/jid.2015.252. PMID 26134944. (anglicky)
- ↑ Leask A, Abraham DJ. TGF-beta signaling and the fibrotic response. FASEB Journal. 2004, s. 816–827. DOI 10.1096/fj.03-1273rev. PMID 15117886. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu Fibróza na Wikimedia Commons
Obrázky, zvuky či videa k tématu Fibróza na Wikimedia Commons
Média použitá na této stránce
Autor: Nephron, Licence: CC BY-SA 3.0
High magnification micrograph of senile cardiac amyloidosis. Movat stain (black = nuclei, elastic fibres; yellow = collagen, reticular fibers; blue = ground substance, mucin; bright red = fibrin; red = muscle). Autopsy specimen.
The micrograph shows amyloid (extracellular muddy brown material - right of image), abundant lipofuscin (dark red granular material) and myocardial fibrosis (yellow - left of image).
Related images
-
Intermed. mag. (H&E).
-
High mag. (H&E).
-
Very high mag. (H&E).
-
Intermed. mag. (congo red).
-
High mag. (congo red).
-
Very high mag. (congo red).
-
Very high mag. (Movat's stain).
Autor: Nephron, Licence: CC BY-SA 3.0
Histologický obraz cirhózy etylické etiologie (trichrom)