Fischerovy karbeny
Fischerovy karbeny jsou karbenové organické ligandy v organokovových sloučeninách, přičemž karben je zde σ-donorem a π-akceptorem. Protože u nich π-retrodonace z kovu bývá slabá, tak má karbenový uhlík vlastnosti elektrofilu.
Tato skupina karbenů je nazvána po Ernstu Ottu Fischerovi.
Struktura
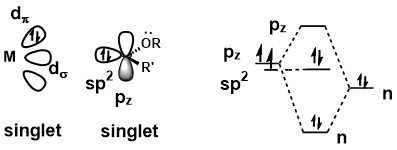
Karbenový komplex kovu je Fischerovým karbenem, pokud je karben v singletovém stavu. Delokalizace volného elektronového páru substituentu na karbenovém uhlíku navyšuje energii orbitalu pz, v důsledku čehož zůstávají dva elektrony karbenu v podobě elektronového páru. Vazby mezi karbenem a kovem vytváří silné dodávání σ elektronů z orbitalu sp2 do prázdného orbitalu d u kovu a slabou π-retrodonaci z kovu do prázdného orbitalu pz. Z důvodu nízké míry π-donace je karbenový uhlík elektrofilní.[1]
Vzhledem k těmto vlastnostem vazeb se Fischerovy karbeny často vyznačují:
- kovy v nízkých oxidačních číslech
- přítomností středních a pozdních přechodných kovů, jako jsou Fe0, Mo0 a Cr0
- π-akceptorovými ligandy
- π-donorovými substituenty, například alkoxy a alkylovanými aminoskupinami, na karbenových uhlících.
Příprava
Nejčastějším způsobem přípravy Fischerova karbenu je postup začínající reakcí karbonylu s organolithnou sloučeninou. Vzniklá sloučenina, podobná lithnému enolátu, je stabilizovaná a je tak třeba použít silně elektrofilní alkylační činidlo, jako například Meerweinovu sůl.[2]
Za přítomnosti katalyzátoru fázového přenosu je možné k alkylaci použít jodmethan.[3]
Lithný kation lze zaměnit za tetraalkylamonný, vzniklý enolát je poté reaktivnější. Tetraalkylamonnou sůl je možné acylovat a získat tak vysoce elektrofilní karben obsahující smíšený anhydrid, jenž může vstupovat do nukleofilních substitučních reakcí s alkoholy.[4]
Fischerovy karbeny obsahující α-vodíky se připravují reakcemi karbonylových aniontů s formamidem. Konečný produkt se vytváří reakcí mmeziproduktu s nadbytkem trimethylsilylchloridu.[4]
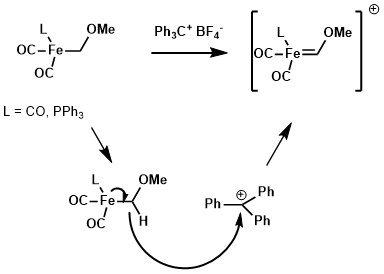
Za přítomnosti vhodné sloučeniny, například tritylového kationtu, lze odštěpit hydridové ionty z alkylových ligandů kovových komplexů a vytvořit tak Fischerovy karbeny.[2]
Deckarbonylace nestabilizovaných karbenoidů
Fischerovy karbeny mohou být získány dekarbonylacemi karbenoidů odvozených od stabilizovaných diazosloučenin.[5]

Reakce
Reakce podobné karbonylům
Karbenový uhlík Fischerových karbenů je elektrofilní a Fischerovy karbeny tak vstupují do podobných reakcí jako karbonylové sloučeniny. Řadu z nich, například transesterifikace, Michaelovy reakce a aldolové reakce, lze popsat s využitím ekvivalentní karboxylové struktury. Skupina Cr(CO)5 způsobuje vydatné odtahování elektronů a α-proton je tak silně kyselý. Karben odvozený od methoxychromu, s methylovým postranním řetězcem má ve směsi vody a acetonitrilu (v poměru objemů 1:1) pKa 12,5.[6][7] U methylacetátu je pKa 25,6, protože se zde neobjevuje odtahování elektronů prostřednictvím Cr(CO)5.
Odtahování elektronů ve Fischerových karbenech se projevuje i na dalších reakcích, jako je Dielsova-Alderova reakce methylakrylátu s isoprenem, která po 7 dnech za pokojové teploty vykazuje jen mírnou para-meta selektivitu, zatímco u odpovídajícího Fischerova karbenu se za pouhé 3 hodiny dosahuje výrazně vyšší para-meta selektivity.[8]
Urotropin, který je slabým nukleofilem, se může účastnit Michaelových adicí na alkynylové Fischerovy karbeny, přičemž se utváří produkty dvojnásobných adicí.[9]
Enoláty vzniklé deprotonacemi Fischerových karbenů lze alkylovat, protože je však karbanion stabilizován, tak je potřeba reaktivní alkylační činidlo, například methylfluorosulfonát nebo methylbromacetát.[10][11]
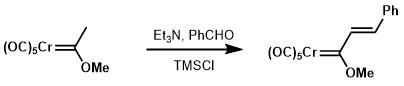
K provedení aldolových kondenzací Fischerových karbenů postačují slabší zásady, například triethylamin, než u karbonylových sloučenin.[12][13]
Demetalace
Fischeovy karnbeny mohou být oxidovány na karbonylové sloučeniny i mírnými oxidanty, jako je dusičnan amonno-ceričitý.[2]
Pokud se na vedlejším řetězci Fischerova karbenu nachází α-proton, tak může být vratně odštěpen slabou zásadou, například pyridinem. Při těchto reakcích se vytvářejí chromhydridové meziprodukty, u kterých poté probíhají redukční eliminace za vzniku cis-enoletherů.[14]
Fotochemické vlastnosti Fischerových karbenů
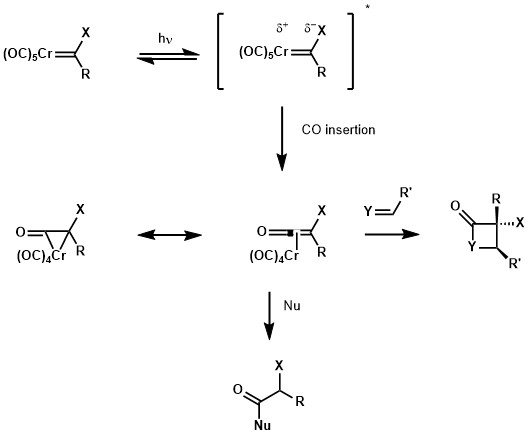
Ultrafialovo-viditelná spektra Fischerových karbenů obsahují absorpční pásy vazeb kov-ligand v blízké ultrafialové oblasti. Příslušná excitace způsobí přesun elektronu z orbitalu kovu do orbitalu ligandu, což zvýší elektronovou hustotu na karbenovém uhlíku. Kovové centrum, mající již pod vlivem karbonylových ligandů nízkou elektronovou hustotu, se stane ještě chudším na elektrony, což vyvolá migrační inserci na CO ligand a vytvoří se Cr-metalocyklopropanon, jenž je rezonanční formou metalovaného ketenu. S využitím reaktivity ketenů lze tuto sloučeninu zachytit pomocí některých nukleofilů, jako jsou alkoholy a aminy, nebo nechat reagovat v [2+2] cykloadicích s alkeny za vzniku cyklobutanů, iminy za vzniku β-laktamů, či s aldehydy na β-laktony.[15]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Fischer carbene na anglické Wikipedii.
- ↑ Robert Crabtree. The Organometallic Chemistry of the Transition Metals 7th edition. [s.l.]: [s.n.], 2019-07-18. ISBN 978-1119465881.
- ↑ a b c Karl Heinz Dötz. Carbene Complexes in Organic Synthesis [New Synthetic Methods (47)]. Angewandte Chemie International Edition in English. 1984, s. 587–608. DOI 10.1002/anie.198405871.
- ↑ Thomas R. Hoye; Kejian Chen; James R. Vyvyan. Preparation of Fischer carbene complexes by alkylation of acylmetalates with alkyl iodides. Organometallics. 1993, s. 2806–2809. DOI 10.1021/om00031a056.
- ↑ a b Roderick Bates. Organic synthesis using transition metals. Chichester, West Sussex: [s.n.], 2012. ISBN 9781119978947.
- ↑ María Álvarez; Maria Besora; Francisco Molina; Feliu Maseras; Tomás R. Belderrain; Pedro J. Pérez. Two Copper-Carbenes from One Diazo Compound. Journal of the American Chemical Society. 2021, s. 4837–4843. DOI 10.1021/jacs.1c01483. PMID 33733762.
- ↑ Claude F. Bernasconi; Weitao Sun. Physical Organic Chemistry of Transition Metal Carbene Complexes. 8.1 Kinetic and Thermodynamic Acidities of Alkoxyalkylcarbene Pentacarbonyl Complexes of Cr, Mo, and W in Aqueous Acetonitrile. Dependence on Metal, Alkyl Group, and Alkoxy Group. Organometallics. 1997, s. 1926–1932. DOI 10.1021/om960936.
- ↑ Claude F. Bernasconi; Aquiles E. Leyes; Mark L. Ragains; Yan Shi; Huan Wang; William D. Wulff. Physical Organic Chemistry of Transition Metal Carbene Complexes. 14.1 Thermodynamic Acidity Measurements of Fischer Carbene Complexes in Acetonitrile. Journal of the American Chemical Society. 1998, s. 8632–8639. DOI 10.1021/ja980608w6.
- ↑ William D. Wulff; Dominic C. Yang. Diels-Alder reactions of Fischer carbene complexes. Journal of the American Chemical Society. 1983, s. 6726–6727. DOI 10.1021/ja00360a037.
- ↑ Rudolf Aumann; Peter Hinterding; Carl Krüger; Richard Goddard. Organische Synthesen mit Übergangsmetall-Komplexen LXV. Aldehyde durch Hydrolyse der M=C-Bindung von Alkoxycarben-Chromkomplexen mit Wasser/Urotropin. Ein zweikerniger verbrückter (β-Amino)vinylcarben-Chromkomplex durch Fragmentierung von Urotropin. Journal of Organometallic Chemistry. 1993, s. 145–149. DOI 10.1016/0022-328X(93)86066-Q.
- ↑ Charles P. Casey; Roger A. Boggs; Ronald L. Anderson. Generation and reactions of anions .alpha. to the carbene carbon atom of transition metal-carbene complexes. Journal of the American Chemical Society. 1972, s. 8947–8949. DOI 10.1021/ja00780a073.
- ↑ Charles P. Casey; Ronald L. Anderson. Reactions of conjugate bases of metal carbene complexes with expoxides and with α-bromo esters. Journal of Organometallic Chemistry. 1974, s. C28–C30. DOI 10.1016/S0022-328X(00)85646-6.
- ↑ Rudolf Aumann; Heinrich Heinen. Organische Synthesen mit übergangsmetallkomplexen, 211) 1-Chroma-1,3-butadiene und 1-Chroma-1,3,5-hexatriene aus (CO)5Cr=C(OC2H5)CH3 durch Carbonyl-Olefinierung mit Triethylamin/Chlortrimethylsilan. Chemische Berichte. 1987, s. 537–540. DOI 10.1002/cber.19871200413.
- ↑ Charles P. Casey; William R. Brunsvold. Synthesis of α-methylene-γ-butyrolactone via transition metal carbene complexes. Journal of Organometallic Chemistry. 1975, s. 175–183. DOI 10.1016/S0022-328X(00)88585-X.
- ↑ Björn C. Söderberg; Jian Liu; Thomas W. Ball; Michael J. Turbeville. Thermal Decomposition of Pentacarbonyl(1-acyloxyalkylidene)chromium(0) Complexes: Formation of Z -Enol Esters. The Journal of Organic Chemistry. 1997, s. 5945–5952. DOI 10.1021/jo962197c.
- ↑ Louis S. Hegedus. Chromium carbene complex photochemistry in organic synthesis. Tetrahedron. 1997, s. 4105–4128. DOI 10.1016/S0040-4020(96)01186-6.
Související články
- Wulffova–Dötzova reakce
Média použitá na této stránce
Autor: Bdoan, Licence: CC BY-SA 4.0
Preparation of Fischer carbene 2
Autor: Bdoan, Licence: CC BY-SA 4.0
Preparation of Fischer carbene 5
step 2 of synthesis of Fischer carbene
step 1 of synthesis of Fischer carbene