Fluorid inditý
| Fluorid inditý | |
|---|---|
 | |
| Obecné | |
| Systematický název | Fluorid inditý |
| Anglický název | Indium(III) fluoride |
| Německý název | Indium(III)-fluorid |
| Sumární vzorec | InF3 |
| Vzhled | bílá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 7783-52-0 |
| EC-no (EINECS/ELINCS/NLP) | 232-005-0 |
| PubChem | 82212 |
| SMILES | F[In](F)F |
| InChI | InChI=1S/3FH.In/h3*1H;/q;;;+3/p-3 Key: JNLSTWIBJFIVHZ-UHFFFAOYSA-K |
| Vlastnosti | |
| Molární hmotnost | 171,82 g/mol |
| Teplota tání | 1172 °C (2142 °F; 1445 K) |
| Teplota varu | >1200 °C (>2192 °F; >1473,15 K) |
| Hustota | 4,39 g/cm3 |
| Index lomu | 1,453 |
| Rozpustnost ve vodě | 0,4 g·l−1 při 20 °C |
| Struktura | |
| Krystalová struktura | romboedrická |
| Hrana krystalové mřížky | a = 5,4103 Å c = 14,3775 Å |
| Bezpečnost | |
| H-věty | H301, H315, H319, H335 |
| P-věty | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405, P501 |
Některá data mohou pocházet z datové položky. | |
Fluorid inditý je anorganická sloučenina s chemickým vzorcem InF3.
Příprava
Fluorid inditý lze vyrábět pyrolýzou hexafluoroinditanu amonného pod proudem fluoru:[1]
(NH4)3[InF6] → InF3 + 3 NH4F
Možná je také příprava reakcí oxidu inditého s fluorem:[1]
2 In2O3 + 6 F2 → 4 InF3 + 3 O2
nebo reakcí chloridu inditého s fluorovodíkem při 100 °C:[1]
InCl3 + 3 HF → 3 HCl + InF3
Vlastnosti
Fluorid inditý je bílá pevná látka, která je odolná vůči studené i teplé vodě.[1] Ve vroucí vodě hydrolyzuje na oxyfluorid inditý.[2] Fluorid inditý se ve vodě rozpouští velmi málo, ale je snadno rozpustný ve zředěných kyselinách. Fluorid inditý se redukuje na téměř čistý fluorid indno-inditý pod velmi pomalým proudem vodíku za 300 °C a na kovové indium pod rychlým proudem vodíku.[1]
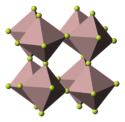
Struktura fluoridu inditého je romboedrická, podobná struktuře fluoridu rhoditého s prostorovou grupou R3c (číslo 167) (a = 5,4103 Å, c = 14,3775 Å).[3] Každé z center je oktaedrické.[4]
Využití
Fluorid inditý se využívá při přípravě neoxidových skel. Používá se také jako katalyzátor adice trimethylsilylkyanidu na aldehydy za vzniku kyanhydrinů.[5][6]
Reference
V tomto článku byly použity překlady textů z článků Indium(III) fluoride na anglické Wikipedii a Indium(III)-fluorid na německé Wikipedii.
- ↑ a b c d e BRAUER, Georg. Handbuch der präparativen anorganischen Chemie. [s.l.]: F. Enke 626 s. Dostupné online. ISBN 978-3-432-02328-1. S. 240. (německy)
- ↑ ZUCKERMAN, J. J.; HAGEN, A. P. Inorganic Reactions and Methods, The Formation of Bonds to Hydrogen (Part 1). [s.l.]: John Wiley & Sons 360 s. Dostupné online. ISBN 978-0-470-14536-4. (anglicky)
- ↑ HOPPE, R.; KISSEL, D. Zur kenntnis von AlF3 und InF3 [1]. Journal of Fluorine Chemistry. 1984-03, roč. 24, čís. 3, s. 327–340. Dostupné online [cit. 2023-10-07]. DOI 10.1016/S0022-1139(00)81321-4. (německy)
- ↑ HEBECKER, Christoph; HOPPE, Rudolf. Zur Kristallstruktur von Indium- und Thalliumtrifluorid. Die Naturwissenschaften. 1966, roč. 53, čís. 4, s. 104–104. Dostupné online [cit. 2023-10-07]. ISSN 0028-1042. DOI 10.1007/BF00601468. (německy)
- ↑ RAHMAN, Atta-ur-. Advances in Organic Synthesis. [s.l.]: Bentham Science Publishers 566 s. Dostupné online. ISBN 978-1-60805-197-7. S. 192. (anglicky)
- ↑ Indium(III) fluoride [online]. Sigma-Aldrich [cit. 2023-10-06]. Dostupné online.
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
(c) Materialscientist na projektu Wikipedie v jazyce angličtina, CC BY-SA 3.0
Structure of FeF3, AlF3 or InF3
Journal = JOURNAL OF FLUORINE CHEMISTRY, Year = 1984, Volume = 24, Page = 327–340, Title = ZUR KENNTNIS VON AlF3 UND InF3, Authors = Hoppe R., Kissel D.