Fosfity

Fosfity nebo fosfitové estery jsou organické sloučeniny s obecným vzorcem P(OR)3. V podstatě se jedná o estery kyseliny fosforité, nestabilního tautomeru kyseliny fosfonové. Nejjednodušší takovou sloučeninou je trimethylfosfit, P(OCH3)3. K částečně esterifikovaným formám této kyseliny patří dialkylfosfity, například dimethylfosfit, HP(O)(OCH3)2. Obvykle jde o bezbarvé kapaliny.
Příprava
Z chloridu fosforitého
Fosfity se nejčastěji připravují reakcí chloridu fosforitého s odpovídajícím alkoholem. Podle podmínek reakce mohou vznikat dialkylfosfity:[1]
- PCl3 + 3 C2H5OH → (C2H5O)2P(O)H + 2 HCl + C2H5Cl
nebo, za přítomnosti akceptorů protonů, C3-symetrické trialkoxyfosfity.[2]
- PCl3 + 3 C2H5OH + 3 R3N → (C2H5O)3P + 3 R3NHCl
U obou těchto druhů bylo připraveno mnoho různých sloučenin.
Transesterifikací
Fosfity lze také získat transesterifikací.[3] Tato reakce je vratná a dá se použít také na přípravu smíšených fosfitů (s různými alkylovými skupinami). Při použití fosfitu odvozeného od těkavého alkoholu, například trimethylfosfitu, lze alkohol odstranit destilací, což umožní úplné provedení reakce.
Reakce a použití trisfosfitů

Tris(2,4-di-terc-butylfenyl)fosfit, látka používaná jako stabilizátor polymerů
Fosfity mohou být oxidovány na fosfátové estery:
- P(OR)3 + [O] → OP(OR)3
Tato reakce znemožňuje využití některých fosfitů ke stabilizaci polymerů.[4]
Alkylfosfity se používají v Perkowově reakci k přípravě vinylfosfonátů a v Michaelisově–Arbuzovově reakci k přípravě fosfonátů. Arylfosfity se těchto reakcí neúčastní a tak jsou používány jako stabilizátory halogenovaných polymerů jako je polyvinylchlorid (PVC).
Fosfity lze použít jako redukční činidla, například diethylfosfit redukuje některé hydrogenperoxidy na alkoholy vytvořené autooxidací;[5] fosfity se přitom přeměňují na fosfátové estery.
Homogenní katalýza
Fosfity fungují jako Lewisovy zásady a mohou tak tvořit komplexy s ionty mnoha kovů. K nejčastěji používaným fosfitovým ligandům patří triethylfosfit ((EtO)3P), trimethylolpropanfosfit a trifenylfosfit. Fosfity mají menší Tolmanův úhel než podobné fosfinové ligandy. Jsou součástmi katalyzátorů využívaných průmyslově při hydroformylačních a hydrokyanačních reakcích.[6]

Odkazy
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu Fosfity na Wikimedia Commons
Obrázky, zvuky či videa k tématu Fosfity na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Phosphite ester na anglické Wikipedii.
- ↑ John E. Malowan. Diethyl phosphite. Inorganic Syntheses. 1953, s. 58–60. DOI 10.1002/9780470132357.ch19.
- ↑ A. H. FORD-MOORE; B. J. PERRY. Triethyl Phosphite. Org. Synth.. 1963. Dostupné online.; Coll. Vol.. S. 955.
- ↑ Friedrich W. Hoffmann; Richard J. Ess; Robert P. Usingef. The Transesterification of Trialkyl Phosphites with Aliphatic Alcohols. Journal of the American Chemical Society. 1956, s. 5817–5821. DOI 10.1021/ja01603a026.
- ↑ Rainer Wolf; Bansi Lal Kaul. Ullmann's Encyclopedia Of Industrial Chemistry. [s.l.]: [s.n.], 2000. DOI 10.1002/14356007.a20_459. Kapitola Plastics, Additives.
- ↑ J. N. Gardner; F. E. Carlon; O. Gnoj. One-step procedure for the preparation of tertiary α-ketols from the corresponding ketones. The Journal of Organic Chemistry. 1968, s. 3294–3297. DOI 10.1021/jo01272a055.
- ↑ Aitor Gual; Cyril Godard; Verónica de la Fuente; Sergio Castillón. Phosphorus(III) Ligands in Homogeneous Catalysis: Design and Synthesis. Příprava vydání Paul C. J. Kamer, Piet W. N. M. van Leeuwen. [s.l.]: John Wiley & Sons, 2012. DOI 10.1002/9781118299715.ch3. Kapitola Design and Synthesis of Phosphite Ligands for Homogeneous Catalysis.
- ↑ Gregory D. Cuny; Stephen L. Buchwald. Practical, High-Yield, Regioselective, Rhodium-Catalyzed Hydroformylation of Functionalized α-olefins. Journal of the American Chemical Society. 1993, s. 2066–2068. DOI 10.1021/ja00058a079.
- ↑ Annemiek Van Rooy; Paul C. J. Kamer; Piet W. N. M. Van Leeuwen; Kees Goubitz; Jan Fraanje; Nora Veldman; Anthony L. Spek. Bulky Diphosphite-Modified Rhodium Catalysts: Hydroformylation and Characterization. Organometallics. 1996, s. 835–847. Dostupné online. DOI 10.1021/OM950549K.
Média použitá na této stránce
(c) V8rik from en.wikipedia.org, CC BY-SA 3.0
Triethylphosphite reduction
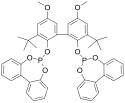
structure of BiPhePhos
Chemical diagram for a generic phosphite