Hemodialýza

Hemodialýza je metoda odstraňování odpadních látek jako např. draslík, močovina, a nadbytečné vody z krve při selhání ledvin. Hemodialýza je jednou ze tří terapií náhrady funkce ledvin (dalšími dvěma jsou transplantace ledvin a peritoneální dialýza).
Hemodialýza může být prováděna buď ve středisku nebo v nemocnici, domácí hemodialýza není příliš častá. Pravidelná hemodialýza je prováděna v nemocnici nebo v samostatných dialyzačních střediscích se školenými ošetřovatelkami, techniky atd., domácí dialýza s pomocí zaškoleného pomocníka, obvykle člena rodiny.
Princip
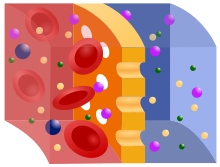
Princip hemodialýzy spočívá v difuzi rozpuštěných látek přes semipermeabilní membránu (polopropustný filtr). Používá se tzv. protisměrný (protiběžný) tok, kdy dialyzační roztok (obvykle o průtoku 500–800 ml/min) protéká podél membrány v opačném směru než jakým teče krev, při němž nastává největší lokální rozdíl koncentrací a dialýza je tak nejúčinnější.
Difúze
Nežádoucí látky s vysokou koncentrací v krvi (např. močovina) přechází dírkami v membráně do dialyzačního roztoku, kde je jejich koncentrace nulová. Kdyby do dialyzátoru nebyl přiváděn stále nový dialyzační roztok, koncentrace nežádoucích látek v krvi a v roztoku by se za určitou dobu vyrovnaly, další nežádoucí látky by pak do roztoku přestaly z krve přecházet a čištění by se zastavilo. Proto je nutné přivádět na membránu stále nový čistý dialyzační roztok.
Schopnost molekul přecházet dírkami v membráně vyjadřujeme číslem mezi 0 a 1, nazvaným ultrafiltrační koeficient, toto číslo závisí samozřejmě hlavně na velikosti dané molekuly. Koeficient 1 označuje rozpuštěnou látku, která prochází zcela bez potíží, tj. s malou molekulou, jako je močovina, cukr, elektrolyty (Na, K,Cl), naopak látky s velkou molekulou, které se prosévají špatně nebo vůbec mají koeficient blížící se 0.
Pomocí difúze lze:
- odstraňovat nežádoucí látky s malou molekulou z krve
- doplňovat do organizmu chybějící látky s malou molekulou
Clearence
Clearance (z anglického clear = čistit) je množství plazmy, které se očistí od této látky za jednotku času. Číselně jde o takový objem krevní plazmy, která je za jednotku času zcela očištěna od dané látky z organizmu. Protože se clearence u různých látek liší, uvádí se vždy, o clearence jaké látky se jedná; nejčastěji se sleduje clearence močoviny a clearence kreatininu.
Clearence závisí na:
- rychlosti proudící krve – od určité rychlosti toku krve se však již clearence nezvyšuje
- rozdílu koncentrací dané látky na obou stranách membrány
- složení dialyzačního roztoku[zdroj?]
- vlastnostech membrány – difúzní koeficient
- velikosti dialýzovaných molekul
Odstraňování vody (ultrafiltrace) se provádí snížením osmotického tlaku dialyzačního roztoku, který pak nadbytečnou vodu spolu s některými rozpustnými složkami přes membránu „vysaje“.
Dialyzační roztok je sterilním roztokem minerálních iontů a glukózy. Močovina a jiné odpadní látky, jako např. draslík a fosfor difundují skrze membránu do dialyzačního roztoku, ovšem koncentrace minerálů a glukózy je v něm stejná jako v krevní plazmě, aby nedocházelo k jejich ztrátám. Pro dorovnání pH krve je do roztoku přidán bikarbonát ve vyšší koncentraci, než je v krevní plazmě.
Vlastní dialyzátor (dialyzační patrona) se skládá z polyuretanového pouzdra, ve kterém jsou uloženy kapiláry se semipermeabilní stěnou, kterými protéká nesrážlivá krev. Zevně jsou kapiláry oplachovány dialyzačním roztokem.
Nastavení
O nastavení parametrů dialýzy rozhoduje nefrolog (specialista na nemoci ledvin). Těmito parametry jsou frekvence (kolikrát týdně bude dialýza probíhat), délka (počet hodin), potřebný minimální průtok krve a dialyzačního roztoku a velikost filtru. Obecně čím má kdo větší hmotnost, tím více potřebuje zdialyzovat, nejčastěji to bývají 3–4 hodiny (velcí pacienti 5 hodin) třikrát týdně, dvakrát týdně chodí pacienti se zbytkovou funkcí ledvin, čtyřikrát týdně buď velmi velcí nebo dočasně silně převodnění pacienti (velké množství vody je nutno odstraňovat pozvolna kvůli vedlejším účinkům).
Vedlejší účinky a komplikace
Při dialýze se obvykle odstraňuje nadbytečná voda z těla, protože většina pacientů už nemočí vůbec nebo skoro vůbec. Tak rychlé odstranění relativně velkého množství vody může způsobit snížení krevního tlaku, vyčerpanost, bolest na hrudi, křeče v nohou, nevolnost a bolest hlavy. Tyto potíže se mohou objevit během dialýzy a pokračovat i po jejím skončení, jejich intenzita je obvykle úměrná množství odstraňované vody, nicméně tato úměra je u různých pacientů velmi odlišná. Tyto nepříjemnosti lze odstranit nebo snížit větší sebekázní v příjmu tekutin (překonáváním nebo oklamáním žízně) nebo častější či delší dialýzou než obvyklé 4–5 hodin třikrát týdně, velké snížení krevního tlaku (bolest a točení hlavy, mžitky před očima na omdlení) lze ihned mírnit přidáním dodatečné tekutiny do vracené krve.
Existují dvě klinické jednotky dialyzační hypotenze
- Občasná hypotenze, která se obvykle vyskytuje před koncem dialýzy a bývá spojena se zvracením, svalovými křečemi nebo i jinými příznaky z dráždění bloudivého nervu (např. zívání.)
- Chronická přetrvávající hypotenze, ke které dochází v důsledku několikaleté léčby chronickou hemodialýzou. Tito pacienti mají systolický TK (tlak krevní) nižší než 100 mmHg.
Faktory přispívající k hypotenzi na dialýze
Seřazeno zhruba od nejběžnějších ke vzácným:
- rychlé snížení plazmatické osmolality, rychlé odstranění tekutiny ve snaze dosáhnout „suchá hmotnost“, u pacientů s velkými mezidialyzačními váhovými přírůstky
- nepřesně určená „suchá hmotnost“
- autonomní neuropatie – postižení bloudivého nervu, dále tzv. „autonomní nervová dysfunkce“ – u dialýzovaných s diabetem bývají časté
- snížení srdeční rezervy (viz „Zlepšení výkonnosti kardiovaskulárního“ dále v textu)
- užívání antihypertenzních léků, které mohou kardiovaskulární stabilitu paradoxně zhoršit
- nesprávná dialyzační taktika (nižší obsah sodíku v dialyzačním roztoku)
- náhlé uvolnění adenosinu během orgánové ischémie
- jídlo podané těsně před nebo během dialýzy
- arytmie nebo perikardiální výpotek s tamponádou (pozor – jedná se o hypotenze nereagující na infusi)
- alergická reakce na dialyzační membránu, což může způsobit, sípání a dušnost, stejně jako hypotenze
- zvýšená syntéza endogenních vazodilatačních látek, jako například oxidu dusnatého (NO)
- ostatní příčiny, jako jsou např. infarkt srdce, hemolýsa, krvácení, infekce, embolie vzduchu do žilního systému (ty jsou sice nepříliš časté, ale na druhou stranu vyžadují okamžitou pozornost lékaře a urgentní léčbu)
Diagnóza hypotenze
- asymptomatická hypotenze – bezpříznaková
- symptomatická hypotenze s těmito příznaky: bolení hlavy, svalové křeče, nevolnost, zvracení, nevůle, zívání, nucení na stolici, tlak za sponou stydkou, dušnost
Léčba hypotenze
Pacient je uložen do Trendelenburgovy polohy, tedy polohy se zvýšenými dolními končetinami a sníženou hlavou. Dalším krokem je snížení rychlosti krevní pumpy na dialyzačním monitoru a zvýšení intravaskulárního objemu např. rychlou infúzí fyziologického roztoku do krevního oběhu.
Zásadní je rychlá identifikace život ohrožující příčiny nízkého krevního tlaku:
Pacientům s chronickou hypotenzí v důsledku neschopnosti adekvátně reagovat na rychlé změny v objemu krve může pomoci převedení na peritoneální dialýzu. Další možností je prodloužení dialyzačního času a/nebo zvýšení frekvence hemodialýzy, nebo převedení pacienta na noční pozvolnou, nízkoprůtokovou 6–8 hodin trvající dialýzu.
Prevence hypotenze
Přesné stanovení tzv. suché váhy
Suchá váha se stále ještě stanovuje na základě empirie – pomocí pokusů a omylů. Suchá hmotnost je taková, pod níž se začnou vyskytovat nepříjemné příznaky: nevolnost a zvracení, či hypotenze. Suchá hmotnost je často proměnlivá a může kolísat i každou dialýzu. Většinou se však mění při přidruženém onemocnění (např. průjmová onemocnění nebo infekce) nebo i se změnami v hemoglobinu. (např. se zvýšenou dávkou erytropoetinu se zvyšuje chuť k jídlu a pacient přibývá na váze.).
Suchá váha se dnes dá určit i objektivně, pomocí monitorování krevního objemu (BVM přístroj – blood volum monitoring) či pomocí bioimpedančních přístrojů. Velice perspektivní se jeví bioimpedanční měření, kterým se posuzuje změna objemů extracelulárních a intracelulárních tekutin.
Modelování ultrafiltrace a natria (Na)
Tzn. na začátku dialýzy se nastaví vyšší ultrafiltrace (UF – odebírání vody z těla) a sodík nad 140 mmol/l a na konci dialýzy je UF nižší a Na se nastaví pod 140. Modelování Na a UF však pomáhá jen v některých vybraných případech. Účinné je spíše u občasné hypotenze. Vysoký obsah sodíku v dialyzačním roztoku zabraňuje výraznému poklesu v plazmě, poklesu osmolality během dialýzy, čímž brání poklesu extracelulárního objemu a minimalizuje (osmotický) ztráty tekutin z buněk.
Modelování natria má svá úskalí, např. může zvýšit postdialyzační žízeň a hypertenzi, což vede k vyšším mezidialyzačním přírůstkům na váze.
Snížit teplotu dialyzátu na 34,5–35 °C
Nízká teplota dialyzačního roztoku může zlepšit hemodynamickou stabilitu, zlepšuje kontraktilitu svalstva v cévách, čímž se zvyšuje žilní tonus. Empiricky bylo pozorováno, že chronická hemodiafiltrace může vést k větší stabilitě ve srovnání s hemodialýzou. To se dnes vysvětluje tím, že je krev ochlazována roztokem přikapávající během hemodiafiltrační procedury. Také snížení teploty není samospasitelné. Dialyzování pacienti jsou většinou zimomřiví, když jim snížíme teplotu dialyzátu, (roztoku, které oplachuje krev na druhé straně dialyzační membrány), tak to špatně snášejí. Na druhou stranu snížení teploty dialyzátu možno s výhodou uplatnit v letním období veder k ochlazování pacientů. Otázka změny účinnosti dialýzy při snížené teplotě, (změna kinetiky malých molekul)je zatím předmětem výzkumu.
Velkou dispozici k chronické hypotenzi mají kardiaci.
Zlepšení kardiovaskulární výkonnosti během dialýzy
- Zvýšením vápníku v dialyzačním roztoku. Standardně užíváme koncentraci inizovaného Ca 1,25 mmol/L. U často opakující se hypotenze je vhodnější užívat vyšší koncentrace např. 1,50–1,75 mmol/L ionizovaného Calcia. To má své úskalí, zvýšené hladiny vápníku v dialyzačním roztoku mohou vyústit v hyperkalcémie a následné ukládání přebytečného vápníků do cév a jejich následné poškození cév kalcifikacemi. Hypercalcemie vede také ke snížení kostního obratu vápníku – vedoucí až k rozvoji adynamické kostní nemoci.
- Korekce anémie např. zvýšením dávky erytropoetinu, nebo transfuzí krve, zlepší výkonnost srdce
- Midodrine – pomáhá hlavně u pacientů s autonomní neuropatií, brání náhlým poklesům tlaku.
- Karnitin – dlouhodobé podávání zlepší výživu srdečního svalu, zlepšuje výkonnost srdce a snižuje výskyt hypotenzní epizod a svalových křečí[zdroj?].
- U kardiaků je vhodné omezit jídlo během dialýzy, protože jídlo způsobí vyplavení velkého množství žaludeční šťávy. Jídlo vede k vasodilataci v oblasti zažívacího traktu, a tak přispět k poklesu systémového krevního tlaku
- Blokádou adenosinu. Adenosin je endogenní vasodilatátor a při vyšší hladině v krvi, může způsobit hypotenzi. Adenosin lze blokovat např. kofeinem, takže podávání kávy během dialýzy může snížit frekvenci hypotenzí.
- infuze vazopresinu (zatím výzkumně) by měla významně snížit výskyt symptomatických hypotenzí.
Při častém výskytu hypotenze je nejlepší zkombinovat několik přístupů, začít od těch nejjednodušších a postupně přidávat ty problematičtější a dražší.
Protože dialýza vyžaduje přístup do krevního oběhu, mohou se do těla dostat mikroby a způsobit sepsi, endokarditidu nebo osteomyelitidu. Velikost tohoto rizika závisí na druhu cévního přístupu a snižuje se důslednějším dodržováním protiinfekčních opatření. Také může dojít ke krvácení, riziko je opět úměrné druhu cévního přístupu.
Heparin je nejpoužívanějším antikoagulačním prostředkem (zabraňujícím srážení krve), je všeobecně dobře snášen a jeho účinek lze rychle zvrátit pomocí protaminsulfátu, alergie na něj je vzácná a projevuje se snížením množství krevních destiček. Pacienty s velkým rizikem krvácení lze dialyzovat i bez něj.
Cévní přístup
Existují tři základní způsoby: nitrožilní katetr, AV zkrat a umělohmotný graft, volí se podle časové tísně, zachovalosti žil apod. Pacient může mít více přístupů zároveň, běžně dokud není nový zkrat dostatečně rozvinutý je používán katetr.
Katetr


Katetr, nazývaný často centrální katetr nebo jen centrál je umělohmotná hadička rozdělená uvnitř na dvě souběžné žíly, na vyčnívajícím konci je rozvětvený do dvou přípojek, v těle zavedený do velké vnitřní žíly, obvykle do horní duté žíly přes krční žílu nebo do stehenní žíly přes tříslo. Z jedné přípojky katetru se krev odebírá, prochází dialyzačním přístrojem a druhou připojkou se vrací, bohužel průtok krve je téměř vždy menší než u dobře rozvinutého zkratu nebo graftu.
Netunelový katetr trčí z těla na místě vpichu a lze jej používat krátkodobě, obvykle kolem deseti dnů.
Tunelový katetr je delší, z místa vpichu je veden tunýlkem pod kůží a ústí o něco dál, nejčastěji míří vpich do krční žíly a vyústění je na hrudi, což je nenápadnější, pohodlnější a bezpečnější než netunelová hadička plandající vzhůru k uchu. Tunel funguje jako zábrana infekci, což obecně prodlužuje životnost katetru na střednědobou (týdny až měsíce), infekce katetru však zůstávají i nadále velkým problémem.
Kromě infekcí jsou problémem katetrů stenozy žil, katetr je v těle cizím předmětem, což může vyprovokovat silnou reakci žilní stěny: zajizvení nebo zúžení v místě žilního vpichu pak způsobuje městnání krve a může dojít k závažnému hromadění v oblastech, které mají být napíchnutou žilou odváděny, může také dojít až k obcházení této žíly a hlavně jejích přívodných žil jinudy, což způsobuje jejich pozdější nepoužitelnost pro zkrat nebo graft. Dlouhodobě dialyzovaní pacienti se tak mohou dostat do situace bez žilního přístupu, což má osudné následky.
Netunelový katetr je obvykle používán při nutnosti rychlé okamžité dialýzy.
Tunelový pro pacienty
- s akutním selháním ledvin u nichž se předpokládá navrácení funkce
- s neléčeným nově objeveným chronickým selháním ledvin do doby než se jim rozvine zkrat nebo graft
- u nichž nelze použít jiný přístup
Tunelový katetr bývá mezi pacienty oblíben protože připojování se obejde bez napichování a ruka zůstává volná, ovšem pro rizika s ním spojená je dlouhodobě používán jen v jinak neřešitelných případech.
AV zkrat

AV (arteriovenózní) zkrat je považován za nejlepší cévní přístup. Nazývá se též shunt (čti „šant“ — z angl. propojka, zkratka), píštěl, fistule, nebo anastomóza, v písemném projevu obvykle s akronymem AV. Při jeho vytvoření propojí cévní chirurg tepnu a žílu. Protože se tím obejdou periferní cévy a vlásečníce, krev protéká zkratem velmi rychle. Přiložením prstu na rozvinutý zkrat je zřetelně cítit víření, poslechem typický šum. Zkrat se obvykle šije na méně používané ruce buď na žíle na palci (tzv. snuffbox shunt), na předloktí (obvykle tzv. radiocefalický zkrat neboli Brescia-Cimino shunt propojující radiální tepnu s cefalickou žílou) nebo na lokti (tzv. brachiocefalický zkrat propojující brachiální tepnu s cefalickou žílou). Zkrat musí před prvním použitím průměrně 4–6 týdnů zrát, během zrání se žíla zvětší a její stěny zesílí, takže pak vydrží pravidelné napichování. Na začátku dialýzy jsou do něj zavedeny dvě jehly, jedna pro čerpání a druhá pro vracení krve.
Zkrat nezavádí do těla žádný cizí materiál, takže riziko infekce je malé, má vyšší průtok krve a menší výskyt trombóz. Komplikací není moc, nicméně zkratem protéká velmi mnoho krve, takže prokrvení ruky pod zkratem se může zhoršit, ve vážnějších případech ruka chladne, svíravě bolí a může dojít až k poškození tkání, řešením je zmenšení propojky na rozumnou míru. Z dlouhodobého hlediska může docházet ke vzniku aneurysmat, což jsou zeslabení žilní stěny způsobená opakovaným napichováním. Lze je chirurgicky opravit, nicméně i tak mohou životnost zkratu zkrátit. Lze jim předcházet promyšleným napichováním na více míst cyklickým způsobem, jinou metodou je napichování tupější jehlou do přesně jednoho a téhož místa, do dvou až tří tzv. „knoflíkových dírek“.
AV Graft

AV (arteriovenózní) graft podobně jako zkrat propojuje tepnu a žílu, propojka je však vyrobena buď z teflonu nebo je použita chemicky upravená sterilizovaná zvířecí céva. Použije se, když pacientův žilní systém neumožňuje vytvořit zkrat. Zraje rychleji než zkrat, zvláště novější grafty. Grafty jsou podstatně náchylnější ke vzniku zúženin, zejména v místě napojení na odvodnou žílu. Ve zúženém místě se mohou začít tvořit hrudky a trombózy. Jako každé cizí těleso uvnitř těla je náchylnější k infekcím. Graft může být dosti dlouhý a lze ho proto přišít na mnoha místech, dokonce i na stehně nebo na krku.
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu hemodialýza na Wikimedia Commons
Obrázky, zvuky či videa k tématu hemodialýza na Wikimedia Commons  Slovníkové heslo hemodialýza ve Wikislovníku
Slovníkové heslo hemodialýza ve Wikislovníku
Média použitá na této stránce
Temporal catheter for hemodialysis
AV fistule
Arteriovenózní graft