Hydroxyderiváty

Hydroxyderiváty (nebo také hydroxysloučeniny) jsou deriváty uhlovodíků, jejichž molekuly obsahují jednu nebo více charakteristických hydroxylových skupin -OH. Podle počtu -OH skupin se rozlišují na monofunkční, difunkční a polyfunkční hydroxyderiváty. Pokud je -OH skupina připojena na uhlíkový atom v uhlovodíkovém řetězci, nazývají se tyto hydroxyderiváty alkoholy. Pokud je -OH skupina připojena na uhlíkový atom benzenového jádra, jsou to fenoly.
Mezi hydroxyderiváty patří také hydroxyaldehydy (glyceraldehyd, salicylaldehyd), hydroxykyseliny (kyselina mléčná, kyselina salicylová) a sacharidy.
Dělení hydroxyderivátů
Podle typu uhlíkového řetězce
- Alkoholy, kde je -OH skupina vázána na uhlíkový atom alifatického řetězce (řetězec není vázán na aromatické jádro).
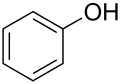
- Fenoly, kde je -OH skupina vázána na uhlíkový atom, který je součástí aromatického jádra.
- Alkohol
- Fenol
Podle počtu uhlíků vázaných na atom uhlík nesoucí -OH skupinu
- Primární alkoholy, kde atom uhlíku nesoucí -OH skupinu (tzv. primární uhlík) se váže na další 1 atom uhlíku
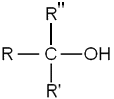
- Sekundární alkoholy, kde atom uhlíku nesoucí -OH skupinu (tzv. sekundární uhlík) se váže na další 2 atomy uhlíku
- Terciární alkoholy, kde atom uhlíku nesoucí -OH skupinu (tzv. terciární uhlík) se váže na další 3 atomy uhlíku
- Primární alkohol
- Sekundární alkohol
- Terciární alkohol
Podle počtu -OH skupin v molekule
- Jednosytné (monofunkční), obsahuje jednu -OH skupinu (například CH3CH2OH)
- Dvojsytné (difunkční), obsahuje dvě -OH skupiny (například OH-CH2-CH2-OH)
- Vícesytné (polyfunkční), obsahuje tři a více -OH skupin (například OH-CH2-CH(OH)-CH2-OH)
Příklady vlastností
- Bod varu roste s počtem -OH skupin vázaných v molekule hydroxyderivátu.
- Přítomnost skupin -OH má vliv na rozpustnost hydroxyderivátů. Nižší alkoholy (methanol, ethanol a propanol jsou s vodou neomezeně mísitelné, vyšší alkoholy jsou mísitelné omezeně a nejvyšší alkoholy se s vodou nemísí.
- Fenoly se ve vodě rozpouštějí poměrně málo.
- Vícesytné fenoly se rozpouštějí ve vodě lépe než jednosytné.
- Primární alkohol je nejvíce kyselý a terciární nejméně kyselý.
- Fenoly jsou více kyselé než alkoholy.
- Skupiny -OH hydroxyderivátů se podílejí na tvorbě vodíkových můstků.
- Hydroxysloučeniny jsou amfoterní látky (chovají se jako kyseliny i jako zásady).
Příklady hydroxyderivátů
- Methanol (metylalkohol) CH3OH, prudce jedovatá kapalina, která způsobuje poškození nebo ztrátu zraku, případně smrt. Smrtelná dávka je v rozmezí 10 – 100 ml. Používá se jako rozpouštědlo.
- Ethanol (etylalkohol, líh) CH3CH2OH, vyrábí se kvašením cukerných šťáv, využití při alkoholických nápojů, léčiv, v kosmetice apod.
- Ethylenglykol (1,2-ethandiol) HOCH2CH2OH, jedovatý, využití jako složka těžko mrznoucích směsí a surovina pro výrobu polyesterů.
- Glycerol (1,2,3-propantriol, glycerin), součást přírodních tuků a olejů, používá se do kosmetických přípravků
- Fenol, bílá krystalická látka, jedovatý a leptá pokožku, používal se k desinfekci, nyní k výrobě léčiv, barviv, výbušnin a plastů.
- Dvojsytné fenoly pyrokatechol, resorcinol, hydrochinon, tuhé, ve vodě rozpustné látky. Pyrokatechol a hydrochinon se používají jako vývojky v černobílé fotografii, resorcinol se používá pro výrobu barviv.
Reference
V tomto článku byl použit překlad textu z článku Pentapeptide repeat na anglické Wikipedii.
V tomto článku byl použit překlad textu z článku Alkohole na německé Wikipedii.
Média použitá na této stránce
3D model of the Hydroxyl group created from .pdb file.
Structure of phenol