Kapalinová chromatografie s hmotnostní spektrometrií

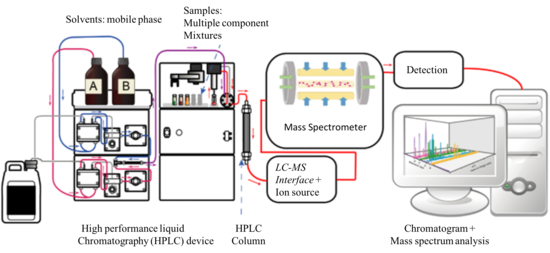
Kapalinová chromatografie s hmotnostní spektrometrií (LC-MS) je analytická metoda využívající k oddělení složek směsi kapalinový chromatograf; speciálním případem je využití vysokoúčinné kapalinové chromatografie (HPLC); a k jejich následné analýze hmotnostní spektrometrii. Kapalinový chromatograf odděluje jednotlivé složky směsi, zatímco hmotnostní spektrometr analyzuje jejich strukturu s vysokou specifitou a citlivostí. Tímto způsobem se analyzují biochemické, organické i anorganické látky, často ve vzorcích pocházejících ze životního prostředí nebo biologického původu. LC-MS tak lze využít v mnoha oblastech, jako jsou biotechnologie, zpracování potravin, výroba léčiv, agrochemie a kosmetika.[1][2]
Součástí aparatury pro LC-MS je zařízení, které přeměňuje látky oddělené pomocí LC na zdroje iontů pro MS.[2][3] Toto rozhraní umožňuje složkám vzorku přejít z mobilní fáze, kterou je stlačená kapalina, do hmotnostního spektrometru, ve kterém je tlak okolo 10−4 Pa; zároveň musí přenést co nejvyšší část analytů a co možná nejméně mobilní fáze a přitom nezměnit jejich chemické vlastnosti. Rovněž by nemělo působit na ionizátor či vakuum uvnitř hmotnostního spektrometru. Nejčastěji používaná LC/MS rozhraní jsou založeny na elektrosprejové ionizaci (ESI), chemické ionizaci za atmosférického tlaku (APCI) nebo fotoionizaci za atmosférického tlaku (APPI). Tato rozhraní se využívají od 90. let 20. století.[4][3]
Historie
Vývoj spojení chromatografie a hmotnostní spektrometrie začal v 50. letech 20. století. V roce 1952 byla představena plynová chromatografie s hmotnostní spektrometrií (GC-MS).[5] U plynové chromatografie procházejí analyty separačním sloupcem jako plyny a spojení s elektronovou nebo chemickou ionizací je technicky snazší. Z tohoto důvodu byl rozvoj GC-MS rychlejší a první soupravy pro LC-MS se objevily až v 70. letech.[3] Vývoj LC-MS trval déle než u GC-MS a přímo souvisel s vývojem vhodných rozhraní. V. L. Tal'roze se svými spolupracovníky zahájil vývoj LC-MS na začátku 70. let, kdy byly k propojení LC a MS použity kapiláry.[6][4] Jednalo se o první způsob spojení kapalinové chromatografie a hmotnostní spektrometrie. Rozhraní pro tuto metodu mělo stejnou kapacitu jako u GC-MS a použití soustavy bylo omezeno na analýzu těkavých analytů a látek s nízkou molární hmotností (pod 400 g/mol). V tomto rozhraní docházelo k odpařování mobilní fáze uvnitř kapiláry.
V několika následujících letech byly vyvinuty další varianty rozhraní. Bylo zjištěno, že pro analýzy složitějších směsí bude potřeba vyvinout plně automatizovanou soustavu pro LC-MS.[4]
Rozhraní s pohyblivým pásem
Rozhraní s pohyblivým pásem byla vyvinuta v roce 1977. Tato rozhraní se skládají z nekonečného pohyblivého pásu, na který přichází mobilní fáze z chromatografu. Na pásu se mírným zahříváním odpařuje rozpouštědlo a páry se převádějí do dvou vakuových komor. Po odstranění kapalné fáze se analyty zachycují na pásu a jsou přesunuty do hmotnostního spektrometru, kde jsou analyzovány. Tato rozhraní byla používána v letech 1978 až 1990, a to díky tomu, že umožňovala propojení LC s MS za použití jak elektronové, tak i chemické ionizace nebo ionizace rychlými atomy (FAB). Propojují se jimi LC sloupce se sektorovými a kvadrupólovými analyzátory. Takovéto spektrometry lze použít na analýzu léčiv, pesticidů, steroidů, alkaloidů a polycyklických aromatických uhlovodíků. Rozhraní s pohyblivým pásem se již nepoužívají, protože jsou mechanicky složitá a obtížná je i výměna pásu za nový. Od roku 1988 byla nahrazena jinými druhy.[4][7]
Rozhraní s přímým vstupem kapaliny
Rozhraní s přímým vstupem kapaliny byla zavedena v roce 1980. U těchto rozhraní dochází k odpařování kapaliny z kapiláry a k oddělení složek kapalné fáze se používá rozprašovač. Následně malá membrána vytváří proud kapek, které jsou vysoušeny v desolvatační komoře. Následně pomocí mikroborové kapiláry přejde takto upravená kapalná fáze do hmotnostního spektrometru. Analyty jsou ionizovány pomocí rozpouštědlem řízené chemické ionizace, přičemž rozpouštědla zde fungují jako reaktivní plyny.
Při použití těchto rozhraní je nutné oddělit proud vstupující do spektrometru od proudu přicházejícího z chromatografu, protože bez narušení vakua ve spektrometru je možné zanalyzovat jen malé množství vzorku (10 až 50 μl/min z 1 ml/min). Jedním z hlavních nedostatků je časté ucpávání otvorů membrány. Rozhraní s přímým vstupem kapaliny se používala v letech 1982 až 1985 při analýzách pesticidů, kortikosteroidů, erythromycinu, vitaminu B12 a metabolitů v moči koní. Byla nahrazena termosprejovými rozhraními, díky kterým došlo k odstranění potíží s omezeným průtokem vzorku i s ucpáváním membrány.[2][4]
Termosprejová rozhraní
Termosprejová (TSP) rozhraní byla vyvinuta v roce 1983. S jejich použitím bylo možné dosáhnout průtoků vzorku okolo 1 ml/min a nebylo potřeba rozdělit vzorek na dvě části. Skládají se ze zahřívané sondy, desolvatační komory a iontoměničového sběrače. Vzorek prochází sondou, kde vytváří proud páry a drobných kapek, jež za nízkého tlaku procházejí desolvatační komorou. K ionizaci dochází přímým odpařováním nebo interakcemi iontů s molekulami, které vyvolává rozpouštědlo. U těchto rozhraní může průtok vzorku z chromatografu dosáhnout až 2 ml/min a tak jsou vhodná například při HPLC na nepolárních adsorbentech. TSP systémy jsou jak rozhraními, tak i rozpouštědlem řízenými zdroji iontů. S postupem času došlo u termosprejových rozhraní k mechanickým zjednodušením a tato rozhraní se stala často používanými ve farmacii například při analýze léčiv, metabolitů, nukleosidů, peptidů a pesticidů. TSP rozhraní byla významným krokem k častějšímu používání LC-MS a používala se do 90. let 20. století. kdy byla nahrazena rozhraními využívajícími ionizaci a atmosférického tlaku.[2][3][7]
FAB rozhraní
Rozhraní využívající bombardování rychlými atomy (FAB) byla vyvinuta v 80. letech 20. století.[7] Dělí se na dva druhy: fritová FAB rozhraní, u kterých se k propojení vyžívá porézní fritová sonda, a FAB s nepřetržitým tokem (CF-FAB), kde k tomuto účelu slouží hrot sondy. CF-FAB se používá častěji; hodí se k analýzám netěkavých a nestabilních látek. Kapalina z chromatografu prochází fritou nebo CF-FAB, na jejímž hrotu vytváří stejnorodou vrstvu. Kapalina je následně ostřelována svazky iontů nebo vysokoenergetickými (tedy rychlými) atomy. Při stabilním průběhu může být průtok vzorku jen 1 až 15 μl a použít lze jen mikroborové nebo kapilární chromatografické sloupce. Analyty zkoumané za použití těchto rozhraní musejí být smíchány s matricí (například glycerolem) před vstříknutím do chromatografického sloupce nebo po projití skrz něj. FAB rozhraní se používala při analýzách peptidů, ovšem v roce 1988 byla nahrazena elektrosprejovými rozhraními.1988.[2][4]
Chromatograf
Kapalinová chromatografie se používá k oddělování složek směsi z kapalných mobilních fází. Dělí se na pět druhů, kterými jsou adsorpční, rozdělovací, iontoměničová, gelová a afinitní chromatografie. Nejčastěji se provádí rozdělovací chromatografie s obrácenou fází, která umožňuje použití nepolární (hydrofobní) stacionární fáze a polární mobilní fáze. Mobilní fází je nejčastěji směs vody a dalších polárních rozpouštědel (například methanolu, isopropanolu nebo acetonitrilu), stacionární fáze se vytváří napojováním alkylových skupin s dlouhými řetězci (například n-oktadecylu) na povrch nepravidelných nebo kulových částeček silikagelu o průměru 5 μm.[2]
Při HPLC se obvykle 20 μl zkoumaného vzorku do proudu mobilní fáze poháněné vysokotlakou pumpou. Analyty v mobilní fázi interagují se stacionární fází. Složky směsí se oddělují na základě rozdílné afinity k mobilní a stacionární fázi. Oddělování spočívá v opakované sorpci a desorpci.[4] Kapalný roztok je poháněn vysokým tlakem (okolo 40 MPa) do sloupce obsahujícího stacionární fázi; vysoký tlak je potřeba k dosažení stálého toku mobilní fáze a opakovatelnosti experimentů. Podle rozdílného zachycování na stacionární fázi procházejí jednotlivé složky vzorku chromatografickou kolonou v rozdílných časech.[7] Chromatografická kolona je nejdůležitější součástí systému a je konstruována tak, aby byla odolná vůči kapalinám o vysokém tlaku. Obvyklá délka chromatografických kolon je 100 až 300 mm s vnějším průměrem 6,4 mm a vnitřním průměrem 3,0 až 4,6 mm. U LC-MS bývá délka menší (30 až 50 mm) a průměr částic stacionární fáze se pohybuje od 3 do 5 μm. Oproti běžným modelům existují také sloupce pro kapalnou chromatografii, které jsou užší a lze tak s nimi dosahovat účinnějšího oddělování analytů i při použití nižších průtoků, než je obvyklá hodnota 1 ml/min.[4] Za účelem ještě lepší citlivosti a rozlišení je možné místo HPLC provést UPLC, při které se používají sloupce s menšími částečkami stacionární fáze (s průměrem kolem 1,7 μm) a vyšší tlaky mobilní fáze (40 až 100 MPa).[2]
Hmotnostní spektrometr
Ve hmotnostní spektrometrii se k analýze využívá poměr hmotnost/náboj (m/z) nabitých částic (iontů). Existuje mnoho různých druhů hmotnostních spektrometrů; všechny však k oddělování iontů vytvořených z analytů a k určení jejich m/z využívají elektrické nebo magnetické pole.[8] Součástmi spektrometru jsou zdroj iontů, hmotnostní analyzátor, detektor a datové a vakuové systémy. Zdroj iontů se nachází v místě, kde do spektrometru přechází vzorek z chromatografu a dochází zde k jejich ionizaci, což může být zajišťováno například svazky elektronů nebo ultrafialovým zářením. Při elektrosprejové ionizaci zdroj iontů přesouvá již vzniklé ionty z roztoku do plynné fáze. Zdroj iontů přeměňuje neutrální molekuly na ionty v plynné fázi, které následně přecházejí do hmotnostního analyzátoru. V analyzátoru se ionty pomocí elektromagnetického pole rozdělují podle hmotností, detektor poté měří intenzitu proudu iontů a podle toho určuje jejich počet. Údaje potřebné k získání použitelného spektra se zpracovávají počítači.
Hmotnostní spektrum lze použít k určení molární hmotnosti analytů, jejich prvkového a izotopového složení, nebo nebo struktury zkoumaných molekul.[2] Analýzu hmotnostním spektrometrem je třeba provádět za velmi nízkých tlaků (10−2 až 10−6 Pa); k rozvoji hmotnostní spektrometrie tak bylo nutné vyvinout soustavy, které převádějí vzorek o vysokém tlaku do prostředí s nízkým tlakem, které je potřeba k analyzování peptidů a dalších organických látek.[9] Hmotnostní spektrometrie je běžně používána v laboratořích zkoumajících fyzikální, chemické i biologické vlastnosti mnoha různých sloučenin.
Použití

Spojení LC a MS se používá často, protože kapalinovou chromatografií lze rozdělit složité směsi přírodních i jiných látek (jako jsou například tělní tekutiny a léčiva), u kterých má být zjištěno podrobné složení. LC má využití při analýze stopových množství těkavých výbušnin.[10] HPLC-MS je široce používanou analytickou metodou například v proteomice[11] , farmaceutických laboratořích[3][2][12] a při analýze potravin, pesticidů[13] a rostlinných fenolů.[4]
Farmakokinetika
LC-MS se používá při bioanalýze, obzvláště při zkoumání farmakokinetiky léčiv. Farmakokinetické studie slouží k určení rychlosti odstraňování léčiv a jejich metabolitů z orgánů a z jaterní krve. Hmotnostní spektrometry se zde využívají díky krátké době trvání analýzy, vysoké citlivosti a specifičnosti oproti ultrafialovým detektorům, které také bývají propojovány s HPLC. Je možné je zapojit do tandemové MS-MS, při níž může detektor z fragmentů oddělovat vybrané ionty. Pokud nedochází k nežádoucím vlivům, tak je možné analýzu provést poměrně rychle.[14]
Proteomika a metabolomika

LC-MS má využití v metabolomice [15] k identifikaci složek složitých směsí. Obvykle se přitom pomocí močoviny bílkoviny zdenaturují, následně rozloží trypsinem a nakonec se pozmění cysteinové zbytky jodacetamidem. Poté lze použít LC-MS i k určení molekulových hmotností peptidů nebo LC-MS/MS ke zjištění posloupnosti aminokyselin.[16] LC-MS je nejčastěji používaná metoda analýzy komplexních vzorků, v nichž se mohou vyskytovat peptidy s podobnými molekulovými hmotnostmi, které nelze rozlišit ani pomocí vysoce citlivé hmotnostní spektrometrie. Biologické vzorky, jako je lidské sérum, lze analyzovat moderními LC-MS soustavami, které lze použít k identifikaci více než 1000 bílkovin; takovéhoto rozlišení lze však dosáhnout pouze pokud byly složky vzorku předtím rozděleny pomocí SDS-PAGE nebo HPLC-SCX.[14]. LC-MS/MS je také možné použít k hledání peptidových biomarkerů; příkladem může být objev biomarkerů čtyř bakterií napadajících dýchací soustavu (Staphylococcus aureus, Moraxella catarrhalis; Haemophilus influenzae a Streptococcus pneumoniae).[17]
LC-MS patří k nejvíce využívaným nástrojům při zkoumání metabolitů v tělních tekutinách[18] a sekundárních metabolitů u rostlin.[19] Soustavy s hmotnostní spektrometrií mohou sloužit k získání množství podrobných údajů o sloučeninách obsažených v biologických vzorcích. LC-NMR je také metodou využívanou při výzkumu metabolismu rostlin, ovšem lze pomocí ní určit pouze několik nejběžnějších metabolitů. Používání LC-MS rozšířilo možnosti výzkumu metabolismu rostlin, když umožnila studium procesů na molekulární úrovni s ohledem k prostředí.[20] První využití kapalinové chromatografie s hmotnostní spektrometrií k analýze rostlinného metabolismu spočívalo v detekci vysoce polárních metabolitů, oligosacharidů, aminokyselin, aminosacharidů a nukleotidů z floému tykve velkoplodé.[21] Dalším příkladem využití této metody je separace a analýza glukózy sacharózy, rafinózy, stachyózy a verbaskosidů z listů huseníčku rolního.[22]
Vývoj léčiv
LC-MS se často využívá při vývoji léčiv, umožňuje rychlé určení molární hmotnosti a struktury látek. Tyto vlastnosti dovolují urychlit přípravu, testování a ověřování různých potenciálně využitelných sloučenin. LC-MS se při vývoji léčiv používá v podobě vysoce automatizovaných metod používaných ke zkoumání peptidů, glykoproteinů a lipidů, identifikaci metabolitů a nečistot, kvantitativní bioanalýze a kontrole kvality.[23]
Nejběžnější aplikační použití kapalinové chromatografie s hmotnostní spektrometrií v této oblasti zahrnuje využití několika výše popsaných technik.
- Aplikační využití LC/MS na bází jednoduchých kvadrupólů především v rutinních jednoduchých analýzách [24]
- Aplikační využití LC/QQQ na bázi trojitých kvadrupólů v případě potřeby cilitvých stopových analýz např. nečistot v léčivech [25]
- Aplikační využití LC/HRMS na bází hmotnostních spektrometrů s vysokým rozlišením v případě potřeby identifikace, strukturní analýzy a především oblasti vývoje a analýz moderních biofarmaceutických léčiv [26]
Odkazy
Související články
- Plynová chromatografie s hmotnostní spektrometrií
- Kapilární elektroforéza s hmotnostní spektrometrií
- Spektrometrie iontové pohyblivosti s hmotnostní spektrometrií
Reference
V tomto článku byl použit překlad textu z článku Liquid chromatography–mass spectrometry na anglické Wikipedii.
- ↑ Patrick Chaimbault. Recent Advances in Redox Active Plant and Microbial Products. Příprava vydání Claus Jacob, Gilbert Kirsch, Alan Slusarenko, Paul G. Winyard, Torsten Burkholz. [s.l.]: Springer Netherlands, 2014-01-01. ISBN 9789401789523. doi:10.1007/978-94-017-8953-0_3. Kapitola The Modern Art of Identification of Natural Substances in Whole Plants, s. 31–94.
- ↑ a b c d e f g h i Chhabil Dass. Fundamentals of Contemporary Mass Spectrometry. [s.l.]: John Wiley & Sons, Inc., 2007-01-01. ISBN 9780470118498. doi:10.1002/9780470118498.ch5. Kapitola Hyphenated Separation Techniques, s. 151–194.
- ↑ a b c d e James J. Pitt. Principles and Applications of Liquid Chromatography-Mass Spectrometry in Clinical Biochemistry. The Clinical Biochemist Reviews. 2017-03-12, s. 19–34. ISSN 0159-8090. PMID 19224008.
- ↑ a b c d e f g h i Wilfried M. A. Niessen. Liquid Chromatography-Mass Spectrometry, Third Edition. Boca Raton: CRC Taylor & Francis, 2006. Dostupné online. ISBN 9780824740825. S. 50–90.
- ↑ A. T. James; A. J. P. Martin. Gas-liquid partition chromatography: the separation and micro-estimation of volatile fatty acids from formic acid to dodecanoic acid. Biochemical Journal. 1952-03-01, s. 679–690. ISSN 0264-6021. doi:10.1042/bj0500679. PMID 14934673.
- ↑ V. L. Tal'roze; T. G. Gorodetskii; N. B. Zolotoy; G. V. Karpov; V. E. Skurat; V. Ya. Maslennikova. Gas-liquid partition chromatography: the separation and micro-estimation of volatile fatty acids from formic acid to dodecanoic acid. Adv. Mass Spectrom. 1978, s. 858.
- ↑ a b c d Robert E. Ardrey. Liquid Chromatography – Mass Spectrometry: An Introduction. Boca Raton: John Wiley & Sons, Ltd, 2003-01-01. Dostupné online. ISBN 9780470867297. doi:10.1002/0470867299.ch1. Kapitola Introduction, s. 1–5.
- ↑ Gordon Roberts. Encyclopedia of Biophysics - Springer. [s.l.]: [s.n.], 2013. ISBN 978-3-642-16711-9. doi:10.1007/978-3-642-16712-6.
- ↑ Thomas R. Sharp. Drug Metabolism Handbook. [s.l.]: [s.n.], 2009-01-01. Dostupné online. ISBN 9780470439265. doi:10.1002/9780470439265.ch8. Kapitola Mass Spectrometry, s. 167–227.
- ↑ Leo Widmer; Stuart Watson; Konrad Schlatter; Andrew Crowson. Development of an LC/MS method for the trace analysis of triacetone triperoxide (TATP). The Analyst. 2002, s. 1627–1632. ISSN 0003-2654. doi:10.1039/b208350g. Bibcode 2002Ana...127.1627W.
- ↑ Aplikace z oblasti Proteomika se zaměřením na LC/MS. lcms.cz [online]. [cit. 2023-05-13]. Dostupné online.
- ↑ Aplikace z oblasti Farmaceutická analýza se zaměřením na LC/MS. lcms.cz [online]. [cit. 2023-05-13]. Dostupné online.
- ↑ Aplikace se zaměřením na LC/MS. lcms.cz [online]. [cit. 2023-05-13]. Dostupné online.
- ↑ a b P. Sudhakar; P. Latha; P. V. Reddy. Phenotyping Crop Plants for Physiological and Biochemical Traits. [s.l.]: Academic Press, 2016-04-05. ISBN 9780470439265, ISBN 9780128041109.
- ↑ Aplikace z oblasti Metabolomika se zaměřením na LC/MS. lcms.cz [online]. [cit. 2023-05-13]. Dostupné online.
- ↑ V. H. Wysocki; K. A. Resing; Q. Zhang; G. Cheng. Mass spectrometry of peptides and proteins. Methods. 2005, s. 211–222. doi:10.1016/j.ymeth.2004.08.013. PMID 15722218.
- ↑ KARLSSON, Roger; THORSELL, Annika; GOMILA, Margarita; SALVÀ-SERRA, Francisco; JAKOBSSON, Hedvig E.; GONZALES-SILES, Lucia; JAÉN-LUCHORO, Daniel. Discovery of Species-unique Peptide Biomarkers of Bacterial Pathogens by Tandem Mass Spectrometry-based Proteotyping. Molecular & Cellular Proteomics. 2020-03-01, s. 518–528. Dostupné online. ISSN 1535-9476. doi:10.1074/mcp.RA119.001667. PMID 31941798. (anglicky)
- ↑ Helen G. Gika; Georgios A. Theodoridis; Robert S. Plumb; Ian D. Wilson. Current practice of liquid chromatography–mass spectrometry in metabolomics and metabonomics. Journal of Pharmaceutical and Biomedical Analysis. 2014, s. 12–25. ISSN 0731-7085. doi:110.1016/j.jpba.2013.06.032. PMID 23916607.
- ↑ M. Stobiecki; A. Skirycz; L. Kerhoas; P. Kachlicki; D. Muth; J. Einhorn; B. Mueller-Roeber. Profiling of phenolic glycosidic conjugates in leaves of Arabidopsis thaliana using LC/MS. Metabolomics. 2006, s. 197–219. doi:10.1007/s11306-006-0031-5.
- ↑ Tiago F. Jorge; João A. Rodrigues; Camila Caldana; Romy Schmidt; Joost T. van Dongen; Jane Thomas-Oates; Carla António. Mass spectrometry-based plant metabolomics: Metabolite responses to abiotic stress. Mass Spectrometry Reviews. 2016-09-01, s. 620–649. ISSN 1098-2787. doi:10.1002/mas.21449. PMID 25589422. Bibcode 2016MSRv...35..620J.
- ↑ Vladimir V. Tolstikov; Oliver Fiehn. Analysis of Highly Polar Compounds of Plant Origin: Combination of Hydrophilic Interaction Chromatography and Electrospray Ion Trap Mass Spectrometry. Analytical Biochemistry. 2002, s. 298–307. Dostupné online. ISSN 1098-2787. doi:10.1006/abio.2001.5513. PMID 11814300.
- ↑ Carla Antonio; Tony Larson; Alison Gilday; Ian Graham; Ed Bergström; Jane Thomas-Oates. Hydrophilic interaction chromatography/electrospray mass spectrometry analysis of carbohydrate-related metabolites from Arabidopsis thaliana leaf tissue. Rapid Communications in Mass Spectrometry. 2008, s. 1399–1407. doi:10.1002/rcm.3519. PMID 18384194. Bibcode 2008RCMS...22.1399A.
- ↑ Mike S. Lee; Edward H. Kerns. LC/MS applications in drug development. Mass Spectrometry Reviews. 1999, s. 187–279. doi:10.1002/(SICI)1098-2787(1999)18:3/4<187::AID-MAS2>3.0.CO;2-K. PMID 10568041. Bibcode 1999MSRv...18..187L.
- ↑ Aplikace z oblasti Farmaceutická analýza se zaměřením na LC/MS, LC/SQ. lcms.cz [online]. [cit. 2023-05-13]. Dostupné online.
- ↑ Aplikace z oblasti Farmaceutická analýza se zaměřením na LC/MS, LC/QQQ. lcms.cz [online]. [cit. 2023-05-13]. Dostupné online.
- ↑ Aplikace z oblasti Farmaceutická analýza se zaměřením na LC/HRMS, LC/MS. lcms.cz [online]. [cit. 2023-05-13]. Dostupné online.
Média použitá na této stránce
Autor: Kermit Murray, Licence: CC BY-SA 4.0
Bruker Amazon Speed ETD ion trap mass spectrometer (left) and Dionex Ultimate 3000 high performance liquid chromatography system (right), comprising a LC MS/MS system.
Autor: Sarka Na kopci, Licence: CC BY-SA 4.0
Liquid chromatograph with mass spectrometer, used in particular for the determination of pesticide residues in foodstuffs, in CAFIA laboratory, Czech Republic
Autor: Sarka Na kopci, Licence: CC BY-SA 4.0
Liquid chromatograph with a mass spectrometer operating on the principle of flight time in combination with a quadrupole analyzer (qTOF). It affects the measurement in the so-called high resolution and serves mainly for the so-called non-target analysis of biologically active substances (eg unauthorized drugs and plant toxins) in food, in CAFIA laboratory, Czech Republic.
Autor: Cwszot | Dagui1929 | CasJu | YassineMrabet, Licence: CC0
Simple functional diagram of an LCMS system with increased clarity



