Karbamát
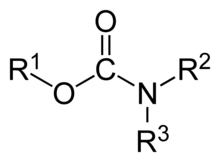
Karbamáty jsou organické sloučeniny odvozené od kyseliny karbamové (NH2COOH). Karbamátová skupina, kyseliny a estery jsou funkční skupiny, které jsou strukturálně vzájemně příbuzné a často lze mezi nimi provádět vzájemné konverze. Karbamátové estery se označují také jako urethany (či uretany).
Syntéza
Karbamové kyseliny se odvozují od aminů:
- R2NH + CO2 → R2NCO2H
Kyselina karbamová je zhruba stejně kyselá jako kyselina octová. Ionizace protonu poskytuje karbamátový aniont, konjugovanou zásadu kyseliny karbamové:
- R2NCO2H → R2NCO2− + H+
Karbamáty vznikají také hydrolýzou chlorformamidů:
- R2NC(O)Cl + H2O → R2NCO2H + HCl
Karbamáty mohou vznikat při Curtiově přesmyku, kdy vznikající isokyanatany reagují s alkoholem:
- RNCO + R'OH → RNHCO2R'
Výskyt a použití
Byť se většina tohoto článku zabývá organickými karbamáty, vyrábí se také velké množství anorganické soli karbamátu amonného jakožto meziprodukt při výrobě močoviny z amoniaku a oxidu uhličitého.
Karbamáty v biochemii
N-terminální aminoskupiny valinových zbytků v α- a β-řetězcích deoxyhemoglobinu jsou přítomny jako karbamáty. Pomáhají stabilizovat bílkovinu, když se z ní stává deoxyhemoglobin a zvyšuje pravděpodobnost uvolnění zbývajících kyslíkových molekul z vazby na bílkovinu. Vliv těchto karbamátů na afinitu hemoglobinu k O2 nesmí být spojován s efektem poklesu kyselosti deoxyhemoglobinu, který se nazývá Bohrův efekt.
ε-aminoskupiny lyzinových zbytků v ureáze a fosfortriesteráze taktéž využívají karbamát. Tento karbamát odvozený od aminoimidazolu je mezproduktem v biosyntéze inosinu. Z karboxyfosfátu vzniká místo CO2 karbamoylfosfát.[1]
Výrobky z karbamátových sloučenin
Karbamátové insekticidy
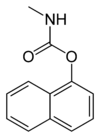
Takzvané karbamátové insekticidy využívají funkční skupiny karbamátových esterů. Patří mezi ně například aldikarb, karbofuran, fenoxykarb, karbaryl, ethionokarb a fenobukarb. Tyto insekticidy usmrcují hmyz reverzibilní inaktivací enzymu acetylcholinesterázy. Organofosfátové pesticidy také inaktivují tento enzym, avšak ireverzibilně, proto způsobují mnohem vážnější cholinergní otravu.[2] Repelent icaridin je substituovaný karbamát.
Polyurethany
Polyurethany (též polyuretany) obsahují ve své struktuře více karbamátových skupin. „Urethan“ není jednotkou (monomerem) polyurethanů. Tyto polymery mohou mít různorodé vlastnosti a jsou komerčně dostupné ve formě pěny (pěnový polyurethan), elastomerů i tuhých látek. Vznikají reakcí alkoholů s isokyanatany:
- RN=C=O + R'OH → RNHC(O)OR'
Typicky se využívají diisokyanatany, např. toluen-diisokyanatan, a dioly, např. bisfenol A.
Lékařství
Urethan čili ethylkarbamát se vyráběl ve Spojených státech jako protinádorové léčivo a pro jiné lékařské účely. Byl však shledán toxickým a téměř neúčinným.[3] Občas se používá ve veterinárním lékařství.
Některé karbamáty se využívají ve farmakoterapii, například inhibitory cholinesterázy neostigmin a rivastigmin, jejichž chemická struktura je založena na přírodním alkaloidu fysostigminu. Mezi další příklady patří meprobamat a jeho deriváty, např. karizoprodol, felbamat a tybamat, třída anxiolytik a myorelaxancií široce používaných v 60. letech 20. století před rozmachem benzodiazepinů; někdy se používají i dnes.
Reference
V tomto článku byl použit překlad textu z článku Carbamate na anglické Wikipedii.
- ↑ Bartoschek, S.; Vorholt, J. A.; Thauer, R. K.; Geierstanger, B. H. and Griesinger, C., "N-Carboxymethanofuran (carbamate) formation from methanofuran and CO2 in methanogenic archaea : Thermodynamics and kinetics of the spontaneous reaction", Eur. J. Biochem., 2001, 267, 3130-3138.
- ↑ Robert L. Metcalf “Insect Control” in Ullmann’s Encyclopedia of Industrial Chemistry” Wiley-VCH, Weinheim, 2002. DOI:10.1002/14356007.a14_263
- ↑ Holland JR, Hosley H, Scharlau C, Carbone PP, Frei E 3rd, Brindley CO, Hall TC, Shnider BI, Gold GL, Lasagna L, Owens AH Jr, Miller SP. A controlled trial of urethane treatment in multiple myeloma. Blood. 1 March 1966, roč. 27, čís. 3, s. 328–42. Dostupné v archivu pořízeném dne 2007-03-28. ISSN 0006-4971. PMID 5933438.
Související články
- Methyl-karbamát
- Ethyl-karbamát
- Polyuretan
Externí odkazy
 Obrázky, zvuky či videa k tématu Karbamát na Wikimedia Commons
Obrázky, zvuky či videa k tématu Karbamát na Wikimedia Commons
Média použitá na této stránce
Skeletal formula of carbaryl, close to the conformation found in the solid state. X-ray crystallographic data from Christine Sandoza, Pierre Lescab, Jean-François Narbonnea and Alain Carpy (2000). "Molecular Characteristics of Carbaryl, a CYP1A1 Gene Inducer". Archives of Biochemistry and Biophysics 373: 275-280. DOI:10.1006/abbi.1999.1515.
Structural formula of the carbamate group, ROCONR2.

