Karbaryl
| Karbaryl | |
|---|---|
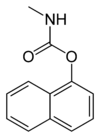 Strukturní vzorec karbarylu | |
 Model molekuly karbarylu | |
| Obecné | |
| Systematický název | 1-naftylmethylkarbamát |
| Triviální název | karbaryl |
| Ostatní názvy | carbaryl |
| Anglický název | Carbaryl |
| Německý název | Carbaryl |
| Sumární vzorec | C12H11NO2 |
| Vzhled | bezbarvé krystaly |
| Identifikace | |
| Registrační číslo CAS | 63-25-2 |
| EC-no (EINECS/ELINCS/NLP) | 200-555-0 |
| Indexové číslo | 006-011-00-7 |
| UN kód | 2757 |
| SMILES | O=C(Oc2cccc1ccccc12)NC |
| InChI | 1S/C12H11NO2/c1-13-12(14)15-11-8-4-6-9-5-2-3-7-10(9)11/h2-8H,1H3,(H,13,14) |
| Číslo RTECS | FC5950000 |
| Vlastnosti | |
| Molární hmotnost | 201,22 g/mol |
| Teplota tání | 142 °C |
| Hustota | 1,2 g/cm³ |
| Rozpustnost ve vodě | velmi nízká |
| Bezpečnost | |
| [1] Varování[1] | |
| H-věty | H351 H332 H302 H400 |
| R-věty | R20/22 R40 R50 |
| S-věty | (S2) S36/37 S46 S61 |
| Teplota vzplanutí | 193–202 °C |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Karbaryl (též carbaryl či 1-naftylmethylkarbamát) je karbamát používaný především jako insekticid. Tato bílá krystalická látka se prodává například pod značkou Sevin (ochranná známka firmy Bayer). Karbaryl objevila a na trh uvedla společnost Union Carbide v roce 1958 (roku 2002 firma Bayer koupila firmu Aventis CropScience, pod kterou patřila i sekce pesticidů Union Carbide). Karbaryl je stále třetí nejpoužívanější insekticid v USA pro oblast zahrádkářství, zemědělství a lesnictví. Pro ochranu zemědělských plodin se v USA v roce 1976 použilo zhruba 11 tisíc tun karbarylu.[2]
Výroba
Karbaryl se vyrábí reakcí methylisokyanátu (3) s 1-naftolem (4).[3]
Alternativně lze 1-naftol (1) nejprve převést na chlorformiát(3), který poté reaguje s methylaminem na požadovaný produkt (4):[3]
První z procesů byl provozován v Bhópálu, kde nakonec došlo k velmi vážné nehodě. V porovnání s tím se v druhé syntéze využívají sice stejná reagencia, ovšem v odlišné sekvenci. Tato syntéza neobsahuje přípravu methylisokynátu; porovnání se často používá jako případová studie zelené chemie. Ovšem druhý postup stejně používá fosgen, který je toxický a reaguje s vodou, a methylamin, což je toxický a hořlavý plyn.
Biochemie
Karbamátové insekticidy jsou reverzibilními inhibitory enzymu acetylcholinesterázy. Napodobují acetylcholin, ovšem nepodléhají konečné hydrolýze. Takto zasahují do nervového systému a způsobují smrt.
Použití
Vývoj karbamátových insekticidů je označován jako velký přelom v oblasti pesticidů. Karbamáty nejsou perzistentní jako chlorované pesticidy. Přestože je karbaryl toxický pro hmyz, u obratlovců je velmi rychle detoxifikován a eliminován. Neukládá se v tucích ani není vylučován do mateřského mléka. Proto je u potravinářských plodin preferován, přinejmenším v USA.[2] Je aktivní složkou šamponu Carylderm proti vším. V Česku se prodával například přípravek Diffusil H Forte obsahující karbaryl a určený pro hubení vši dětské a muňky na lidském těle.[4]. Byl ale nahrazen přípravkem Diffusil H Forte B85, který již karbaryl ani jiný insekticid neobsahuje.[5].
Rizika
Karbaryl usmrcuje jak cílový škodlivý hmyz (např. komáry přenášející malárii), tak i hmyz užitečný (např. včelu medonosnou) a korýše.
Přestože je karbaryl schválen v USA pro použití na více než 100 různých plodin, v některých státech je zakázán, například ve Spojeném království, Rakousku, Dánsku, Švédsku, Německu a Angole.[6]
Bezpečnost
Karbaryl je inhibitor cholinesterázy a je pro člověka toxický. Americká agentura EPA ho klasifikuje jako pravděpodobný lidský karcinogen.[7]
Orální LD50:
Reference
V tomto článku byl použit překlad textu z článku Carbaryl na anglické Wikipedii.
- ↑ a b Carbaryl. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ a b Robert L. Metcalf “Insect Control” in Ullmann’s Encyclopedia of Industrial Chemistry” Wiley-VCH, Weinheim, 2002. DOI:10.1002/14356007.a14_263
- ↑ a b Thomas A. Unger. Pesticide synthesis handbook. [s.l.]: William Andrew, 1996. Dostupné online. ISBN 0815514018. S. 67–68.
- ↑ Diffusil H Forte. www.biolit.cz [online]. [cit. 2013-12-13]. Dostupné v archivu pořízeném dne 2013-12-15.
- ↑ Diffusil H Forte B85. www.biolit.cz [online]. [cit. 2013-12-13]. Dostupné v archivu pořízeném dne 2013-12-15.
- ↑ Carbaryl Insecticide Hazard Data. www.grandcountywater.com [online]. [cit. 2010-07-31]. Dostupné v archivu pořízeném dne 2010-05-11.
- ↑ Interim Reregistration Eligibility Decision for Carbaryl, U.S. EPA, June 2003.
Externí odkazy
 Obrázky, zvuky či videa k tématu Karbaryl na Wikimedia Commons
Obrázky, zvuky či videa k tématu Karbaryl na Wikimedia Commons - (anglicky) Carbaryl Technical Fact Sheet - National Pesticide Information Center
- (anglicky) Carbaryl General Fact Sheet - National Pesticide Information Center
- (anglicky) Carbaryl Pesticide Information Profile - Extension Toxicology Network
- (anglicky) Cholinesterase Inhibition - Extension Toxicology Network
- (anglicky) EPA info
- (anglicky) EPA factsheet
- (anglicky) IPCS (WHO) Health and Safety Guide
- (anglicky) Environmental Health Criteria - WHO
- (anglicky) Exclusive Chemistry Ltd - routes of Sevin synthesis
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
Alternative synthesis of carbaryl, which bypasses methyl isocyanate. Adapted from Thomas A. Unger (1996) Pesticide synthesis handbook (Google Books excerpt), William Andrew, pp. 67−68 ISBN: 0815514018.
Skeletal formula of carbaryl, close to the conformation found in the solid state. X-ray crystallographic data from Christine Sandoza, Pierre Lescab, Jean-François Narbonnea and Alain Carpy (2000). "Molecular Characteristics of Carbaryl, a CYP1A1 Gene Inducer". Archives of Biochemistry and Biophysics 373: 275-280. DOI:10.1006/abbi.1999.1515.
Ball-and-stick model of the carbaryl molecule, as found in the solid state. X-ray crystallographic data from Christine Sandoza, Pierre Lescab, Jean-François Narbonnea and Alain Carpy (2000). "Molecular Characteristics of Carbaryl, a CYP1A1 Gene Inducer". Archives of Biochemistry and Biophysics 373: 275-280. DOI:10.1006/abbi.1999.1515.
Synthesis of carbaryl, which uses methyl isocyanate. Adapted from Thomas A. Unger (1996) Pesticide synthesis handbook (Google Books excerpt), William Andrew, pp. 67−68 ISBN: 0815514018.











