Karbonyly kovů


Karbonyly kovů jsou komplexní sloučeniny přechodných kovů a oxidu uhelnatého. Mají využití v organické syntéze a jako katalyzátory či jejich prekurzory v homogenní katalýze, například při hydroformylačních reakcích. V Mondově procesu se používá tetrakarbonyl niklu na přečišťování niklu. V organokovové chemii se z nich připravují další organokovové komplexy.
Karbonyly kovů jsou toxické při styku s kůží, vdechnutí nebo požití, protože karbonylují hemoglobin na karboxyhemoglobin, který brání přenosu kyslíku.[1]
Názvosloví
Názvy karbonylů kovů se vytvářejí podle náboje komplexu, počtu a druhu centrálních atomů a počtu a druhu ligandů a jejich vazeb. Karbonyly mohou tvořit neutrální komplexy, mohou být kladně nabité a vytvářet tak karbonylové kationty. a také záporně nabité karbonyláty. Oxid uhelnatý v nich může být navázán na jeden atom kovu nebo vytvářet můstek mezi několika kovovými atomy. Jsou také známy jak homoleptické karbonyly, obsahující pouze CO ligandy, například tetrakarbonyl niklu (Ni(CO)4), tak i heteroleptické, ve kterých se vyskytuje více různých ligandů.
Jednojaderné karbonyly mají pouze jeden centrální atom kovu. Neutrální homoleptické jednojaderné komplexy vytváří s výjimkou hexakarbonylu vanadu pouze prvky se sudými protonovými čísly, jako jsou chrom, železo a nikl. Vícejaderné karbonyly se tvoří od prvků, které mají lichá protonová čísla nebo vytvářejí kovové vazby.[2] Komplexy obsahující atomy různých kovů, ale pouze jeden druh ligandu, se označují jako isoleptické.[2]
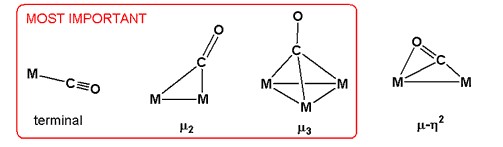
Oxid uhelnatý může být na kovy navázán více způsoby, které se mohou lišit hapticitou (η) a způsobem tvorby můstků. V komplexech typu η2-CO jsou na kov vázány uhlík i kyslík. Častěji je navázán pouze uhlík, poté se hapticita neuvádí.[3]
V dimerech a složitějších shlucích lze nalézt různé způsoby navazování karbonylů. Nejčastější z nich, označovaný μ2 nebo zjednodušeně μ, CO ligandy spojují dvojice kovů. Tyto vazby se vyskytují u některých běžných karbonylů, jako jsou Co2(CO)8, Fe2(CO)9, Fe3(CO)12 a Co4(CO)12.[4]
V některých vícejaderných shlucích vytvářejí molekuly CO mezi třemi nebo i čtyřmi atomy kovů; tyto ligandy se označují μ3-CO a μ4-CO. Méně časté jsou sloučeniny, kde vazbu s kovem tvoří atomy C i O, patří sem například μ3η2.
Struktura

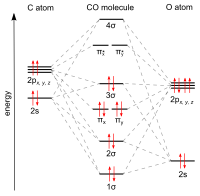
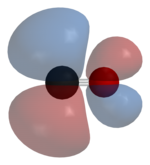
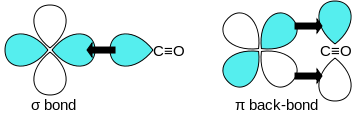
Oxid uhelnatý se na kovy váže prostřednictvím „synergických vazeb pí“. Vazba M-C má tři složky a má tak povahu částečně trojné vazby. Vazba sigma (σ) vzniká překryvem nevazebného (nebo slabě protivazebného) sp-hybridizovaného elektronového páru na uhlíku s d-, s- a p v atomu kovu. Dvojice vazeb pí (π) se utváří překryvem zaplněných orbitalů d-na kovu s π*-protivazebnými orbitaly molekuly CO. Druhý z těchto druhů vazby vyžaduje přítomnost d-elektronů v atomu kovu, který se také musí nacházet v nízkém oxidačním čísle (0 nebo +1), které způsobuje výhodnost dodávání elektronové hustoty. Když elektrony kovu zaplní π protivazebný orbital CO, tak oproti volnému oxidu uhelnatému oslabí vazbu uhlík–kyslík, zatímco vazba uhlík-kov se zesílí. Vzhledem k násobnosti vazby M–CO jsou vzdálenosti mezi atomy uhlíku a kovů poměrně krátké, často menší než 180 pm, zhruba o 20 pm kratší než vazby kov–alkyl. Přesné hodnoty vzdáleností M-CO a MC-O závisí na přítomnosti dalších ligandů na kovu. Jako příklad lze uvést následující údaje u Mo-C a C-O v Mo(CO)6 a Mo(CO)3(4-methylpyridin)3: 206/190 a 111/118 pm.[5]
K nalezení můstkových karbonylových ligandů je vhodná infračervená spektroskopie. U sloučenin s dvojitými CO můstky, označovanými μ2-CO nebo μ-CO, jsou frekvence prodlužování vazeb νCO obvykle posunuty o 100–200 cm−1 k nižším energiím oproti koncovým CO, které je mají okolo 1800 cm−1. Pásy u (μ3) CO ligandů se objevuj í na ještě nižších energiích. Vedle symetrických vazeb může CO tvořit můstky rovněž asymetricky.[6][7][8]
Fyzikální vlastnosti
Jednojaderné karbonylové komplexy jsou většinou bezbarvé či světle žluté kapaliny nebo pevné látky, hořlavé a toxické.[9] Hexakarbonyl vanadu, neobvykle stálý 17elektronový karbonyl, je ovšem modrou kapalinou.[1] Karbonyly obsahující více atomů kovů mívají výraznější zbarvení; dodekakarbonyl triželeza (Fe3(CO)12) například tvoří tmavě zelené krystaly. Krystalické karbonyly kovů často za nízkých tlaků sublimují, což mnohdy bývá doprovázeno rozkladem. Karbonyly bývají rozpustné v nepolárních i polárních organických rozpouštědlech, jako například benzenu, diethyletheru, acetonu, kyselině octové a tetrachlormethanu. Některé soli kationtových a aniontových karbonylů se rozpouští ve vodě a nižších alkoholech.[10]
Analytické zkoumání

Kromě rentgenové krystalografie lze pro zkoumání karbonylů kovů také použít infračervenou spektroskopii a 13C NMR. Tyto postupy poskytují informace o struktuře v odlišných časových měřítkách. Infračervenou spektroskopií lze prozkoumat vibrační hladiny, například u vibrací souvisejících s natahováním vazeb CO-, které obvykle probíhají velmi rychle, zatímco NMR přechody probíhají na nižších frekvencích a jejich trvání je srovnatelné s vnitromolekulárními výměnami ligandů.[11]
Při provádění infračervené spektroskopie u oktakarbonylu dikobaltu (Co2(CO)8) bylo nalezeno 13 νCO pásů, mnohem více, než bylo u jakékoliv jednotlivé sloučeniny očekáváno, což naznačuje přítomnost isomerů, z nichž některé mají a některé nemají můstkové CO ligandy. V 13C NMR spektru této látky se objevil jediný signál u chemického posunu 204 ppm. Tato jednoduchost NMR spektra je způsobena rychlou přeměnou isomerů mezi sebou.
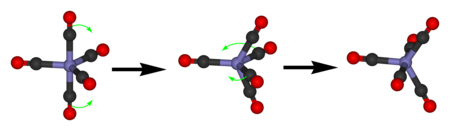
Pentakarbonyl železa má v 13C NMR spektru jediný signál, v důsledku rychlé výměny axiálních a ekvatoriálních CO ligandů Berryho pseudorotací.
Infračervená spektra

Důležitou metodou určování struktury karbonylů kovů je infračervená spektroskopie.[13]
Vibrace vazeb C-O, obvykle značené νCO, se u oxidu uhelnatého objevují při 2143 cm−1. Energie νCO pásů karbonylů kovů odpovídají síle vazby uhlík-kyslík a s jejich rostoucí silou klesá síla vazeb π mezi kovem a uhlíkem. π-zásaditost kovového centra je závislá na mnoha faktorech; u izoelektronické řady od titanu po železo se u příslušných hexakarbonylů vazby π oslabují s rostoucím kladným nábojem kovu. Nárůst této zásaditosti ligandů zvyšuje π-elektronovou hustotu na kovu a omezuje νCO. Tolmanův elektronový parametr využívá Ni(CO)3 fragment pro srovnání ligandů podle jejich schopností dodávat π elektrony.[14][15]
Počet vibračních módů karbonylu lze určit pomocí teorie grup. Pouze ty módy, které se přeměňují jako operátory elektrických dipólů mají nenulové přímé součiny a mohou být pozorovány. Počet pozorovatelných infračervených přechodů (ovšem nikoliv jejich energie) tak je možné předvídat.[16][17][18]
Například CO ligandy oktaedrických komplexů, jako je hexakarbonyl chromu, Cr(CO)6, se přeměňují jako a1g, eg a t1u, ale jen t1u mód (antisymetrické natažení apikálních karbonylů) je možné pozorovat a ve spektrech oktaedrických hexakarbonylů se tak vyskytuje pouze jeden νCO pás. Spektra komplexů s nižšími symetriemi jsou složitější, například infračervené spektrum nonakarbonylu diželeza, Fe2(CO)9,obsahuje CO pásy na 2082, 2019 a 1829 cm−1. Počet pozorovatelných pásů několika karbonylů je uveden v tabulce níže. Existují příslušné tabulky pro velký počet karbonylů.[13]
Tato pravidla se vztahují na karbonyly kovů v roztocích a v plynném skupenství. K dosažení vysokého rozlišení je vhodné použít málo polární rozpouštědlo. Při měření spekter pevných vzorků se počet pásů může navýšit.[19]
| Sloučenina | νCO (cm−1) | 13C NMR posun (ppm) | průměrná vzdálenost M-CO (pm) | průměrná vzdálenost C-O (pm) |
|---|---|---|---|---|
| CO | 2143 | 181 | ||
| Ti(CO) 2− 6 | 1748 | 245 | 204[20] | 116 |
| V(CO)6 | (paramagnetický) | 200 | 113[21] | |
| V(CO) − 6 | 1859 | 193 (PPN+ salt)[21] | ||
| Cr(CO)6 | 2000 | 212 | 191[22] | 114 |
| Mn(CO) + 6 | 2100 | |||
| Fe(CO) 2+ 6 | 2204 | 191 | 112 (BF4− salt)[23] | |
| Fe(CO)5 | 2022, 2000 | 209 | 180[24] | 112 |
| Ru(CO)5 | 2038, 2002[25] | |||
| Ni(CO)4 | 181 | 113 |
| Karbonyl | νCO, µ1 (cm−1) | νCO, µ2 (cm−1) | νCO, µ3 (cm−1) |
|---|---|---|---|
| Rh2(CO)8 | 2060, 2084 | 1846, 1862 | |
| Rh4(CO)12 | 2044, 2070, 2074 | 1886 | |
| Rh6(CO)16 | 2045, 2075 | 1819 |
NMR spektroskopie
Karbonyly kovů jsou často zkoumány 13. K dosažení lepší citlivosti se karbonyly mohou obohacovat o 13CO. Obvyklé chemické posuny koncových ligandů jsou 150-220 ppm. Můstkové ligandy rezonují mezi 230 a 280 ppm.[1]
signály 13C se s rostoucím protonovým číslem kovu posouvají k vyšším hodnotám.
Aktivační energie výměny ligandů je možné zjistit pomocí tepelné závislosti rozšiřování čar.[26]
Hmotnostní spektrometrie
Hmotnostní spektrometrie poskytuje údaje o struktuře a složení komplexů. Spektra polykarbonylů jsou často snadno vyhodnotitelná, protože hlavním druhem fragmentace je ztráta karbonylových ligandů, s poměrem hmotnosti k náboji (m/z) = 28.
- M(CO) +
n → +
n + M(CO) +
n-1 + CO
Při zkoumání neutrálních karbonylů kovů se většinou používá elektronová ionizace. Neutrální karbonyly mohou být přeměněny na nabité derivatizací, což umožňuje použití elektrosprejové ionizace, pro kterou je vybavení často dobře dostupné; například za přítomnosti alkoxidu se vytváří anionty metalakarboxylových kyselin použitelné k tomuto způsobu analýzy:
- LnM(CO) + RO− → [LnM−C(=O)OR]−
Některé karbonyly kovů reagují s azidy za vzniku isokyanátokomplexů a dusíku.[27] Tímto postupem lze určit molární hmotnosti původních komplexů a změny ve struktuře, jako jsou ztráty karbonylových skupin za podmínek analýzy.[28]
Míru fragmentace lze ovládat změnami napětí a teploty.
Spojením hmotnostní spektrometrie s infračervenou fotodisociační spektroskopií je možné u komplexů iontových karbonylů v plynné fázi získat údaje o vibracích molekul.[29]
Výskyt

Při zkoumání infračervených spekter ze středu Mléčné dráhy byly v mezihvězdném prachu nalezeny vibrace odpovídající karbonylům železa.[31]
Pozorování shluků karbonylů železa byla též učiněna u chondritových meteoritů zkoumaných infračervenou spektroskopií. Objevily se čtyři pásy koncových a můstkových karbonylových ligandů.[32]
V atmosféře Země, bohaté na kyslík, se karbonyly oxidují na oxidy kovů. Probíhají diskuze o tom, zda se tyto komplexy vytvářely v redukčních hydrotermálních prostředích a mohly fungovat jako katalyzátory tvorby důležitých biomolekul, jako je například kyselina pyrohroznová.[33]
Některé enzymy patřící mezi hydrogenázy obsahují CO vázaný na železo. Předpokládá se, že CO stabilizuje nízká oxidační čísla, což usnadňuje navazování vodíku. Metabolismu oxidu uhelnatého se také účastní CO dehydrogenáza a acetyl-CoA syntáza.[34]
Komplexy obsahující oxid uhelnatý mají vliv na toxicitu CO a na signalizování.[35]
Příprava
Přípravy různých karbonylů kovů jsou častým předmětem výzkumu v organokovové chemii. Bylo vyvinuto mnoho postupů přípravy jednojaderných i vícejaderných karbonylů.[36]
Reakce kovů s oxidem uhelnatým
Tetrakarbonyl niklu a pentakarbonyl železa lze připravit reakcemi kovu s oxidem uhelnatým:[37]
- Ni + 4 CO → Ni(CO)4 (1 bar, 55 °C)
- Fe + 5 CO → Fe(CO)5 (100 bar, 175 °C)
Tetrakarbonyl niklu se tvoří i při 80 °C za atmosférického tlaku, železo reaguje mezi 150 a 200 °C a tlaku oxidu uhelnatého od 50 do 200 bar.[38]
Ostatní karbonyly kovů se připravují jinými postupy.[39]
Redukce solí a oxidů
Některé karbonyly se získávají redukcemi halogenidů kovů za přítomnosti oxidu uhelnatého o vysokém tlaku. Lze přitom použít široké rozmezí redukčních činidel, například měď, hliník, vodík a alkyly kovů, jako jsou triethylhliník. Příkladem může být tvorba hexakarbonylu chromu z bezvodého chloridu chromitého redukcí hliníkem a katalýzy chloridem hlinitým; jako rozpouštědlo se zde používá benzen:[37]
- CrCl3 + Al + 6 CO → Cr(CO)6 + AlCl3
Používání triethylhliníku či diethylzinku, nebo jiných alkylů, jako redukčních činidel způsobuje oxidační párování alkylových radikálů za vzniku dimerních alkanů:
- WCl6 + 6 CO + 2 Al(C2H5)3 → W(CO)6 + 2 AlCl3 + 3 C4H10
Soli wolframu, molybdenu, manganu a rhodia lze redukovat hydridem lithnohlinitým. Hexakarbonyl se připravuje pomocí sodíku v chelatujících rozpouštědlech, jako je diglym.[9]
- VCl3 + 4 Na + 6 CO + 2 diglyme → Na(diglyme)2[V(CO)6] + 3 NaCl
- [V(CO)6]− + H+ → H[V(CO)6] → 1/2 H2 + V(CO)6
Soli niklu a kobaltu mohou být redukovány ve vodných roztocích, například dithioničitanem sodným. Kobaltnaté soli se za přítomnosti CO kvantitativně přeměňují na tetrakarbonylkobaltnanový anion:[9]
- 2 Co2+ + 3 S2O 2−
4 + 12 OH− + 8 CO → 2 Co(CO) −
4 + 6 SO 2−
3 + 6 H2O
U některých karbonylů může být k jejich přípravě být jako redukční činidlo použit přímo oxid uhelnatý; takto byl například poprvé připraven dekakarbonyl dirhenia z oxidu:[40]
- Re2O7 + 17 CO → Re2(CO)10 + 7 CO2
Při použití oxidů kovů je oxid uhelnatý jedním z produktů reakce. Při redukci chloridů CO se vytváří fosgen; příkladem takové reakce může být příprava chloridu karbonylu osmia z chloridů.[36] CO lze také použít k redukcím sulfidů, kde se jako vedlejší produkt vytváří karbonylsulfid.
Fotolýza a termolýza
Fotolýzou či termolýzou jednojaderných karbonylů vznikají vícejaderné karbonyly, jako je nonakarbonyl diželeza (Fe2(CO)9).[41][42]
- 2 Fe(CO)5 → Fe2(CO)9 + CO
Dalším zahříváním vzniká kov a oxid uhelnatý.
Tepelným rozkladem dodekakarbonylu triosmia (Os3(CO)12) vznikají mnohojaderné shluky, jako Os4(CO)13, Os6(CO)18 a Os8(CO)23.[9]
Karbonyly se smíšenými ligandy, například rutheniem, osmiem, rhodiem a iridiem se mohou získat odštěpením CO z molekul některých rozpouštědel, jako jsou dimethylformamid (DMF) a 2-methoxyethanol. Takto se připravuje Vaskův komplex (IrCl(CO)(PPh3)2) reakcí chloridu iriditého a trifenylfosfinu ve vroucím DMF.[43]
Podvojné záměny
Podvojnými záměnami solí, například reakcí KCo(CO)4 s [Ru(CO)3Cl2]2 lze účinně vytvářet smíšené karbonyly, zde jde o RuCo2(CO)11.[44]
- 4 KCo(CO)4 + [Ru(CO)3Cl2]2 → 2 RuCo2(CO)11 + 4 KCl + 11 CO
Příperava karbonylových kationtů a karbonylátů
Iontové karbonylové komplexy je možné získat oxidacemi či redukcemi neutrálních komplexů, například aniontové karbonyly lze připravit redukcemi dvojjaderných karbonylů sodíkem. Takto vzniká například sodná sůl tetrakarbonylátu železa (Na2Fe(CO)4, Collmanovo činidlo), používaná v organické syntéze.[45]
Soli kationtů hexakarbonylů manganu, technecia a rhenia lze vytvořit reakcemi karbonylhalogenidů s Lewisovými kyselinami
- Mn(CO)5Cl + AlCl3 + CO → [Mn(CO) +
6 ][AlCl −
4 ]
Pomocí silných kyselin se podařilo připravit kationty karbonylů zlata, jako například [Au(CO)2]+, používaný ke katalyzování karbonylací alkenů.[46] Kationtový komplex platiny [Pt(CO)4]2+ může být získán za přítomnosti superkyselin, jako je fluorid antimoničný.[47] Přestože bývá CO považován především za ligand vhodný pro kovy v nízkých oxidačních číslech, tak je znám i 16elektronový komplex čtyřmocného železa [Cp*2Fe]2+, který kvantitativně váže karbonylové ligandy za tvorby diamagnetického 18elektronového komplexu Fe4+-CO.[48]
Reakce
Karbonyly kovů často slouží na přípravu organokovových sloučenin. K běžným reakcím u nich patří náhrady oxidu uhelnatého jinými ligandy, oxidace a redukce kovových center a reakce karbonylových ligandů.[1]
Náhrady CO
CO ligandy lze tepelně či fotochemicky vyvolávanými reakcemi nahrazovat donorovými ligandy, jako jsou fosfiny, kyanidy (CN−), donory dusíku, a ethery, především ty, které mají chelatační vlastnosti. Alkeny, především dieny, mohou sloužit jako prekurzory synteticky významných sloučenin. Substituce 18elektronových komplexů obvykle probíhají disociačně přes 16elektronové meziprodukty:[49]
- M(CO)n → M(CO)n−1 + CO
- M(CO)n−1 + L → M(CO)n−1L
disociační energie činí tetrakarbonylu niklu 105 kJ/mol a u hexakarbonylu chromu 155 kJ/mol.[1]
Substituce (vzácně se objevujících) 17elektronových komplexů probíhají asociačně přes 19elektronové meziprodukty:
- M(CO)n + L → M
(CO)nL
- M(CO)nL → M(CO)n−1L + CO
Rychlosti substitucí 18elektronových komplexů lze někdy urychlit katalytickými množstvími oxidačních činidel, skrze přenosy elektronů.[50]
Redukce
Karbonyly kovů reagují s redukčními činidly, jako jsou sodík nebo sodíkový amalgám za vzniku karbonylátových aniontů:
- Mn2(CO)10 + 2 Na → 2 Na[Mn(CO)5]
Z pentakarbonylu železa takto vznikají tetrakarbonylželeznatany:
- Fe(CO)5 + 2 Na → Na2[Fe(CO)4] + CO
Rtuť se může navázat na vazby kov-kov některých vícejaderných karbonylů:
- Co2(CO)8 + Hg → (CO)4Co−Hg−Co(CO)4
Nukleofilní ataky na CO
CO ligandy mohou být atakovány nukleofily, například trimethylaminoxid přeměňuje CO ligandy na CO2 a bis(trimethylsilyl)amid draselný na CN−. V Hieberově reakci hydroxidový anion reaguje s CO ligandy na metalakarboxylové kyseliny, po čemž následuje uvolnění CO2 a tvorba hydridů kovů nebo karbonylmetalátů. Jako příklad takovéto nukleofilní adice může sloužit pžeměna pentakarbonylu železa na tetrakarbonylhydridoželeznatý anion:
- Fe(CO)5 + NaOH → Na[Fe(CO)4CO2H]
- Na[Fe(CO)4COOH] + NaOH → Na[HFe(CO)4] + NaHCO3
Karbonylové ligandy mohou také, hlavně v kationtových komplexech, reagovat s hydridy, za vzniku formylových sloučenin:
- [Re(CO)6]+ + H− → Re(CO)5CHO
Organolithné sloučeniny reagují s karbonyly kovů a při tom je mění na acylkarbonylové anionty. O-alkylacemi těchto aniontů, například Meerweinovými solemi, se tvoří Fischerovy karbeny.
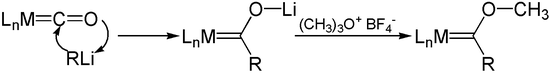
Reakce s elektrofily
I přes obecně nízká oxidační čísla kovů reagují karbonyly s elektrofily jen omezeně, jsou například odolné vůči alkylačním činidlům, slabším kyselinám a slabým oxidačním činidlům. Většina karbonylů kovů může vstupovat do halogenačních reakcí, například pentakarbonyl železa vytváří železnaté karbonylhalohenidy:
- Fe(CO)5 + X2 → Fe(CO)4X2 + CO
Halogeny mohou štěpit vazby kov-kov. Takovéto reakce lze považovat za oxidace kovů:
- Mn2(CO)10 + Cl2 → 2 Mn(CO)5Cl
Příklady sloučenin
Většina karbonylových komplexů, například Vaskův komplex, IrCl(CO)(P(C6H5)3)2, a methylcyclopentadienyltrikarbonyl manganu, (CH3C5H4)Mn(CO)3. Základními sloučeninami jsou zde mnohdy binární karbonyly, [Mx(CO)n]z, z nichž jsou některé komerčně dostupné. Občas tyto karbonyly mohou porušovat pravidlo 18 elektronů.
Neutrální binární karbonyly
- Kovy alkalických zemin, vápník, stroncium a baryum, mohou vytvářet oktakarbonyly M(CO)8 (M = Ca, Sr, Ba). Tyto sloučeniny byly prozkoumány v kryogenních matricích pomocí vibrační spektroskopie a v plynných fázích s využitím hmotnostní spektrometrie.[51]
- Sloučeniny prvků 4. skupiny, se 4 valenčními elektrony, by měly tvořit heptakarbonyly; ty jsou v čisté podobě vzácné, jsou však známy substituované deriváty Ti(CO)7.
- Karbonyly kovů 5. skupiny, majících 5 valenčních elektronů, vykazují sterické efekty, které brání vzniku sloučenin s vazbami M–M, jako by měl být V2(CO)12, jenž nebyl popsán; je však znám 17elektronový hexakarbonyl vanadu, V(CO)6.
- Prvky 6. skupiny, se 6 valenčními elektrony, tvoří hexakarbonyly, Cr(CO)6, Mo(CO)6, W(CO)6 a Sg(CO)6. Kovy 6. (a také 7. skupiny) také vykazují v organokovové syntéze cis (labilizaci CO v poloze cis).
- Prvky 7. skupiny, se sedmi elektrony ve valenčních vrstvách, vytvářejí dimerní pentakarbonyly, Mn2(CO)10, Tc2(CO)10 a Re2(CO)10.
- Z kovů 8. skupinyvznikají pentakarbonyly, Fe(CO)5, Ru(CO)5 a Os(CO)5. U Ru a Os jsou jednojaderné karbonyly nestabilní a dekarbonylují se na Ru3(CO)12 a Os3(CO)12. Významnými karbonyly železa jsou také Fe3(CO)12 a Fe2(CO)9.
- 9. skupina obsahuje kovy, u nichž se předpokládá tvorba dimerů tetrakarbonylů, M2(CO)8. Jedinou stabilní sloučeninou tohoto typu je oktakarbonyl dikobaltu, větší shluky jsou však známy od více kovů: Co4(CO)12, Rh4(CO)12, Rh6(CO)16 a Ir4(CO)12. Oktakarbonyl dikobaltu, Co2(CO)8, je, na rozdíl od většiny 18elektronových karbonylů přechodných kovů, citlivý na přítomnost kyslíku.
- Karbonyly kovů 10. skupiny, majících 10 valenčních elektronů, tvoří tetrakarbonyly, jako je Ni(CO)4; Pd(CO)4 a Pt(CO)4 jsou však nestabilní.
Aniontové binární karbonyly
- Od prvků 3. skupiny, skandia, yttria a lanthanu, jsou známy monoanionty, [M(CO)8]− (M = Sc, Y, La), patřící mezi 20elektronové karbonyly.[52]
- Kovy 4. skupiny vytváří dianionty podobné neutrálním sloučeninám kovů 6. skupiny, například [Ti(CO)6]2−.[53]
- Monoaniontové karbonyly prvků 5. skupiny, například [V(CO)6]−, se také podobají neutrálním sloučeninám kovů 6. skupiny.
- Monoanionty karbonylů kovů 7. skupiny, [M(CO)5]− (M = Mn, Tc, Re), jsou podobné neutrálním karbonylům prvků 8 skupiny.
- Prvky 8. skupiny tvoří dianionty s vlastnostmi blízkými neutrálním karbonylům prvků 10. skupiny, [M(CO)4]2− (M = Fe, Ru, Os). Jsou zde také zámy kondenzované deriváty.
- I monoanionty karbonylů 9. skupiny, například [Co(CO)4]−, mají vlastnosti blízké neutrálním komplexům 10. skupiny.
Byly rovněž popsány velké aniontové shluky niklu, palladia a platiny. Řadu aniontových karbonylů lze protonovat na příslušné hydridy.
Kationtové binární karbonyly
- [Kovy 2. skupiny vytváří ionty typu [M(CO)8]+ (M = Ca, Sr, Ba).[51]
- Z kovů 3. skupiny vznikají v plynných fázích sloučeniny [Sc(CO)7]+ a [Y(CO)8]+.[54]
- Monokationtové karbonyly kovů 7. skupiny, [M(CO)6]+ (M = Mn, Tc, Re), jsou svými vlastnostmi podobné neutrálním karbonylům kovů 6. skupiny.
- Dikationtové karbonyly prvků 8. skupiny, [M(CO)6]2+ (M = Fe, Ru, Os), jsou také podobné neutrálním karbonylům 6. skupiny.[55]
Neklasické karbonyly
Jako neklasické se označují karbonyly, u kterých je νCO vyšší a vazby C-O jsou kratší než u volného CO (113,7 pm). Tuto vlastnost má například [Fe(CO)6]2+, kde je dC-O pouze 112,9 pm. Obvykle jde o kationtové, někdy i dikationtové komplexy.[56]
Použití

Metalurgická využití
Karbonyly kovů se používají v rámci několika průmyslových procesů, jako je extrakce a přečišťování niklu pomocí tetrakarbonylu niklu v Mondově procesu.
Podobně se i čisté železo vyrábí tepelným rozkladem svého karbonylu. Karbonyl železa se mimo jiné používá na výrobu cívek, pigmentů, doplňků stravy,[57] a materiálů pohlcujících rádiové vlny v rámci technik stealth.[58]
Katalýza
Karbonyly kovu jsou zapojovány do řady průmyslových karbonylačních reakcí. Při oxo procesu reagují alken, vodík a oxid uhelnatý za přítomnosti katalyzátoru, například oktakarbonylu dikobaltu, přičemž vzniká aldehyd. Jako příklad lze uvést výrobu butyraldehydu z propenu:
- CH3CH=CH2 + H2 + CO → CH3CH2CH2CHO
Butyraldehyd se dále přeměňuje na 2-ethylhexanol, prekurzor plastifikátorů PVC, k čemuž slouží aldolová kondenzace následovaná hydrogenací vzniklého hydroxyaldehydu. Takto vytvořené oxo-aldehydy slouží dále na výrobu mastných alkoholů, z nichž poté vznikají tenzidy.
Další důležitou skupinou reakcí katalyzovaných karbonyly kovů jsou hydrokarboxylace. Níže je zobrazeno jejich využití k výrobě kyseliny akrylové a jejich esterů:
Také při cyklizaci acetylenu na cyklooktatetraen se používají jako katalyzátory karbonyly kovů:[59]
Při výrobě octové z methanolu, oxidu uhelnatého a vody se jako katalyzátory používají jodovodík a karbonyly rhodia a iridia. Existuje i obdobná karbonylace vytvářející anhydrid kyseliny octové.[60]
Molekuly uvolňující CO
Molekuly uvolňující oxid uhelnatý jsou karbonylové komplexy kovů vyvinuté jako možná léčiva pro uvolňování CO. Oxid uhelnatý při nízkých koncentracích působí jako vazodilatans a antiflogistikum. Tyto látky jsou předměty výzkumu, protože mohou být použity k doručování řízených množství CO do tkání a orgánů.[61]
Podobné sloučeniny
Nitrosylové komplexy
Existuje velké množství nitrosylových komplexů kovů, obsahujících NO ligandy. Na rozdíl od karbonylů ovšem homoleptické nitrosylové komplexy nejsou běžné. NO je silnějším π-akceptorem než CO.
Příklady mohou být CoNO(CO)3 a Fe(NO)2(CO)2, což jsou analogy Ni(CO)4.[62]
Thiokarbonylové komplexy
Komplexy obsahující CS ligandy jsou známy, i když nejsou běžné.[63][64] Jejich vzácnost částečně způsobuje nestabilita výchozího materiálu, sulfidu uhelnatého; musí tak být připravovány nepřímo, například reakcí tetrakarbonylželeznatanu sodného s thiofosgenem:
- Na2Fe(CO)4 + CSCl2 → Fe(CO)4CS + 2 NaCl
Byly také popsány komplexy obsahující selenokarbonylové (CSe) a tellurokarbonylové (CTe) ligandy.[65]
Isokyanidové komplexy
Izokyanidy také tvoří širokou skupinu komplexů podobných karbonylům kovů. Nejčastějšími ligandy z této skupiny jsou methylizokyanid a t (Me3CNC). Také sem patří trifluormethylizokyanid (CF3NC), nestabilní sloučenina tvořící stabilní komplexy s vlastnostmi podobnými karbonylům kovů.[66]
Toxikologie
Toxicitu karbonylů kovů způsobují oxid uhelnatý, samotný kov, a také jejich těkavost a nestabilita; samotná toxicita kovu se obvykle zvyšuje, což je způsobeno snadným vystavením látce; to může proběhnout vdechnutím a u kapalných karbonylů také použitím či absorpcí kůží v důsledku dobré rozpustnosti v tucích. Většina klinických dat byla získána z otrav tetrakarbonylem niklu a pentakarbonylem železa, které se často používají v průmyslu. Tetrakarbonyl niklu je považován za jeden z nejsilnějších inhalačních jedů.[67]
Vdechnutí tetrakarbonylu niklu způsobuje akutní nespecifické příznaky podobné otravě oxidem uhelnatým, jako jsou nauzea, kašel, bolest hlavy a horečka. Po delší době se objevují další příznaky, například tachykardie a cyanóza či potíže s trávicí soustavou. Poškození se objevují na plicích (například metalace plicních sklípků), mozku, játrech, ledvinách, nadledvinkách a slezině. Zotavování z otravy karbonyly kovů je často dlouhé.[68]
Chronické vystavení nízkým koncentracím tetrakarbonylu niklu může způsobovat nespavost, bolest hlavy, nevolnost a ztrátu paměti.[68] Tetrakarbonyl niklu je považován za karcinogen, ovšem klinicky zachytitelný tento účinek může být až za 20-30 let.[69]
Reference
V tomto článku byl použit překlad textu z článku Metal carbonyl na anglické Wikipedii.
- ↑ a b c d e C. Elschenbroich. Organometallics. [s.l.]: Wiley-VCH, 2006. ISBN 978-3-527-29390-2.
- ↑ a b Arnold F. Holleman; Nils Wiberg. Lehrbuch der Anorganischen Chemie. [s.l.]: [s.n.], 2007. Dostupné online. ISBN 978-3-11-017770-1. S. 1780.
- ↑ F. Albert Cotton. Proposed nomenclature for olefin-metal and other organometallic complexes. Journal of the American Chemical Society. 1968, s. 6230–6232. doi:10.1021/ja01024a059.
- ↑ P. J. Dyson; J. S. McIndoe. Transition Metal Carbonyl Cluster Chemistry. [s.l.]: Gordon & Breach, 2000. Dostupné online. ISBN 978-90-5699-289-7.
- ↑ D. A. Schut; D. R. Tyler; T. J. R. Weakley. The Crystal Structure of Tris(4-methylpyridine) Tricarbonylmolybdenum(0). Journal of Chemical Crystallography. 1996, s. 235–237. doi:10.1007/BF01673678.
- ↑ G. O. Spessard; G. L. Miessler. Organometallic Chemistry. New York: Oxford University Press, 2010. Dostupné online. ISBN 978-0-19-533099-1. S. 79–82.
- ↑ A. L. Sargent; M. B. Hall. Linear Semibridging Carbonyls. 2. Heterobimetallic Complexes Containing a Coordinatively Unsaturated Late Transition Metal Center. Journal of the American Chemical Society. 1989, s. 1563–1569. doi:10.1021/ja00187a005.
- ↑ P. Li; M. D. Curtis. A New Coordination Mode for Carbon Monoxide. Synthesis and Structure of Cp4Mo2Ni2S2(η1, μ4-CO). Journal of the American Chemical Society. 1989, s. 8279–8280. doi:10.1021/ja00203a040.
- ↑ a b c d A. F. Holleman; E. WIBERG; N. WIBERG. Lehrbuch der Anorganischen Chemie. 102nd. vyd. Berlin: de Gruyter, 2007. ISBN 978-3-11-017770-1. S. 1780–1822.
- ↑ W. McFarlane; G. Wilkinson. Inorganic Syntheses. [s.l.]: [s.n.], 1966. ISBN 9780470132395. doi:10.1002/9780470132395.ch47. Kapitola Triiron Dodecacarbonyl, s. 181–183.
- ↑ C. H. Londergan; C. P. Kubiak. Electron Transfer and Dynamic Infrared-Band Coalescence: It Looks like Dynamic NMR spectroscopy, but a Billion Times Faster. Chemistry: A European Journal. 2003, s. 5962–5969. doi:10.1002/chem.200305028. PMID 14679508.
- ↑ G. L. Miessler; D. A. Tarr. Inorganic Chemistry. Upper Saddle River, NJ: Pearson Prentice Hall, 2011. Dostupné online. S. 109–119; 534–538.
- ↑ a b P. S. Braterman. Metal Carbonyl Spectra. [s.l.]: Academic Press, 1975. Dostupné online.
- ↑ R. H. Crabtree. The Organometallic Chemistry of the Transition Metals. [s.l.]: Pearson Prentice Hall, 2005. ISBN 9780471718765. doi:10.1002/0471718769.ch4. Kapitola 4. Carbonyls, Phosphine Complexes, and Ligand Substitution Reactions, s. 87–124.
- ↑ C. A. Tolman. Steric effects of Phosphorus Ligands in Organometallic Chemistry and Homogeneous Catalysis. Chemical Reviews. 1977, s. 313–348. doi:10.1021/cr60307a002.
- ↑ F. A. Cotton. Chemical Applications of Group Theory. [s.l.]: Wiley Interscience, 1990. Dostupné online. ISBN 978-0-471-51094-9. S. 87–124.
- ↑ R. L. Carter. Molecular Symmetry and Group Theory. [s.l.]: Wiley, 1997. Dostupné online. ISBN 978-0-471-14955-2.
- ↑ D. C. Harris; M. D. Bertolucci. Symmetry and Spectroscopy: Introduction to Vibrational and Electronic Spectroscopy. [s.l.]: Oxford University Press, 1980. Dostupné online. ISBN 978-0-19-855152-2.
- ↑ H. J. Buttery; G. Keeling; S. F. A. Kettle; I. Paul; P. J. Stamper. Correlation between crystal structure and carbonyl-bond stretching vibrations of methyl benzene transition metal tricarbonyls. Faraday Discussions of the Chemical Society. 1969, s. 48. doi:10.1039/DF9694700048.}
- ↑ ELLIS, John E.; CHI, Kai Ming. Highly reduced organometallics. 28. Synthesis, isolation, and characterization of [K(cryptand 2.2.2)]2[Hf(CO)6], the first substance to contain hafnium in a negative oxidation state. Structural characterization of [K(cryptand 2.2.2)]2[M(CO)6].cntdot.pyridine (M = Ti, Zr, and Hf). Journal of the American Chemical Society. American Chemical Society (ACS), 1990, s. 6022–6025. ISSN 0002-7863. doi:10.1021/ja00172a017.
- ↑ a b BELLARD, S.; RUBINSON, K. A.; SHELDRICK, G. M. Crystal and Molecular Structure of Vanadium Hexacarbonyl. Acta Crystallographica. 1979, s. 271–274. doi:10.1107/S0567740879003332.
- ↑ JOST, A.; REES, B.; YELON, W. B. Electronic structure of chromium hexacarbonyl at 78 K. I. Neutron diffraction study. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry. International Union of Crystallography (IUCr), 1975-11-01, s. 2649–2658. ISSN 0567-7408. doi:10.1107/s0567740875008394.
- ↑ FINZE, Maik; BERNHARDT, Eduard; WILLNER, Helge; LEHMANN, Christian W.; AUBKE, Friedhelm. Homoleptic, σ-Bonded Octahedral Superelectrophilic Metal Carbonyl Cations of Iron(II), Ruthenium(II), and Osmium(II). Part 2: Syntheses and Characterizations of [M(CO)6][BF4]2 (M = Fe, Ru, Os). Inorganic Chemistry. American Chemical Society (ACS), 2005-05-10, s. 4206–4214. ISSN 0020-1669. doi:10.1021/ic0482483. PMID 15934749.
- ↑ BRAGA, Dario; GREPIONI, Fabrizia; ORPEN, A. Guy. Nickel carbonyl [Ni(CO)4] and iron carbonyl [Fe(CO)5]: molecular structures in the solid state. Organometallics. American Chemical Society (ACS), 1993, s. 1481–1483. ISSN 0276-7333. doi:10.1021/om00028a082.
- ↑ Adams R. D., Barnard T. S., Cortopassi J. E., Wu W., Li Z. Inorganic Syntheses. [s.l.]: [s.n.], 1998. (Inorganic Syntheses; sv. 32). ISBN 9780470132630. doi:10.1002/9780470132630.ch44. Kapitola Platinum-ruthenium carbonyl cluster complexes, s. 280–284.
- ↑ E. Riedel; R. Alsfasser; C. Janiak; T. M. Klapötke. Moderne Anorganische Chemie. [s.l.]: de Gruyter, 2007. ISBN 978-3-11-019060-1.
- ↑ W. Henderson; J. S. McIndoe. Mass Spectrometry of Inorganic, Coordination and Organometallic Compounds: Tools – Techniques – Tips. [s.l.]: John Wiley & Sons, 2005-04-01. Dostupné online. ISBN 978-0-470-85015-2.
- ↑ C. P. G. Butcher; P. J. Dyson; B. F. G. Johnson; T. Khimyak; J. S. McIndoe. Fragmentation of Transition Metal Carbonyl Cluster Anions: Structural Insights from Mass Spectrometry. Chemistry: A European Journal. 2003, s. 944–950. doi:10.1002/chem.200390116. PMID 12584710.
- ↑ A. M. Ricks; Z. E. Reed; M. A. Duncan. Infrared spectroscopy of mass-selected metal carbonyl cations. Journal of Molecular Spectroscopy. 2011, s. 63–74. ISSN 0022-2852. doi:10.1016/j.jms.2011.03.006. Bibcode 2011JMoSp.266...63R.
- ↑ G. B. Vásquez; X. Ji; C. Fronticelli; G. L. Gilliland. Human Carboxyhemoglobin at 2.2 Å Resolution: Structure and Solvent Comparisons of R-State, R2-State and T-State Hemoglobins. Acta Crystallographica D. 1998, s. 355–366. doi:10.1107/S0907444997012250. PMID 9761903.
- ↑ A. G. Tielens; D. H. Wooden; L. J. Allamandola; J. Bregman; F. C. Witteborn. The Infrared Spectrum of the Galactic Center and the Composition of Interstellar Dust. The Astrophysical Journal. 1996, s. 210–222. doi:10.1086/177049. PMID 11539170. Bibcode 1996ApJ...461..210T.
- ↑ Y. Xu; X. Xiao; S. Sun; Z. Ouyang. IR Spectroscopic Evidence of Metal Carbonyl Clusters in the Jiange H5 Chondrite. Lunar and Planetary Science. 1996, s. 1457–1458. Dostupné online. Bibcode 1996LPI....27.1457X.
- ↑ G. D. Cody; N. Z. Boctor; T. R. Filley; R. M. Hazen; J. H. Scott; A. Sharma; H. S. Yoder. Primordial Carbonylated Iron–Sulfur Compounds and the Synthesis of Pyruvate. Science. 2000, s. 1337–1340. doi:10.1126/science.289.5483.1337. PMID 10958777. Bibcode 2000Sci...289.1337C.
- ↑ Bioorganometallics: Biomolecules, Labeling, Medicine. Příprava vydání G. Jaouen. Weinheim: Wiley-VCH, 2006. ISBN 978-3-527-30990-0.
- ↑ J. Boczkowski; J. J. Poderoso; R. Motterlini. CO–Metal Interaction: Vital Signaling from a Lethal Gas. Trends in Biochemical Sciences. 2006, s. 614–621. doi:10.1016/j.tibs.2006.09.001. PMID 16996273.
- ↑ a b W. A. Herrmann. 100 Jahre Metallcarbonyle. Eine Zufallsentdeckung macht Geschichte. Chemie in unserer Zeit. 1988, s. 113–122. doi:10.1002/ciuz.19880220402.
- ↑ a b J. Huheey; E. Keiter; R. Keiter. Anorganische Chemie. [s.l.]: de Gruyter, 1995. Kapitola Metallcarbonyle.
- ↑ A. Mittasch. Über Eisencarbonyl und Carbonyleisen. Angewandte Chemie. 1928, s. 827–833. doi:10.1002/ange.19280413002. Bibcode 1928AngCh..41..827M.
- ↑ Gary L. Miessler; Paul J. Fischer; Donald Arthur Tarr. Inorganic Chemistry. [s.l.]: Prentice Hall, 2013. ISBN 978-0321811059. S. 696.
- ↑ W. Hieber; H. Fuchs. Über Metallcarbonyle. XXXVIII. Über Rheniumpentacarbonyl. Zeitschrift für anorganische und allgemeine Chemie. 1941, s. 256–268. doi:10.1002/zaac.19412480304.
- ↑ R. B. King. Organometallic Syntheses. New York: Academic Press, 1965.
- ↑ E. H. Braye; W. Hübel; M. D. Rausch; T. M. Wallace. Diiron Enneacarbonyl. Inorganic Syntheses. 1966, s. 178–181. doi:10.1002/9780470132395.ch46.
- ↑ G. S. Girolami; T. B. Rauchfuss; R. J. Angelici. Synthesis and Technique in Inorganic Chemistry. [s.l.]: University Science Books, 1999. Dostupné online. ISBN 0-935702-48-2. S. 190.
- ↑ E. Roland; H. Vahrenkamp. Zwei neue Metallcarbonyle: Darstellung und Struktur von RuCo2(CO)11 und Ru2Co2(CO)13. Chemische Berichte. 1966, s. 1133–1142. doi:10.1002/cber.19851180330.
- ↑ R. D. Pike. Encyclopedia of Reagents for Organic Synthesis. [s.l.]: [s.n.], 2001. ISBN 978-0471936237. doi:10.1002/047084289X.rd465. Kapitola Disodium Tetracarbonylferrate(−II).
- ↑ Q. Xu; Y. IMAMURA; M. FUJIWARA; Y. SOUMA. A New Gold Catalyst: Formation of Gold(I) Carbonyl, [Au(CO)n]+ (n = 1, 2), in Sulfuric Acid and Its Application to Carbonylation of Olefins. Journal of Organic Chemistry. 1997, s. 1594–1598. doi:10.1021/jo9620122.
- ↑ H. Sillner; M. BODENBINDER; R. BROCHLER; HWANG, G.; RETTIG, S. J.; TROTTER, J.; VON AHSEN, B. Superelectrophilic Tetrakis(carbonyl)palladium(II)- and platinum(II) Undecafluorodiantimonate(V), [Pd(CO)4][Sb2F11]2 and [Pt(CO)4][Sb2F11]2: Syntheses, Physical and Spectroscopic Properties, Their Crystal, Molecular, and Extended Structures, and Density Functional Theory Calculations: An Experimental, Computational, and Comparative Study. Journal of the American Chemical Society. 2001, s. 588–602. doi:10.1021/ja002360s. PMID 11456571.
- ↑ MALISCHEWSKI, Moritz; SEPPELT, Konrad; SUTTER, Jörg; MUNZ, Dominik; MEYER, Karsten. A Ferrocene-Based Dicationic Iron(IV) Carbonyl Complex. Angewandte Chemie International Edition. 2018, s. 14597–14601. ISSN 1433-7851. doi:10.1002/anie.201809464. PMID 30176109.
- ↑ Jim D. Atwood. Inorganic and Organometallic Reaction Mechanisms. [s.l.]: Wiley, 1997. ISBN 9780471188971.
- ↑ H. H. Ohst; J. K. Kochi. Electron-Transfer Catalysis of Ligand Substitution in Triiron Clusters. Journal of the American Chemical Society. 1986, s. 2897–2908. doi:10.1021/ja00271a019.
- ↑ a b Xuan Wu, Lili Zhao, Jiaye Jin, Sudip Pan, Wei Li, Xiaoyang Jin, Guanjun Wang, Mingfei Zhou, Gernot Frenking. Observation of alkaline earth complexes M(CO)8 (M = Ca, Sr, or Ba) that mimic transition metals. Science. 2018-08-31, s. 912–916. ISSN 0036-8075. doi:10.1126/science.aau0839. PMID 30166489. Bibcode 2018Sci...361..912W.
- ↑ Jiaye Jin, Tao Yang, Ke Xin, Guanjun Wang, Xiaoyang Jin, Mingfei Zhou, Gernot Frenking. Octacarbonyl Anion Complexes of Group Three Transition Metals [TM(CO)8]− (TM = Sc, Y, La) and the 18-Electron Rule. Angewandte Chemie International Edition. 2018-04-25, s. 6236–6241. ISSN 1433-7851. doi:10.1002/anie.201802590. PMID 29578636.
- ↑ J. E. Ellis. Metal Carbonyl Anions: from [Fe(CO)4]2− to [Hf(CO)6]2− and Beyond. Organometallics. 2003, s. 3322–3338. ISSN 1433-7851. doi:10.1021/om030105l.
- ↑ Antonio D. Brathwaite; Jonathon A. Maner; Michael A. Duncan. Testing the Limits of the 18-Electron Rule: The Gas-Phase Carbonyls of Sc+ and Y+. Inorganic Chemistry. 2013, s. 1166–1169. ISSN 0020-1669. doi:10.1021/ic402729g. PMID 24380416.
- ↑ M. Finze; E. Bernhardt; H. Willner; C. W. Lehmann; F. Aubke. Homoleptic, σ-Bonded Octahedral Superelectrophilic Metal Carbonyl Cations of Iron(II), Ruthenium(II), and Osmium(II). Part 2: Syntheses and Characterizations of [M(CO)6][BF4]2 (M = Fe, Ru, Os). Inorganic Chemistry. 2005, s. 4206–4214. doi:10.1021/ic0482483. PMID 15934749.
- ↑ Stephanie C. C. Lubbe; Pascal Vermeeren; Célia Fonseca Guerra; F. Matthias Bickelhaupt. The Nature of Nonclassical Carbonyl Ligands Explained by Kohn–Sham Molecular Orbital Theory. Chemistry – A European Journal. 2020, s. 15690–15699. doi:10.1002/chem.202003768. PMID 33045113.
- ↑ S. J. Fairweather-Tait; B. Teucher. Iron and Calcium Bioavailability of Fortified Foods and Dietary Supplements. Nutrition Reviews. 2002, s. 360–367. doi:10.1301/00296640260385801. PMID 12462518.
- ↑ D. Richardson. Stealth-Kampfflugzeuge: Täuschen und Tarnen in der Luft. Zürich: Dietikon, 2002. ISBN 978-3-7276-7096-1. S. 360–367.
- ↑ Günther Wilke. Organo Transition Metal Compounds as Intermediates in Homogeneous Catalytic Reactions. Pure and Applied Chemistry. 1978, s. 677–690. Dostupné online. doi:10.1351/pac197850080677.
- ↑ John Hartwig. Organotransition Metal Chemistry: From Bonding to Catalysis. New York: University Science Books, 2010. Dostupné online. ISBN 978-1-938787-15-7. S. 1160.
- ↑ Roberto Motterlini; Leo Otterbein. The therapeutic potential of carbon monoxide. Nature Reviews Drug Discovery. 2010, s. 728–743. doi:10.1038/nrd3228. PMID 20811383.
- ↑ T. W. Hayton; P. Legzdins; W. B. Sharp. Coordination and Organometallic Chemistry of Metal−NO Complexes. Chemical Reviews. 2002, s. 935–992. doi:10.1021/cr000074t. PMID 11942784.
- ↑ W. Petz. 40 Years of Transition-Metal Thiocarbonyl Chemistry and the Related CSe and CTe Compounds. Coordination Chemistry Reviews. 2008, s. 1689–1733. doi:10.1016/j.ccr.2007.12.011.
- ↑ A. F. Hill; J. D. E. T. Wilton-Ely. Chlorothiocarbonyl-bis(triphenylphosphine) iridium(I) [IrCl(CS)(PPh3)2]. Inorganic Syntheses. 2002, s. 244–245. ISBN 978-0-471-20825-9. doi:10.1002/0471224502.ch4.
- ↑ George R. Clark; Karen Marsden; Warren R. Roper; L. James Wright. Carbonyl, Thiocarbonyl, Selenocarbonyl, and Tellurocarbonyl Complexes Derived from a Dichlorocarbene Complex of Osmium. Journal of the American Chemical Society. 1980, s. 1206–1207. doi:10.1021/ja00523a070.
- ↑ D. Lentz. Fluorinated Isocyanides - More than Ligands with Unusual Properties. Angewandte Chemie International Edition in English. 1994, s. 1315–1331. doi:10.1002/anie.199413151.
- ↑ B. Madea. Rechtsmedizin. Befunderhebung - Rekonstruktion – Begutachtung. [s.l.]: Springer-Verlag, 2003. Dostupné online. ISBN 978-3-540-43885-4.
- ↑ a b J. M. Stellman. Encyclopaedia of Occupational Health and Safety. [s.l.]: International Labour Org, 1998. ISBN 978-91-630-5495-2.
- ↑ G. Mehrtens; M. Reichenbach; D. Höffler; G. G. Mollowitz. Der Unfallmann: Begutachtung der Folgen von Arbeitsunfällen, privaten Unfällen und Berufskrankheiten. Berlin / Heidelberg: Springer, 1998. ISBN 978-3-540-63538-3.
Externí odkazy
 Obrázky, zvuky či videa k tématu Karbonyly kovů na Wikimedia Commons
Obrázky, zvuky či videa k tématu Karbonyly kovů na Wikimedia Commons
Média použitá na této stránce
Synthese von Fischer-Carbene
Autor: unknown, Licence: CC BY-SA 3.0
Reppe Chemistry Reaction of Acetylene with alcohol
structure of cobalt carbonyl
Diagram showing synergic π back-bonding in transition metal carbonyls
Autor: Aishik Rehman (ঐশিক রেহমান), Licence: CC BY-SA 4.0
Carbon-monoxide-HOMO-phase-3D-balls
Ball-and-stick model of the iron pentacarbonyl molecule, Fe(CO)5, as found in the crystalline solid.
X-ray crystallographic data from J. Donohue, A. Caron (1964). "The crystal structure of iron pentacarbonyl: space group and refinement of the structure". Acta Cryst. 17: 663-667. DOI:10.1107/S0365110X6400161X..
Model constructed in CrystalMaker 8.1.
Image generated in Accelrys DS Visualizer.Autor: Muskid, Licence: CC BY-SA 3.0
MO scheme for CO after Wiberg N., Inorganic chemistry, 2001, Academic Press, ISBN 0123526515 p. 1538. Labeling of sigma MOs after CATHERINE E. HOUSECROFT AND ALAN G. SHARPE, Inorganic Chemistry
General structure of metal carbonyls with number of IR peaks. This is a Vector replacement for the file Metallcarbonyle.PNG and is fundamentally based on the file Table 3.png by Bwd.
Autor: Smokefoot, Licence: CC BY-SA 4.0
The inorganic compound: iron(0) pentacarbonyl [Fe(CO)5], as a orange liquid at room temperature, in air. Photographed at the University of Illinois at Urbana–Champaign.
Výměna ligandů Berryho pseudorotací u pentakarbonylu železa
Autor: Rifleman 82, Licence: CC BY-SA 3.0
The heme fragment of human carboxyhemoglobin, from the crystal structure determined in Gregory B. Vásquez, Xinhua Ji, Clara Fronticelli, Gary L. Gilliland (1998). "Human Carboxyhemoglobin at 2.2 Å Resolution: Structure and Solvent Comparisons of R-State, R2-State and T-State Hemoglobins". Acta Crys. D 54 (3): 355–366. DOI:10.1107/S0907444997012250., published as PDB 1AJ9.