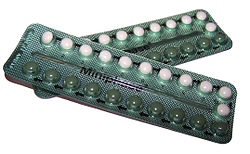
Kombinovaná perorální antikoncepce
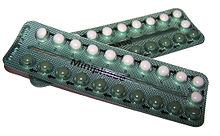
Kombinovaná perorální antikoncepce je typ antikoncepce, která je určena k perorálnímu užívání ženami. Obsahuje kombinaci estrogenu (obvykle ethinylestradiolu) a progestagenu (konkrétně progestinu). Při správném užívání mění menstruační cyklus tak, aby se vyloučila ovulace a zabránilo se otěhotnění.
Poprvé byly tyto tablety schváleny pro antikoncepční použití ve Spojených státech v roce 1960 a jsou velmi oblíbenou formou antikoncepce. Používá je více než 100 milionů žen na celém světě a téměř 12 milionů žen ve Spojených státech.[1] V letech 2015-2017 12,6 % žen ve věku 15-49 let v USA uvedlo, že perorální antikoncepci užívá, což z ní činí druhou nejčastější metodu antikoncepce v tomto věkovém rozmezí, přičemž nejčastější metodou je ženská sterilizace. Užívání se značně liší podle země, věku, vzdělání a rodinného stavu. Například ve Spojeném království užívá v současné době kombinované tablety nebo tablety obsahující pouze progestagen třetina žen ve věku 16–49 let, zatímco v Japonsku je to méně než 3 % žen (stav v letech 1950–2014).[2]
Kombinovaná perorální antikoncepce je na seznamu základních léčiv Světové zdravotnické organizace. Byla katalyzátorem sexuální revoluce.[3]
Lékařské využití
Antikoncepce
Kombinované perorální antikoncepční tablety jsou typem perorálního léku, který je určen k užívání každý den ve stejnou denní dobu, aby se zabránilo otěhotnění. Existuje mnoho různých přípravků nebo značek, ale průměrné balení je určeno k užívání po dobu 28 dnů nebo cyklu. Prvních 21 dní se denně užívá jedna tableta, která obsahuje hormony (estrogen a progestagen). Posledních 7 dní cyklu je bez hormonů. Některá balení obsahují pouze 21 tablet a následující týden se tablety neužívají. Jiná balení obsahují dalších 7 placebo tablet nebo biologicky neaktivních tablet. Některé novější přípravky obsahují 24 dní aktivních hormonálních tablet, po kterých následují 4 dny placeba (příkladem jsou Yaz 28 a Loestrin 24 Fe) nebo dokonce 84 dní aktivních hormonálních tablet, po kterých následuje 7 dní placebo tablet (Seasonale). Během dnů užívání placebo tablet nebo dnů bez tablet se objevuje krvácení z vysazení a i během této doby je uživatelka stále chráněna před otěhotněním.
Spolehlivost
Pokud se kombinovaná peroální antikoncepce užívá přesně podle návodu, odhadované riziko otěhotnění je 0,3 %, tedy přibližně 3 z 1000 uživatelek otěhotní během jednoho roku. Při typickém užívání je však spolehlivost nižší, kvůli chybám v pravidelnosti času užívání, opomenutí tablety nebo nežádoucím vedlejším účinkům. Při typickém užívání je odhadované riziko otěhotnění přibližně 9 %, neboli přibližně 9 ze 100 žen užívajících tento ryp antikoncepce otěhotní během jednoho roku.[4] Míra selhání při dokonalém užívání vychází z přehledu míry otěhotnění v klinických studiích, míra selhání při typickém užívání vychází z váženého průměru odhadů z amerických národních průzkumů z let 1995 a 2002, korigovaných o nenahlášené interrupce.[5]
Spolehlivost při typickém užívání je nižší než při spráném užívání, a to zněkolika důvodů:
- chyby na straně těch, kteří poskytují návod na správné užívání
- chyby na straně uživatelky
- vědomé nedodržení pokynů ze strany uživatelky
Uživatelka perorální hormonální antikoncepce může například dostat nesprávné informace o frekvenci užívání, zapomenout tabletu jeden den užít nebo včas nesehnat další balení.
Kombinované peroální antikoncepční tablety jsou účinnou metodou antikoncepce již od první tablety, pokud je užita do pěti dnů od začátku menstruačního cyklu (do pěti dnů od prvního dne menstruace). Pokud jsou tablety nasazeny kdykoli jindy v průběhu menstruačního cyklu, poskytují účinnou antikoncepci až po sedmi po sobě jdoucích dnech užívání aktivních tablet, proto je do té doby potřeba používat záložní metodu antikoncepce (např. kondom). Kombinované peroální antikoncepční tablety by se měly užívat každý den přibližně ve stejnou dobu.
Účinnost antikoncepce může být narušena mnoha dalšími léky. V každém z těchto případů by měla být použita záložní metoda, dokud se interagující lék nevysadí nebo se nevyřeší dané onemocnění a aktivní tablety nejsou opět důsledně užívány po dobu alespoň 7 po sobě jdoucích dnů.
Faktory snižující účinnost:
- opomenutí užití jedné nebo více aktivních tablet v balení
- opožděný začátek užívání dalšího balení
- střevní malabsorpce účinných tablet v důsledku zvracení nebo průjmu
- interakce jiných léků s aktivními tabletami
Další využití
Hormony obsažené v tabletách se používají také k léčbě různých onemocnění, jako je syndrom polycystických ovarií, endometrióza, adenomyóza, akné, hirsutismus, amenorea, menstruační křeče, menstruační migrény, menoragie (nadměrné menstruační krvácení), anémie související s menstruací nebo fibroidy a dysmenorea (bolestivá menstruace).[4] Kromě akné nebyla žádná perorální antikoncepce schválena americkým Úřadem pro kontrolu potravin a léčiv pro výše uvedená použití, a to i přes jejich časté předepisování pro tyto účely.
Syndrom polycystických ovarií
Syndrom polycystických ovarií je způsobený hormonální nerovnováhou. Ženy se syndromem polycystických ovarií mají často vyšší hladiny estrogenu, než je obvyklé, protože jejich hormonální cykly nejsou pravidelné. Vysoké hladiny estrogenu mohou časem vést k hyperplazii endometria neboli nadměrnému růstu tkáně v děloze. U tohoto přerůstání je větší riziko, že se stane rakovinným, než u normální endometriální tkáně. Ačkoli se přesná data liší, většina gynekologických společností se obecně shoduje na tom, že vzhledem k vysokým hladinám estrogenů, které mají ženy se symdromem polycystických ovarií, jsou vystaveny vyššímu riziku hyperplazie endometria.[6] Ke snížení tohoto rizika se často doporučuje, aby tyto ženy užívaly hormonální antikoncepci, která hladinu jejich hormonů reguluje. Doporučuje se jak kombinovaná antikoncepce, tak metody obsahující pouze progestin. Kombinovaná antikoncepce se upřednostňuje u žen, které trpí také silným akné a příznaky hirsutismu neboli mužského ochlupení, protože kombinovaná antikoncepce může pomoci tyto příznaky léčit.
Endometrióza
U pánevní bolesti spojené s endometriózou se kombinovaná peroální antikoncepce považuje za lék první volby spolu s nesteroidními antiflogistiky, agonisty GnRH a inhibitory aromatázy. Kombinovaná antikoncepce potlačuje růst mimoděložní endometriální tkáně. To zmírňuje její zánětlivé působení. Kombinovaná antikoncepce však spolu s dalšími výše uvedenými medikamenty narostlou mimoděložní tkáň nepotlačuje, pouze zmírňuje její příznaky. Jedinou definitivní léčbou je chirurgický zákrok. Studie zabývající se mírou recidivy pánevní bolesti po operaci ukázaly, že nepřerušované kontinuální užívání kombinované antikoncepce je při snižování recidivy bolesti účinnější než cyklické užívání.[7]
Adenomyóza
Podobně jako endometrióza se i adenomyóza často léčí pomocí kombinované antkoncepce, aby se potlačil růst endometriální tkáně, která prorostla do myometria. Na rozdíl od endometriózy jsou však při adenomyóze pro zmírnění pánevní bolesti než kombinované peroální tablety účinnější nitroděložní tělíska obsahující levonorgetrel.
Akné
Kombinovaná perorální antikoncepce se někdy předepisuje jako lék na mírné nebo středně těžké akné, ačkoli žádný z nich není schválen americkým Úřadem pro kontrolu potravin a léčiv pouze pro tento účel. Čtyři různé druhy perorální antikoncepce byly schváleny americkým Úřadem pro kontrolu potravin a léčiv k léčbě středně těžké akné, pokud je osobě alespoň 14 nebo 15 let, již začala menstruovat a potřebuje antikoncepci. Patří mezi ně Ortho Tri-Cyclen, Estrostep, Beyaz a YAZ.
Amenorea
Ačkoli jsou tablety někdy předepisovány k vyvolání pravidelné menstruace u žen, které trápí nepravidelný menstruační cyklus, ve skutečnosti normální menstruační cyklus potlačují a poté napodobují pravidelný 28denní měsíční cyklus.
Kontraindikace
Kombinovaná perorální antikoncepce je obecně považována za relativně bezpečný lék, je však kontraindikována u osob s určitými zdravotními potížemi. Světová zdravotnická organizace a americké Centrum pro kontrolu a prevenci nemocí zveřejňují pokyny, tzv. kritéria zdravotní způsobilosti, týkající se bezpečnosti antikoncepce v souvislosti se zdravotními stavy. Estrogen ve vysokých dávkách může u člověka zvýšit riziko vzniku krevních sraženin. U všech uživatelek kombinované antikoncepce dochází k malému zvýšení rizika žilního tromboembolismu ve srovnání s neuživatelkami; toto riziko je největší během prvního roku užívání kombinované antikoncepce.[8] Osoby s jakýmkoli zdravotními potížemi, které rovněž zvyšují riziko vzniku krevních sraženin, mají při užívání kombinované antikoncepce významnější zvýšení rizika trombotických příhod.[8] Mezi tyto stavy patří mimo jiné vysoký krevní tlak, kardiovaskulární onemocnění (např. chlopenní vada nebo ischemická choroba srdeční[9]), tromboembolie nebo plicní embolie v anamnéze, cerebrovaskulární příhoda a familiární sklon k tvorbě krevních sraženin (např. familiární faktor V Leiden). Existují zdravotní potíže, které v souvislosti s užíváním kombinované antikoncepce zvyšují riziko jiných nežádoucích účinků než trombózy. Například lidé s migrénou v anamnéze mají při užívání kombinované peroální antikoncepce zvýšené riziko cévní mozkové příhody a lidé, kteří kouří ve věku nad 35 let a užívají kombinovanou peroální antikoncepci, mají vyšší riziko infarktu myokardu.
Kombinovaná peroální antikoncepce je rovněž kontraindikována u osob s pokročilým diabetem, jaterními nádory, jaterním adenomem nebo těžkou jaterní cirhózou.[4] Kombinovaná peroální antikoncepce se metabolizuje v játrech, a proto může jaterní onemocnění vést ke snížené eliminaci léku. Ženy s rakovinou prsu nebo podezřením na ni, rakovinou endometria nebo neobjasněným děložním krvácením by rovněž neměly užívat kombinovanou peroální antikoncepci, aby se vyhnuly zdravotním rizikům.[9]
Těhotné ženy by kombinovanou antikoncepci užívat neměly. Ženám po porodu, které kojí, se rovněž doporučuje s užíváním kombinované antikoncepce dříve než 4 týdny po porodu z důvodu zvýšeného rizika vzniku krevních sraženin. Ačkoli studie prokázaly rozporuplné výsledky ohledně vlivu kombinované peroální antikoncepce na délku laktace a objem mléka, existují obavy z přechodného rizika kombinované antikoncepce na tvorbu mateřského mléka v době, kdy je s kojením začínáno brzy po porodu.[10] Vzhledem k uvedeným rizikům a dalším obavám ohledně laktace se ženám, které kojí, nedoporučuje začít užívat kombinovanou peroální antikoncepci dříve než šest týdnů po porodu, zatímco ženy, které nekojí a nemají jiné rizikové faktory pro vznik krevních sraženin, mohou začít užívat kombinovanou peroální antikoncepci 21 dní po porodu. Těžká hypercholesterolemie a hypertriglyceridémie jsou v současné době rovněž kontraindikací, ale důkazy prokazující, že kombinovaná peroální antikoncepce vede u těchto osob k horším výsledkům, jsou slabé. Obezita není považována za kontraindikaci užívání kombinované perorální antikoncepce.
Vedlejší účinky
Obecně se uznává, že zdravotní rizika perorální antikoncepce jsou nižší než rizika těhotenství a porodu a že „zdravotní přínosy jakékoli antikoncepční metody jsou mnohem vyšší než případná rizika této metody“. Některé organizace tvrdí, že srovnávání antikoncepční metody s žádnou metodou (těhotenstvím) není relevantní – místo toho by se bezpečnost měla srovnávat mezi dostupnými metodami antikoncepce.
Běžné
Různé zdroje uvádějí různý výskyt nežádoucích účinků. Nejčastějším nežádoucím účinkem je krvácení mimo menstruaci. Francouzský přehledový článek z roku 1992 uvádí, že až 50 % nových uživatelek přeruší užívání antikoncepčních pilulek před koncem prvního roku z důvodu obtěžujících nežádoucích účinků, jako je krvácení mimo menstruaci a amenorea.[11] Studie Kinseyho institutu z roku 2001 zkoumající indikátory přerušení užívání perorální antikoncepce zjistila, že 47 % ze 79 žen ji užívat přestalo.[12] Jedna studie z roku 1994 zjistila, že ženy užívající antikoncepční tablety mrkaly o 32 % častěji než ty, které antikoncepci neužívaly.[13]
Na druhou stranu mohou tablety někdy zdravotní potíže zlepšit, jako v případech dysmenorey, premenstruačního syndromu a akné,[14] zmírnit příznaky endometriózy a syndromu polycystických ovarií a snížit riziko anémie. Užívání perorální antikoncepce také snižuje celoživotní riziko rakoviny vaječníků a endometria.[15][16][17]
Může se objevit nevolnost, zvracení, bolest hlavy, nadýmání, citlivost prsou, otoky kotníků/nohou nebo změna hmotnosti. Může se objevit vaginální krvácení mezi menstruacemi (špinění) nebo vynechání/nepravidelná menstruace, zejména během několika prvních měsíců užívání.
Srdce a cévy
Kombinovaná perorální antikoncepce zvyšuje riziko žilní tromboembolie (včetně hluboké žilní trombózy a plicní embolie).[18]
I když užívání tablet kombinované antikoncepce s nižšími dávkami estrogenu může být méně rizikové co se týká mrtvice a infarktu myokardu ve srovnání s tabletami s vyšší dávkou estrogenu (50 μg/den), uživatelky tablet kombinované antikoncepce s nízkou dávkou estrogenu mají stále zvýšené riziko ve srovnání s neuživatelkami.[19] Tato rizika jsou největší u žen s dalšími rizikovými faktory, jako je kouření (které riziko výrazně zvyšuje) a dlouhodobé užívání tablet, zejména u žen starších 35 let.
Celkové absolutní riziko žilní trombózy na 100 000 žen při současném užívání kombinované perorální antikoncepce je přibližně 60, ve srovnání s 30 u žen, které ji neužívají.[20] Riziko tromboembolie se liší u různých typů antikoncepčních tablet; ve srovnání s kombinovanou perorální antikoncepcí obsahující levonorgestrel a při stejné dávce estrogenu a délce užívání je poměr míry výskytu hluboké žilní trombózy u kombinované perorální antikoncepce s norethisteronem 0,98, s norgestimátem 1,19, s desogestrelem 1,82, s gestodenem 1,86, s drospirenonem 1,64 a s cyproteron acetátem 1,88.[20] Pro srovnání, žilní tromboembolie se každoročně vyskytuje ve 100–200 případech na 100 000 těhotných žen.[20]
Jedna studie prokázala více než 600% zvýšení rizika vzniku krevních sraženin u žen užívajících kombinovanou peroální antikoncepci s drospirenonem ve srovnání s neužívajícími, zatímco u žen užívajících antikoncepční tablety obsahující levonorgestrel bylo toto riziko o 360 % vyšší.[21] Americký Úřad pro kontrolu potravin a léčiv inicioval studie hodnotící zdravotní stav více než 800 000 žen užívajících kombinovanou peroální antikoncepci a zjistil, že riziko hluboké žilní trmbózy bylo o 93 % vyšší u žen, které užívaly kombinovanou peroální antikoncepci s drospirenonem po dobu 3 měsíců nebo kratší, a o 290 % vyšší u žen užívajících kombinovanou peroální antikoncepci s drospirenonem po dobu 7–12 měsíců ve srovnání s ženami užívajícími jiné typy perorální antikoncepce.[22]
Na základě těchto studií americký Úřad pro kontrolu potravin a léčiv v roce 2012 aktualizoval etiketu kombinované peroální antikoncepce s drospirenonem tak, aby obsahovala varování, že antikoncepce s drospirenonem může zvýšit riziko vzniku nebezpečných krevních sraženin.
Systematický přehled a metaanalýza z roku 2015 zjistily, že kombinované antikoncepční tablety jsou spojeny se 7,6krát vyšším rizikem trombózy mozkových žilních splavů, což je vzácná forma cévní mozkové příhody, při níž dochází ke srážení krve v mozkových žilních splavech.[23]
Rakovina
Systematický přehled z roku 2010 nepotvrdil zvýšené celkové riziko rakoviny u uživatelek kombinovaných perorálních antikoncepčních tablet, ale zjistil mírné zvýšení rizika rakoviny prsu u současných uživatelek, které mizí 5–10 let po ukončení užívání.[24]
Ochranné účinky
Kombinovaná peroální antikoncepce snižuje riziko rakoviny vaječníků, endometria a kolorektálního karcinomu.[14][25] Dvě velké kohortové studie publikované v roce 2010 zjistily významné snížení relativního rizika úmrtí na rakovinu vaječníků a endometria u osob, které někdy užívaly peroální antikoncepci, ve srovnání s osobami, které peroální antikoncepci nikdy neužívaly.[26][27]
Užívání perorální antikoncepce (antikoncepčních tablet) po dobu pěti a více let snižuje riziko rakoviny vaječníků v pozdějším věku o 50 %.[25] Užívání kombinované perorální antikoncepce snižuje riziko rakoviny vaječníků o 40 % a riziko rakoviny děložní sliznice o 50 % ve srovnání s uživatelkami, které antikoncepci nikdy neužívaly. Riziko se snižuje s délkou užívání, přičemž při užívání delším než 10 let se riziko rakoviny vaječníků i endometria snižuje o 80 %. Snížení rizika rakoviny vaječníků i endometria přetrvává po dobu nejméně 20 let.
Zvýšení rizika
Zpráva pracovní skupiny Mezinárodní agentury pro výzkum rakoviny z roku 2005 uvádí, že kombinovaná perorální antikoncepce zvyšuje riziko rakoviny prsu (u současných i nedávných uživatelek), děložního čípku a jater (u populace s nízkým rizikem infekce virem hepatitidy B). Metaanalýza z roku 2013 dospěla k závěru, že každé užívání antikoncepčních tablet je spojeno s mírným zvýšením rizika rakoviny prsu (relativní riziko 1,08) a snížením rizika rakoviny tlustého střeva (relativní riziko 0,86) a rakoviny děložní sliznice (relativní riziko 0,57). Riziko rakoviny děložního čípku u osob infikovaných lidským papiloma virem je zvýšené.[28] Podobné malé zvýšení rizika rakoviny prsu bylo pozorováno i v dalších metaanalýzách.[29][30]
Hmotnost
Systematický přehled z roku 2013 dospěl ke zjištění, že studie kombinované hormonální antikoncepce neprokázaly žádný velký rozdíl v hmotnosti ve srovnání se skupinami s placebem nebo bez intervence.[31] Důkazy sice nebyly dostatečně silné na to, aby bylo možné s jistotou říci, že antikoncepční metody nezpůsobují určité změny hmotnosti, ale nebyl zjištěn žádný významný vliv.[31] Tento přehled také zjistil, „že ženy nepřestaly užívat tablety nebo náplasti kvůli změně hmotnosti“.[31]
Sexualita
Kombinovaná peroální antikoncepce může zvýšit přirozenou vaginální lubrikaci. U jiných žen dochází během užívání tablet ke snížení libida nebo ke snížení lubrikace. Někteří vědci zpochybňují příčinnou souvislost mezi užíváním kombinované peroální antikoncepce a snížením libida; studie z roku 2007, které se zúčastnilo 1700 žen, zjistila, že u uživatelek kombinované peroální antikoncepce nedošlo k žádné změně týkající se sexuálního uspokojení.[32] Laboratorní studie genitálního vzrušení z roku 2005 testovala čtrnáct žen před a po zahájení užívání kombinované peroální antikoncepce. Studie zjistila, že ženy po zahájení užívání tablet zažívaly výrazně širší škálu reakcí na vzrušení; poklesy i nárůsty vzrušení byly stejně časté.[33][34]
Studie z roku 2006, které se zúčastnilo 124 žen před menopauzou, měřila globulin vázající pohlavní hormony, a to i před a po vysazení perorálních antikoncepčních tablet. Ženy pokračující v užívání perorální antikoncepce měly hladinu tohoto glubulinu čtyřikrát vyšší než ty, které ji nikdy neužívaly, a hladina zůstala zvýšená i ve skupině, která jejich užívání přerušila.[35] Teoreticky může být toto zvýšení fyziologickou reakcí na zvýšenou hladinu hormonů, ale může snižovat volné hladiny jiných hormonů, např. androgenů, kvůli nespecifičnosti jeho vazby na pohlavní hormony.
Deprese
Nízká hladina serotoninu je spojována s depresí. Bylo prokázáno, že vysoké hladiny estrogenu, jako je tomu u kombinované peroální antikoncepce první generace, a progestinu, jako je tomu u některých antikoncepčních přípravků obsahujících pouze progestin, snižují hladinu serotoninu v mozku tím, že zvyšují koncentraci mozkového enzymu, který serotonin snižuje. Rostoucí počet vědeckých důkazů naznačuje, že hormonální antikoncepce může mít nepříznivý vliv na psychické zdraví žen.[36][37][38] V roce 2016 rozsáhlá dánská studie na jednom milionu žen (sledovaných od ledna 2000 do prosince 2013) ukázala, že užívání kombinované hormonální antikoncepce, zejména u dospívajících, je spojeno se statisticky významně zvýšeným rizikem následné deprese (například 2,1 % žen, které užívaly jakoukoli formu perorální antikoncepce, byla poprvé předepsána antidepresiva, zatímco v kontrolní skupině to bylo 1,7 % žen).[37] Podobně byly v roce 2018 zveřejněny výsledky rozsáhlé celonárodní švédské kohortové studie zkoumající vliv hormonální antikoncepce na duševní zdraví žen (n=815 662, ve věku 12–30 let), které upozorňují na souvislost mezi hormonální antikoncepcí a následným užíváním psychotropních drog u žen v reprodukčním věku.[38] Tato korelace byla obzvláště velká u mladých dospívajících (ve věku 12–19 let).[38] Autoři vyzývají k dalšímu výzkumu vlivu různých druhů hormonální antikoncepce na psychické zdraví mladých žen.[38]
Je známo, že antikoncepce obsahující pouze progestin zhoršuje stav žen, které již depresí trpí.[39][40] Současné lékařské referenční učebnice o antikoncepci a významné organizace, jako je i Světová zdravotnická organizace, se však shodují, že podle současných poznatků nízké dávky kombinované perorální antikoncepce pravděpodobně nezvyšují riziko deprese a pravděpodobně nezhoršují stav žen, které již depresí trpí.
Vysoký krevní tlak
Bradykinin snižuje krevní tlak tím, že způsobuje rozšíření cév. Některé enzymy jsou schopny odbourávat bradykinin (angiotenzin konvertující enzym, aminopeptidáza P). Progesteron může zvyšovat hladinu aminopeptidázy P (AP-P), a tím zvyšovat odbourávání bradykininu, což zvyšuje riziko vzniku vysokého krevního tlaku.[41]
Reference
V tomto článku byl použit překlad textu z článku Combined oral contraceptive pill na anglické Wikipedii.
- ↑ MOSHER, William D.; MARTINEZ, Gladys M.; CHANDRA, Anjani; ABMA, Joyce C.; WILLSON, Stephanie J. Use of contraception and use of family planning services in the United States: 1982-2002. S. 1–36. Advance Data [online]. 2004-12-10. Čís. 350, s. 1–36. Dostupné online. ISSN 0147-3956. PMID 15633582. (anglicky)
- ↑ YOSHIDA, Honami; SAKAMOTO, Haruka; LESLIE, Asuka; TAKAHASHI, Osamu; TSUBOI, Satoshi; KITAMURA, Kunio. Contraception in Japan: Current trends. S. 475–477. Contraception [online]. 2016-06. Roč. 93, čís. 6, s. 475–477. Dostupné online. DOI 10.1016/j.contraception.2016.02.006. PMID 26872717. (anglicky)
- ↑ HARRIS, Gardiner. It Started More Than One Revolution. The New York Times [online]. 2010-05-03 [cit. 2022-05-13]. Dostupné online. ISSN 0362-4331. (anglicky)
- ↑ a b c CURTIS, Kathryn M.; TEPPER, Naomi K.; JATLAOUI, Tara C.; BERRY-BIBEE, Erin; HORTON, Leah G.; ZAPATA, Lauren B.; SIMMONS, Katharine B. U.S. Medical Eligibility Criteria for Contraceptive Use, 2016. S. 1–103. MMWR. Recommendations and Reports [online]. 2016-07-29. Roč. 65, čís. 3, s. 1–103. Dostupné online. DOI 10.15585/mmwr.rr6503a1. PMID 27467196. (anglicky)
- ↑ TRUSSELL, James. Contraceptive failure in the United States. S. 397–404. Contraception [online]. 2011-05. Roč. 83, čís. 5, s. 397–404. Dostupné online. DOI 10.1016/j.contraception.2011.01.021. PMID 21477680. (anglicky)
- ↑ HARDIMAN, Paul; PILLAY, Ouma S; ATIOMO, William. Polycystic ovary syndrome and endometrial carcinoma. S. 1810–1812. The Lancet [online]. 2003-05. Roč. 361, čís. 9371, s. 1810–1812. Dostupné online. DOI 10.1016/S0140-6736(03)13409-5. PMID 12781553. (anglicky)
- ↑ ZORBAS, Konstantinos A.; ECONOMOPOULOS, Konstantinos P.; VLAHOS, Nikos F. Continuous versus cyclic oral contraceptives for the treatment of endometriosis: a systematic review. S. 37–43. Archives of Gynecology and Obstetrics [online]. 2015-07. Roč. 292, čís. 1, s. 37–43. Dostupné online. DOI 10.1007/s00404-015-3641-1. PMID 25644508. (anglicky)
- ↑ a b BLACK, Amanda; GUILBERT, Edith; COSTESCU, Dustin; DUNN, Sheila; FISHER, William; KIVES, Sari; MIROSH, Melissa. No. 329-Canadian Contraception Consensus Part 4 of 4 Chapter 9: Combined Hormonal Contraception. S. 229–268.e5. Journal of Obstetrics and Gynaecology Canada [online]. 2017-04. Roč. 39, čís. 4, s. 229–268.e5. Dostupné online. DOI 10.1016/j.jogc.2016.10.005. PMID 28413042. (anglicky)
- ↑ a b COOPER, Danielle B.; PATEL, Preeti; MAHDY, Heba. Oral Contraceptive Pills. StatPearls [online]. StatPearls Publishing, 2022. Dostupné online. PMID 28613632. (anglicky)
- ↑ LOPEZ, Laureen M; GREY, Thomas W; STUEBE, Alison M; CHEN, Mario; TRUITT, Sarah T; GALLO, Maria F. Combined hormonal versus nonhormonal versus progestin-only contraception in lactation. Cochrane Database of Systematic Reviews [online]. 2015-03-20. Dostupné online. DOI 10.1002/14651858.CD003988.pub2. PMID 25793657. (anglicky)
- ↑ SERFATY, D. Medical aspects of oral contraceptive discontinuation. S. 21–33. Advances in Contraception [online]. 1992-10. Roč. 8, čís. S1, s. 21–33. Dostupné online. DOI 10.1007/BF01849448. PMID 1442247. (anglicky)
- ↑ SANDERS, Stephanie A; GRAHAM, Cynthia A; BASS, Jennifer L; BANCROFT, John. A prospective study of the effects of oral contraceptives on sexuality and well-being and their relationship to discontinuation. S. 51–58. Contraception [online]. 2001-07. Roč. 64, čís. 1, s. 51–58. Dostupné online. DOI 10.1016/S0010-7824(01)00218-9. PMID 11535214. (anglicky)
- ↑ YOLTON, D. P.; YOLTON, R. L.; LÓPEZ, R.; BOGNER, B.; STEVENS, R.; RAO, D. The effects of gender and birth control pill use on spontaneous blink rates. S. 763–770. Journal of the American Optometric Association [online]. 1994-11. Roč. 65, čís. 11, s. 763–770. Dostupné online. ISSN 0003-0244. PMID 7822673. (anglicky)
- ↑ a b HUBER, Johannes C; BENTZ, Eva-Katrin; OTT, Johannes; TEMPFER, Clemens B. Non-contraceptive benefits of oral contraceptives. S. 2317–2325. Expert Opinion on Pharmacotherapy [online]. 2008-09. Roč. 9, čís. 13, s. 2317–2325. Dostupné online. DOI 10.1517/14656566.9.13.2317. PMID 18710356. (anglicky)
- ↑ VO, Christine; CARNEY, Michael E. Ovarian Cancer Hormonal and Environmental Risk Effect. S. 687–700. Obstetrics and Gynecology Clinics of North America [online]. 2007-12-01. Roč. 34, čís. 4, s. 687–700. Dostupné online. DOI 10.1016/j.ogc.2007.09.008. PMID 18061864. (anglicky)
- ↑ BANDERA, Christina A. Advances in the understanding of risk factors for ovarian cancer. S. 399–406. The Journal of Reproductive Medicine [online]. 2005-06. Roč. 50, čís. 6, s. 399–406. Dostupné online. ISSN 0024-7758. PMID 16050564. (anglicky)
- ↑ PRAGOUT, D.; LAURENCE, V.; BAFFET, H.; RACCAH-TEBEKA, B.; ROUSSET-JABLONSKI, C. Contraception et cancer. RPC Contraception CNGOF. S. 834–844. Gynécologie Obstétrique Fertilité & Sénologie [online]. 2018-12. Roč. 46, čís. 12, s. 834–844. Dostupné online. DOI 10.1016/j.gofs.2018.10.010. PMID 30385358. (anglicky)
- ↑ BLANCO-MOLINA, Ángeles; MONREAL, Manuel. Venous thromboembolism in women taking hormonal contraceptives. S. 211–215. Expert Review of Cardiovascular Therapy [online]. 2010-02. Roč. 8, čís. 2, s. 211–215. Dostupné online. DOI 10.1586/erc.09.175. PMID 20136607. (anglicky)
- ↑ ROACH, Rachel E.J.; HELMERHORST, Frans M; LIJFERING, Willem M.; STIJNEN, Theo; ALGRA, Ale; DEKKERS, Olaf M. Combined oral contraceptives: the risk of myocardial infarction and ischemic stroke. Cochrane Database of Systematic Reviews [online]. 2015-08-27. Dostupné online. DOI 10.1002/14651858.CD011054.pub2. PMID 26310586. (anglicky)
- ↑ a b c EICHINGER, S.; EVERS, J.L.H.; GLASIER, A.; LA VECCHIA, C.; MARTINELLI, I.; SKOUBY, S.; SOMIGLIANA, E. Venous thromboembolism in women: a specific reproductive health risk. S. 471–482. Human Reproduction Update [online]. 2013-09-01. Roč. 19, čís. 5, s. 471–482. Dostupné online. DOI 10.1093/humupd/dmt028. PMID 23825156. (anglicky)
- ↑ LIDEGAARD, Øjvind; MILSOM, Ian; GEIRSSON, Reynir Tomas; SKJELDESTAD, Finn Egil. Hormonal contraception and venous thromboembolism: Hormonal contraception and venous thromboembolism. S. 769–778. Acta Obstetricia et Gynecologica Scandinavica [online]. 2012-07 [cit. 2022-05-17]. Roč. 91, čís. 7, s. 769–778. Dostupné v archivu pořízeném z originálu dne 2022-05-17. DOI 10.1111/j.1600-0412.2012.01444.x. PMID 22568831. (anglicky)
- ↑ DUNN, N. The risk of deep venous thrombosis with oral contraceptives containing drospirenone. S. d2519–d2519. BMJ [online]. 2011-04-21. Roč. 342, čís. apr21 2, s. d2519–d2519. Dostupné online. DOI 10.1136/bmj.d2519. PMID 21511807. (anglicky)
- ↑ AMOOZEGAR, Farnaz; RONKSLEY, Paul E.; SAUVE, Reg; MENON, Bijoy K. Hormonal Contraceptives and Cerebral Venous Thrombosis Risk: A Systematic Review and Meta-Analysis. Frontiers in Neurology [online]. 2015-02-02. Roč. 6. Dostupné online. DOI 10.3389/fneur.2015.00007. PMID 25699010.
- ↑ CIBULA, D.; GOMPEL, A.; MUECK, A. O.; LA VECCHIA, C.; HANNAFORD, P. C.; SKOUBY, S. O.; ZIKAN, M. Hormonal contraception and risk of cancer. S. 631–650. Human Reproduction Update [online]. 2010-11-01. Roč. 16, čís. 6, s. 631–650. Dostupné online. DOI 10.1093/humupd/dmq022. PMID 20543200. (anglicky)
- ↑ a b BAST, Robert C.; BREWER, Molly; ZOU, Changping; HERNANDEZ, Mary A.; DALEY, Mary; OZOLS, Robert; LU, Karen. Prevention and Early Detection of Ovarian Cancer: Mission Impossible?. S. 91–100. Cancer Prevention [online]. 2007. Roč. 174, s. 91–100. Dostupné online. DOI 10.1007/978-3-540-37696-5_9. PMID 17302189. (anglicky)
- ↑ HANNAFORD, Philip C; IVERSEN, Lisa; MACFARLANE, Tatiana V; ELLIOTT, Alison M; ANGUS, Valerie; LEE, Amanda J. Mortality among contraceptive pill users: cohort evidence from Royal College of General Practitioners' Oral Contraception Study. S. c927–c927. BMJ [online]. 2010-03-11. Roč. 340, čís. mar11 1, s. c927–c927. Dostupné online. DOI 10.1136/bmj.c927. PMID 20223876. (anglicky)
- ↑ VESSEY, Martin; YEATES, David; FLYNN, Susan. Factors affecting mortality in a large cohort study with special reference to oral contraceptive use. S. 221–229. Contraception [online]. 2010-09-01. Roč. 82, čís. 3, s. 221–229. Dostupné online. DOI 10.1016/j.contraception.2010.04.006. PMID 20705149. (anglicky)
- ↑ GIERISCH, Jennifer M.; COEYTAUX, Remy R.; URRUTIA, Rachel Peragallo; HAVRILESKY, Laura J.; MOORMAN, Patricia G.; LOWERY, William J.; DINAN, Michaela. Oral Contraceptive Use and Risk of Breast, Cervical, Colorectal, and Endometrial Cancers: A Systematic Review. S. 1931–1943. Cancer Epidemiology Biomarkers & Prevention [online]. 2013-11. Roč. 22, čís. 11, s. 1931–1943. Dostupné online. DOI 10.1158/1055-9965.EPI-13-0298. PMID 24014598. (anglicky)
- ↑ ANOTHAISINTAWEE, Thunyarat; WIRATKAPUN, Cholatip; LERDSITTHICHAI, Panuwat; KASAMESUP, Vijj; WONGWAISAYAWAN, Sansanee; SRINAKARIN, Jiraporn; HIRUNPAT, Siriporn. Risk Factors of Breast Cancer: A Systematic Review and Meta-Analysis. S. 368–387. Asia Pacific Journal of Public Health [online]. 2013-09. Roč. 25, čís. 5, s. 368–387. Dostupné online. DOI 10.1177/1010539513488795. PMID 23709491. (anglicky)
- ↑ ZHU, Hang; LEI, Xun; FENG, Jing; WANG, Yang. Oral contraceptive use and risk of breast cancer: A meta-analysis of prospective cohort studies. S. 402–414. The European Journal of Contraception & Reproductive Health Care [online]. 2012-12. Roč. 17, čís. 6, s. 402–414. Dostupné online. DOI 10.3109/13625187.2012.715357. PMID 23061743. (anglicky)
- ↑ a b c LOPEZ, Laureen M; EDELMAN, Alison; CHEN, Mario; OTTERNESS, Conrad; TRUSSELL, James; HELMERHORST, Frans M. Progestin-only contraceptives: effects on weight. S. CD008815.pub3. Cochrane Database of Systematic Reviews [online]. 2013-07-02. S. CD008815.pub3. Dostupné online. DOI 10.1002/14651858.CD008815.pub3. PMID 23821307. (anglicky)
- ↑ WESTHOFF, Carolyn L.; HEARTWELL, Stephen; EDWARDS, Sharon; ZIEMAN, Mimi; STUART, Gretchen; CWIAK, Carrie; DAVIS, Anne. Oral contraceptive discontinuation: do side effects matter?. S. 412.e1–412.e7. American Journal of Obstetrics and Gynecology [online]. 2007-04. Roč. 196, čís. 4, s. 412.e1–412.e7. Dostupné online. DOI 10.1016/j.ajog.2006.12.015. PMID 17403440. (anglicky)
- ↑ SEAL, Brooke N.; BROTTO, Lori A.; GORZALKA, Boris B. Oral contraceptive use and female genital arousal: Methodological considerations. S. 249–258. Journal of Sex Research [online]. 2005-08. Roč. 42, čís. 3, s. 249–258. Dostupné online. DOI 10.1080/00224490509552279. (anglicky)
- ↑ HIGGINS, Jenny A.; DAVIS, Anne R. Contraceptive sex acceptability: a commentary, synopsis and agenda for future research. S. 4–10. Contraception [online]. 2014-07. Roč. 90, čís. 1, s. 4–10. Dostupné online. DOI 10.1016/j.contraception.2014.02.029. PMID 24792147. (anglicky)
- ↑ PANZER, Claudia; WISE, Sarah; FANTINI, Gemma; KANG, Dongwoo; MUNARRIZ, Ricardo; GUAY, Andre; GOLDSTEIN, Irwin. ORIGINAL RESEARCH—WOMEN's SEXUAL DYSFUNCTION: Impact of Oral Contraceptives on Sex Hormone‐Binding Globulin and Androgen Levels: A Retrospective Study in Women with Sexual Dysfunction. S. 104–113. The Journal of Sexual Medicine [online]. 2006-01. Roč. 3, čís. 1, s. 104–113. Dostupné online. DOI 10.1111/j.1743-6109.2005.00198.x. PMID 16409223. (anglicky)
- ↑ KULKARNI, Jayashri. Depression as a side effect of the contraceptive pill. S. 371–374. Expert Opinion on Drug Safety [online]. 2007-07. Roč. 6, čís. 4, s. 371–374. Dostupné online. DOI 10.1517/14740338.6.4.371. PMID 17688380. (anglicky)
- ↑ a b SKOVLUND, Charlotte Wessel; MØRCH, Lina Steinrud; KESSING, Lars Vedel; LIDEGAARD, Øjvind. Association of Hormonal Contraception With Depression. S. 1154. JAMA Psychiatry [online]. 2016-11-01. Roč. 73, čís. 11, s. 1154. Dostupné online. DOI 10.1001/jamapsychiatry.2016.2387. PMID 27680324. (anglicky)
- ↑ a b c d ZETTERMARK, Sofia; PEREZ VICENTE, Raquel; MERLO, Juan. Hormonal contraception increases the risk of psychotropic drug use in adolescent girls but not in adults: A pharmacoepidemiological study on 800 000 Swedish women. S. e0194773. PLOS ONE [online]. 2018-03-22. Roč. 13, čís. 3, s. e0194773. Dostupné online. DOI 10.1371/journal.pone.0194773. PMID 29566064. (anglicky)
- ↑ KULKARNI, Jayashri; LIEW, Jacynth; GARLAND, Kathryn A. Depression associated with combined oral contraceptives--a pilot study. S. 990. Australian Family Physician [online]. 2005-11. Roč. 34, čís. 11, s. 990. Dostupné online. ISSN 0300-8495. PMID 16299641. (anglicky)
- ↑ YOUNG, Elizabeth A.; KORNSTEIN, Susan G.; HARVEY, Anne T.; WISNIEWSKI, Stephen R.; BARKIN, Jennifer; FAVA, Maurizio; TRIVEDI, Madhukar H. Influences of hormone-based contraception on depressive symptoms in premenopausal women with major depression. S. 843–853. Psychoneuroendocrinology [online]. 2007-08. Roč. 32, čís. 7, s. 843–853. Dostupné online. DOI 10.1016/j.psyneuen.2007.05.013. PMID 17629629. (anglicky)
- ↑ LA CORTE, Amy L Cilia; CARTER, Angela M; TURNER, Anthony J; GRANT, Peter J; HOOPER, Nigel M. The bradykinin-degrading aminopeptidase P is increased in women taking the oral contraceptive pill. S. 221–225. Journal of the Renin-Angiotensin-Aldosterone System [online]. 2008-12. Roč. 9, čís. 4, s. 221–225. Dostupné online. DOI 10.1177/1470320308096405. PMID 19126663. (anglicky)
Externí odkazy

Přečtěte si prosím pokyny pro využití článků o zdravotnictví.
Média použitá na této stránce
Star of life, blue version. Represents the Rod of Asclepius, with a snake around it, on a 6-branch star shaped as the cross of 3 thick 3:1 rectangles.
Design:
The logo is basically unicolor, most often a slate or medium blue, but this design uses a slightly lighter shade of blue for the outer outline of the cross, and the outlines of the rod and of the snake. The background is transparent (but the star includes a small inner plain white outline). This makes this image usable and visible on any background, including blue. The light shade of color for the outlines makes the form more visible at smaller resolutions, so that the image can easily be used as an icon.
This SVG file was manually created to specify alignments, to use only integers at the core 192x192 size, to get smooth curves on connection points (without any angle), to make a perfect logo centered in a exact square, to use a more precise geometry for the star and to use slate blue color with slightly lighter outlines on the cross, the rod and snake.
Finally, the SVG file is clean and contains no unnecessary XML elements or attributes, CSS styles or transforms that are usually added silently by common SVG editors (like Sodipodi or Inkscape) and that just pollute the final document, so it just needs the core SVG elements for the rendering. This is why its file size is so small.