Kyselina azidovodíková
| Kyselina azidovodíková | |
|---|---|
 Vazebné úhly a délky azoimidu | |
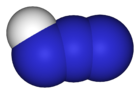 3D struktura azoimidu | |
| Obecné | |
| Systematický název | Kyselina azidovodíková |
| Ostatní názvy | Azoimid Kyselina dusíkovodíková |
| Anglický název | Hydrazoic acid |
| Německý název | Stickstoffwasserstoffsäure |
| Sumární vzorec | HN3 |
| Vzhled | Bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 7782-79-8 |
| SMILES | [N-]=[N+]=N |
| Vlastnosti | |
| Molární hmotnost | 43,029 g/mol |
| Teplota tání | −80 °C |
| Teplota varu | 35,7 °C |
| Hustota | 1,126 g/cm3 (20 °C) |
| Disociační konstanta pKa | 4,59 |
| Tlak páry | 523 hPa (20 °C) |
| Struktura | |
| Tvar molekuly | lineární |
| Dipólový moment | 2,83 Cm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | 294 kJ/mol (plyn) |
| Entalpie varu ΔHv | 697 J/g |
| Standardní molární entropie S° | 238,8 JK−1mol−1 (plyn) |
| Standardní slučovací Gibbsova energie ΔGf° | +328 kJ/mol (plyn) |
| Izobarické měrné teplo cp | 1,015 JK−1g−1 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H200, H319, H335, H370 |
| P-věty | P201, P202, P260, P261, P264, P270, P271, P280, P281, P304+340, P305+351+338, P307+311, P312, P321, P337+313, P372, P373, P380, P401, P403+233, P405, P501 |
| R-věty | R1, R2 R4 |
| S-věty | ? |
Některá data mohou pocházet z datové položky. | |
Kyselina azidovodíková neboli azoimid (dle nového názvosloví) či kyselina dusíkovodíková je jednou ze tří základních sloučenin dusíku s vodíkem (amoniak, hydrazin, azoimid). Její vzorec je HN3. V její molekule jsou na sebe vázány tři atomy dusíku. Vazby v molekule nejsou rovnocenné. Kyselina azidovodíková je bezbarvá kapalina ostrého zápachu, její bod varu je 35,7 °C, její páry jsou explozivní. Je smrtelným (i když nekumulativním) jedem; ve vzduchu může být nebezpečná i při koncentracích pod 1 ppm. Ve vodných roztocích je stálá. Je to slabá kyselina (zhruba stejně silná jako kyselina octová). Tvoří jeden typ solí – azidy. Koncentrovaná kyselina azidovodíková je velmi silnou a nebezpečnou výbušninou.
Příprava
Existují dva způsoby přípravy kyseliny azidovodíkové:
1. reakcí azidu sodného s kyselinou sírovou (tímto způsobem HN3 poprvé připravil v roce 1890 německý chemik Theodor Curtius):
- 2 NaN3 + H2SO4 → 2 HN3 + Na2SO4
2. reakcí soli hydrazinia s kyselinou dusitou:
- N2H5+ + HNO2 → HN3 + H+ + 2 H2O
Použití
Nejdůležitějším azidem je azid sodný NaN3, ze kterého se připravují ostatní azidy. Tato sloučenina je poměrně stálá, dá se bez rozkladu tavit. Využívá se pro exploze airbagů v automobilech. Azidy alkalických kovů a kovů alkalických zemin se chovají podobně, naproti tomu azidy těžkých kovů velmi snadno vybuchují (např. azid olovnatý Pb(N3)2, který se používá jako náplň do rozbušek).
Reference
- ↑ a b Hydrazoic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
Externí odkazy
 Obrázky, zvuky či videa k tématu kyselina azidovodíková na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina azidovodíková na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
Structure and dimensions of the hydrogen azide molecule, HN3.
Structural data from Greenwood, N. N.; Earnshaw, A. (1997) Chemistry of the Elements (2. ed.), Oxford:Butterworth-Heinemann ISBN: 0-7506-3365-4.Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for explosive substances







