Kyselina ferulová
| Kyselina ferulová | |
|---|---|
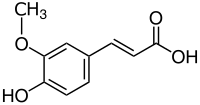 Strukturní vzorec | |
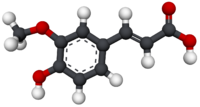 Model molekuly | |
| Obecné | |
| Systematický název | kyselina (2E)-3-(4-hydroxy-3-methoxyfenyl)prop-2-enová |
| Sumární vzorec | C10H10O4 |
| Vzhled | krystalický prášek |
| Identifikace | |
| Registrační číslo CAS | 1135-24-6 |
| EC-no (EINECS/ELINCS/NLP) | 214-490-0 |
| PubChem | 445858 |
| SMILES | COC1=C(C=CC(=C1)C=CC(=O)O)O |
| InChI | 1S/C10H10O4/c1-14-9-6-7(2-4-8(9)11)3-5-10(12)13/h2-6,11H,1H3,(H,12,13)/b5-3+ |
| Vlastnosti | |
| Molární hmotnost | 194,18 g/mol |
| Teplota tání | 174 °C (447 K)[1] |
| Disociační konstanta pKa | 4,42[1] |
| Rozpustnost ve vodě | 0,597 g/100 ml[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustná v ethanolu a ethylacetátu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustná v benzenu a diethyletheru[1] |
| Bezpečnost | |
| [1] Varování[1] | |
| H-věty | H315 H319 H335[1] |
| P-věty | P261 P264 P271 P280 P302+352 P304+340 P305+351+338 P312 P321 P332+313 P337+313 P362 P403+233 P405 P501[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Kyselina ferulová je organická sloučenina patřící mezi hydroxyskořicové kyseliny. Jedná se o fenolickou sloučeninu často přítomnou ve stěnách rostlinných buněk, kde bývá navázána na vedlejší řetězce molekul jako jsou arabinoxylany. Tato kyselina je složkou ligninu a slouží jako prekurzor při výrobě dalších aromatických sloučenin. Název je odvozen od jejího výskytu v rostlinách rodu ločidlo (Ferula).
Výskyt
Kyselina ferulová je stavebním prvkem lignocelulóz, jako jsou pektiny[2] a ligniny.
V potravinách
Kyselina ferulová se nachází v řadě druhů zeleniny, v poměrně vysokých koncentracích je přítomna v popcornu a bambusových výhoncích.[3][4] Jde, společně s kyselinou kávovou a isoferulovou, o hlavní metabolit chlorogenových kyselin u lidí a absorbována je v tenkém střevu, zatímco ostatní metabolity kyseliny chlorogenové, jako jsou kyselina dihydroferulová a feruloylglycin, se absorbují působením střevní mikroflóry v tlustém střevu.[5]
U obilovin se kyselina ferulová vyskytuje v otrubách. V pšenici jsou fenolické sloučeniny nejvíce přítomny jako kyselina ferulová vázaná na nerozpustné sloučeniny, což ovlivňuje odolnost pšenice vůči houbovým chorobám.[6] Nejvyšší koncemntrace glukosidů kyseliny ferulové byly nalezeny ve lněných semenech (4,1±0,2 g/kg).[7]
Přítomnost kyseliny ferulové byla také prokázána u zrn ječmenu.[8]
Kyselina ferulová se také vyskytuje v čaji z listu jakonu (Smallanthus sonchifolius), rostliny pěstované v severních a středních Andách. Obsahují ji rovněž fazole [9] a nachází se v semenech rostliny Macrotyloma uniflorum.
Biodostupnost kyseliny ferulové závisí na formě, ve které je přítomna: volná kyselina se špatně rozpouští ve vodě a její biodostupnost je tak nízká. V pšenici je vázána na polysacharidy v buněčné stěně, což umožňuje její uvolnění a absorpci v tenkém střevě.[10]
V léčivých rostlinách
Kyselina ferulová byla nalezena v rostlinách používaných v tradiční čínské medicíně, jako jsou andělika čínská (Angelica sinensis), Cimicifuga heracleifolia[11] a Ligusticum chuangxiong. Vyskytuje se také v čaji připraveném z zeměžluči hořké (Centaurium erythraea), používané k léčení v mnoha částech Evropy.[12]
Ve zpracovaných potravinách
Z vařené kukuřice se uvolňuje kyselina ferulová.[13]
Ve formě esterů se steroly se tato sloučenina nachází v oleji z rýžových otrub, často používaném při přípravě jídel v některých asijských zemích.[14]
Glukosid kyseliny ferulové lze nalézt v chlebech obsahujících lněná semena.[15]
Chléb z režné mouky obsahuje dehydrodimery kyseliny ferulové.[16]
Metabolismus
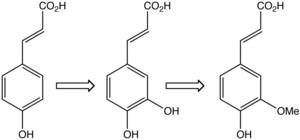
Biosyntéza
Kyselina ferulová se v rostlinách tvoří z kyseliny kávové působením enzymu kafeát O-methyltransferázy.[17]
Kyselina ferulová je, společně s kyselinou dihydroferulovou, součástí lignocelulózy, kde propojuje lignin s polysacharidy, čímž zajišťuje pevnost buněčných stěn.[18]
Jedná se o meziprodukt syntézy monolignolů, monomerů lignin, a také o prekurzor lignanů.
Biodegradace
Některé druhy kvasinek, jako jsou druhy využívané při výrobě pšeničných piv, například Saccharomyces delbrueckii (Torulaspora delbrueckii), přeměňují kyselinu ferulovou na 4-vinyl guajakol (2-methoxy-4-vinylfenol), který těmto pivům dodává typické hřebíčkovité aroma. Saccharomyces cerevisiae (pivařské kvasnice) a Pseudomonas fluorescens také mohou měnit kyselinu trans-ferulovou na 2-methoxy-4-vinylfenol.[19] U P. fluorescens se podařilo izolovat dekarboxylázu kyseliny ferulové.[20]
Ekologický význam
Kyselina ferulová je jednou z látek iniciujících virulenci bakterie Agrobacterium tumefaciens, a tak ji umožňuje napadat buňky rostlin.[21]
Extrakce
Kyselinu ferulovou lze extrahovat z pšeničných a kukuřičných otrub pomocí koncentrovaných zásad.[22]

Použití v hmotnostní spektrometrii
Kyselina ferulová slouží jako matrice při analýze bílkovin metodou MALDI.[23]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Ferulic acid na anglické Wikipedii.
- ↑ a b c d e f g h i Ferulic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Luc Saulnier; Jean-François Thibault. Ferulic acid and diferulic acids as components of sugar-beet pectins and maize bran heteroxylans. Journal of the Science of Food and Agriculture. 1999-03-01, s. 396–402. DOI 10.1002/(SICI)1097-0010(19990301)79:3<396::AID-JSFA262>3.0.CO;2-B.
- ↑ Zhaohui Zhao; Mohammed H. Moghadasian. Chemistry, natural sources, dietary intake and pharmacokinetic properties of ferulic acid: A review. Food Chemistry. 2008, s. 691–702. DOI 10.1016/j.foodchem.2008.02.039. PMID 26049981.
- ↑ Naresh Kumar; Vikas Pruthi. Potential applications of ferulic acid from natural sources. Biotechnology Reports. 2014, s. 86–93. DOI 10.1016/j.btre.2014.09.002. PMID 28626667.
- ↑ Debasis Bagchi; Hiroyoshi Moriyama; Anand Swaroop. Green Coffee Bean Extract in Human Health. [s.l.]: CRC Press, 2016. ISBN 9781315353982. S. 92.
- ↑ Pierre Gelinas; Carole M. McKinnon. Effect of wheat variety, farming site, and bread-baking on total phenolics. International Journal of Food Science and Technology. 2006, s. 326–332. DOI 10.1111/j.1365-2621.2005.01057.x.
- ↑ Vickram Beejmohun; Ophélie Fliniaux. Microwave-assisted extraction of the main phenolic compounds in flaxseed. Phytochemical Analysis. 2007, s. 275–285. DOI 10.1002/pca.973. PMID 17623361.
- ↑ Zory Quinde-Axtell; Byung-Kee Baik. Phenolic Compounds of Barley Grain and Their Implication in Food Product Discoloration. Journal of Agricultural and Food Chemistry. 2006, s. 9978–9984. DOI 10.1021/jf060974w. PMID 17177530.
- ↑ Devanand L. Luthria; Marcial A. Pastor-Corrales. Phenolic acids content of fifteen dry edible bean (Phaseolus vulgaris L.) varieties. Journal of Food Composition and Analysis. 2006, s. 205–211. DOI 10.1016/j.jfca.2005.09.003.
- ↑ Nuria Mateo Anson; Robin van den Berg; Aalt Bast; Guido R. M. M. Haenen. Bioavailability of ferulic acid is determined by its bioaccessibility. Journal of Cereal Science. 2009, s. 296–300. DOI 10.1016/j.jcs.2008.12.001.
- ↑ S. Sakai; H. Kawamata; T. Kogure; N. Mantani; K. Terasawa; M. Umatake; H. Ochiai. Inhibitory effect of ferulic acid and isoferulic acid on the production of macrophage inflammatory protein-2 in response to respiratory syncytial virus infection in RAW264.7 cells. Mediators of Inflammation. 1999, s. 173–175. DOI 10.1080/09629359990513. PMID 10704056.
- ↑ P. Valentão; E. Fernandes; F. Carvalho; P. R. Andrade; R. M. Seabra; M. L. Bastos. Antioxidant Activity of Centaurium erythraea Infusion Evidenced by Its Superoxide Radical Scavenging and Xanthine Oxidase Inhibitory Activity. Journal of Agricultural and Food Chemistry. 2001, s. 3476–3479. DOI 10.1021/jf001145s. PMID 11453794.
- ↑ Cooking sweet corn boosts its ability to fight cancer and heart disease by freeing healthful compounds, Cornell scientists find [online]. Cornell News [cit. 2009-09-07]. Dostupné online.
- ↑ Bailey's Industrial Oil and Fat Products. [s.l.]: John Wiley & Sons, 2005. ISBN 978-0-471-38552-3. Kapitola Chapter 10: Rice Bran Oil, s. 465.
- ↑ C. Strandås; A. Kamal-Eldin; R. Andersson; P. Åman. Phenolic glucosides in bread containing flaxseed. Journal of Agricultural and Food Chemistry. 2008, s. 997–999. DOI 10.1016/j.foodchem.2008.02.088. PMID 26047292.
- ↑ BOSKOV HANSEN, H.; ANDREASEN, M.; NIELSEN, M.; LARSEN, L.; KNUDSEN, Bach K.; MEYER, A.; CHRISTENSEN, L. Changes in dietary fibre, phenolic acids and activity of endogenous enzymes during rye bread-making. European Food Research and Technology. 2014, s. 33–42. ISSN 1438-2377. DOI 10.1007/s00217-001-0417-6. (anglicky)
- ↑ Fereidoon Shahadi; Marian Naczk. Phenolics in Food and Nutraceuticals. Florida: CRC Press, 2004. Dostupné online. ISBN 978-1-58716-138-4. S. 4.
- ↑ K. Iiyama; T. B.-T. Lam; B. A. Stone. Covalent Cross-Links in the Cell Wall. Plant Physiology. 1994, s. 315–320. ISSN 0032-0889. DOI 10.1104/pp.104.2.315. PMID 12232082.
- ↑ Z. Huang; L. Dostal; J. P. Rosazza. Microbial transformations of ferulic acid by Saccharomyces cerevisiae and Pseudomonas fluorescens. Applied and Environmental Microbiology. 1993, s. 2244–2250. DOI 10.1128/AEM.59.7.2244-2250.1993. PMID 8395165.
- ↑ Z. Huang; L. Dostal; J. P. Rosazza. Purification and characterization of a ferulic acid decarboxylase from Pseudomonas fluorescens. Journal of Bacteriology. 1994, s. 5912–5918. DOI 10.1128/jb.176.19.5912-5918.1994. PMID 7928951.
- ↑ Virginia S. Kalogeraki; Jun Zhu; Anatol Eberhard; Eugene L. Madsen; Stephen C. Winans. The phenolic vir gene inducer ferulic acid is O-demethylated by the VirH2 protein of an Agrobacterium tumefaciens Ti plasmid. Molecular Microbiology. 1999, s. 512–522. DOI 10.1046/j.1365-2958.1999.01617.x. PMID 10564493.
- ↑ Anvar U. Buranov; G. Mazza. Extraction and purification of ferulic acid from flax shives, wheat and corn bran by alkaline hydrolysis and pressurised solvents. Food Chemistry. 2009, s. 1542–1548. DOI 10.1016/j.foodchem.2009.01.059.
- ↑ R. C. Beavis; B. T. Chait; H. M. Fales. Cinnamic acid derivatives as matrices for ultraviolet laser desorption mass spectrometry of proteins. Rapid Communications in Mass Spectrometry. 1989, s. 432–435. DOI 10.1002/rcm.1290031207. PMID 2520223. Bibcode 1989RCMS....3..432B.
Související články
- Kyselina kumarová
- Diferulové kyseliny
- Eugenol
Externí odkazy
 Obrázky, zvuky či videa k tématu Kyselina ferulová na Wikimedia Commons
Obrázky, zvuky či videa k tématu Kyselina ferulová na Wikimedia Commons - TOMARO-DUCHESNEAU, Catherine; SAHA, Shyamali; MALHOTRA, Meenakshi; COUSSA-CHARLEY, Michael; KAHOULI, Imen; JONES, Mitchell L.; LABBE, Alain. Probiotic Ferulic Acid Esterase Active Lactobacillus fermentum NCIMB 5221 APA Microcapsules for Oral Delivery: Preparation and In Vitro Characterization. Pharmaceuticals. 2012, s. 236–248. DOI 10.3390/ph5020236. PMID 24288090. (anglicky)
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
structure of caffeic acid as an intermediate
Chemical structure of ferulic acid.
Autor: Manuel Almagro Rivas, Licence: CC BY-SA 4.0
3D ball-and-stick model of a ferulic acid molecule.





