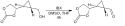Kyselina jodoxybenzoová
| Kyselina jodoxybenzoová | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | 1-hydroxy-1λ5,2-benziodoxol-1,3-dion |
| Ostatní názvy | kyselina 2-jodoxybenzoová, 1-hydroxy-1λ3,2-benziodoxol-3(1H)-on-1-oxid, IBX |
| Sumární vzorec | C7H5IO4 |
| Identifikace | |
| Registrační číslo CAS | 61717-82-6 |
| EC-no (EINECS/ELINCS/NLP) | 629-407-7 |
| PubChem | 339496 |
| ChEBI | 52701 |
| SMILES | O=C1OI(=O)(O)c2ccccc12 |
| InChI | 1S/C7H5IO4/c9-7-5-3-1-2-4-6(5)8(10,11)12-7/h1-4H,(H,10,11) |
| Vlastnosti | |
| Molární hmotnost | 280,02 g/mol |
| Teplota rozkladu | 233 °C (506 K) |
| Bezpečnost | |
| [1] | |
| H-věty | H314 H315 H319 H335[1] |
| P-věty | P260 P261 P264 P265 P271 P280 P301+330+331 P302+352 P304+340 P305+351+338 P321 P363 P403+233 P405 P501[1] |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Kyselina jodoxybenzoová (zkráceně IBX) je organická sloučenina používaná v organické syntéze jako oxidační činidlo. Používá se na oxidace alkoholů na aldehydy. IBX se připravuje z kyseliny 2-jodbenzoové, bromičnanu draselného a kyseliny sírové.[2] Bromičnan draselný lze nahradit lépe dostupným hydrogenperoxosíranem.[3]
Nevýhodou této sloučeniny je její špatná rozpustnost; IBX je ve většině běžných organických rozpouštědel nerozpustná. V minulosti byla IBX považována za citlivou na náraz, ovšem zjistilo se, že tato citlivost vzorků IBX byla pravděpodobně způsobena zbytky bromičnanu draselného z její přípravy.[3][4]
Komerčně prodávané vzorky IBX jsou stabilizovány karboxylovými kyselinami. například benzoovou nebo isoftalovou.
Mechanismus oxidací
Reakční mechanismus oxidace alkoholu na aldehyd, jak bylo zjištěno metodami výpočetní chemie začíná výměnou ligandů,[5] kdy se odštěpí hydroxylová skupina z alkoholu, poté proběhne eliminace. Úvodní krok je nutný, protože dvojná vazba mezi jodem a kyslíkem je mimo rovinu alkoxy skupiny a soustředěná eliminace tak neprobíhá. Dochází v něm k přesmyku, kdy se atom kyslíku přemístí do správné polohy a eliminací se poté utvoří pětičlenný cyklický meziprodukt; tato část určuje rychlost reakce. Tímto mechanismem lze vysvětlit, proč oxidace probíhá rychleji u alkoholů s většími molekulami než u menších. Jeho hnací silou jsou sterické efekty vyvolané ortho-vodíkem a protony z alkoxyskupiny, u větších alkoxyskupin je sterické odpuzování větší. Podle stejných výpočtů reaguje přibližně 100krát rychleji derivát IBX s ortho-vodíkem nahrazeným methylovou skupinou.

IBX se vyskytuje jako směs dvou tautomerů, kde jeden z nich má podobu karboxylové kyseliny. Kyselost IBX, jež byla změřena ve vodném roztoku (pKa 2,4) a dimethylsulfoxidu (pKa 6,65),[6] má na reakce významný vliv, což se projevuje například u kysele katalyzovaných izomerizací zahrnujících oxidace.
Rozsah
Kyselina jodoxybenzoová je také dostupná jako navázaná na silikagel nebo polystyren. V mnoha případech se nahrazuje Dessovým–Martinovým perjodinanem, lépe rozpustným v obvyklých organických rozpouštědlech. Jako příklad reakce může sloužit oxidace pomocí této kyseliny zahrnutá do totální syntézy eikosanoidů:[7]
J. D. More a N. S. Finney[8] a S. Van Arman[9] ukázali, že pro řadu oxidací za použití IBX jsou, i přes nízkou rozpouštěcí schopnost, vhodná mnohá běžná rozpouštědla; produkt se pak i mnohdy snadněji přečišťuje.
V roce 2001 K. C. Nicolaou se svými spolupracovníky vydal několik článků popisujících, kromě jiných přeměn, použití IBX k oxidaci primárních benzylových uhlíků na aromatické aldehydy a sekundárních na ketony.[10]
Oxidační štěpení
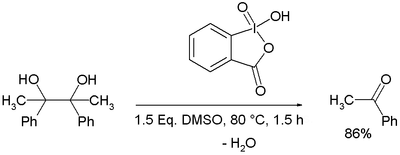
IBX oxiduje vicinální dioly na diketony aniž by docházelo ke štěpením vazeb uhlík–uhlík,[11] oxidační štěpení glykolů na dva aldehydy lze ovšem provést při změněných podmínkách (vyšších teplotách nebo použití kyseliny trifluoroctové jako rozpouštědla).[12]
Mechanismus tohoto glykolového štěpení začíná tvorbou aduktu 10-I-4 IBX a DMSO za vzniku 12-I-5 meziproduktu, 3, v němž DMSO vytváří odstupující skupinu pro alkohol 4, čímž vznikne meziprodukt 5. Působením jednoho ekvivalentu vody se utvoří 12-I-5 spirobicyklický perjodinan 6, který se fragmentuje na 7. Za přítomnosti hydroxylových alfa protonů se objevuje vedlejší reakce v podobě oxidace na acyloin.
α-hydroxylace
S. F. Kirsch se spolupracovníky provedl hydroxylace ketonů kyselinou jodoxybenzoovou do poloh α za mírných podmínek.[13]
Tento postup lze použít i na β-ketoestery.[14]
Oxidace β-hydroxyketonů na β-diketony
S. L. Bartlett a C. M. Beaudry zjistili, že IBX je užitečná pro převody β-hydroxyketonů na β-diketony. IBX poskytuje lepší výtěžnosti než Swernův i Dessův–Martinův postup.[15]
Reference
V tomto článku byl použit překlad textu z článku 2-Iodoxybenzoic acid na anglické Wikipedii.
- ↑ a b c https://pubchem.ncbi.nlm.nih.gov/compound/339496
- ↑ BOECKMAN, R. K.; SHAO, P.; MULLINS, J. J. Dess–Martin periodinane: 1,1,1-Triacetoxy-1,1-dihydro-1,2-benziodoxol-3(1H)-one. Org. Synth.. 2000, s. 141. Dostupné online. (anglicky); Coll. Vol.. S. 696. (anglicky)
- ↑ a b M. Frigerio; M. Santagostino; S. Sputore. A User-Friendly Entry to 2-Iodoxybenzoic Acid (IBX). Journal of Organic Chemistry. 1999, s. 4537–4538. DOI 10.1021/jo9824596.
- ↑ D. B. Dess; J. C. Martin. A Useful 12-I-5 Triacetoxyperiodinane (the Dess–Martin Periodinane) for the Selective Oxidation of Primary or Secondary Alcohols and a Variety of Related 12-I-5 Species. Journal of the American Chemical Society. 1991, s. 7277–7287. DOI 10.1021/ja00019a027.
- ↑ J. T. Su; W. A. Goddard. Enhancing 2-Iodoxybenzoic Acid Reactivity by Exploiting a Hypervalent Twist. Journal of the American Chemical Society. 2005, s. 1414–14147. Dostupné online. DOI 10.1021/ja054446x. PMID 16218584.
- ↑ M. J. Gallen; R. Goumont; T. Clark; F. Terrier; C. M. Williams. o-Iodoxybenzoic Acid (IBX): pKa and Proton-Affinity Analysis. Angewandte Chemie International Edition. 2006, s. 2929–2934. DOI 10.1002/anie.200504156. PMID 16566050.
- ↑ D. K. Mohapatra; G. S. Yellol. Asymmetric Total Synthesis of Eicosanoid. Arkivoc. 2005, s. 144–155. DOI 10.3998/ark.5550190.0006.316.
- ↑ J. D. More; N. S. Finney. A Simple and Advantageous Protocol for the Oxidation of Alcohols with o-Iodoxybenzoic Acid (IBX). Organic Letters. 2002, s. 3001–3003. DOI 10.1021/ol026427n. PMID 12182609.
- ↑ S. Van Arman. 2-Methyl-2-propanol as solvent for o-iodoxybenzoic acid (IBX) oxidation of 1˚ alcohols to aldehydes. Tetrahedron Letters. 2009, s. 4693–4695. DOI 10.1016/j.tetlet.2009.06.045.
- ↑ K. C. Nicolaou; T. Montagnon; P. S. Baran; Y.-L. Zhong. Iodine(V) Reagents in Organic Synthesis. Part 4. o-Iodoxybenzoic Acid as a Chemospecific Tool for Single Electron Transfer-Based Oxidation Processes. Journal of the American Chemical Society. 2002-03-01, s. 2245–2258. ISSN 0002-7863. DOI 10.1021/ja012127+. PMID 11878978.
- ↑ M. Frigerio; M. Santagostino. A Mild Oxidizing Reagent for Alcohols and 1,2-Diols: o-Iodoxybenzoic Acid (IBX) in DMSO. Tetrahedron Letters. 1994, s. 8019–8022. DOI 10.1016/0040-4039(94)80038-3.
- ↑ J. N. Moorthy; N. Singhal; K. Senapati. Oxidative Cleavage of Vicinal Diols: IBX can do what Dess–Martin Periodinane (DMP) can. Organic & Biomolecular Chemistry. 2007, s. 767–771. DOI 10.1039/b618135j. PMID 17315062.
- ↑ S. F. Kirsch. IBX-Mediated α-Hydroxylation of α-Alkynyl Carbonyl Systems. A Convenient Method for the Synthesis of Tertiary Alcohols. Journal of Organic Chemistry. 2005, s. 10210-10212. DOI 10.1021/jo051898j. PMID 16292876.
- ↑ S. F. Kirsch; A. Duschek. Novel Oxygenations with IBX. Chemistry: A European Journal. 2009, s. 10713-10717. DOI 10.1002/chem.200901867. PMID 19760735.
- ↑ S. L. Bartlett; C. M. Beaudry. High Yielding Oxidation of β-Hydroxyketones to β-Diketones Using o-Iodoxybenzoic Acid.Chybí název periodika! 2011, s. 9852–9855. DOI 10.1021/jo201810c. PMID 22023037.
Externí odkazy
 Obrázky, zvuky či videa k tématu Kyselina jodoxybenzoová na Wikimedia Commons
Obrázky, zvuky či videa k tématu Kyselina jodoxybenzoová na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Ball-and-stick model of the 2-iodoxybenzoic acid molecule, C7H5IO4, as found in the crystal structure.
Colour code:
- Carbon, C: grey-black
- Hydrogen, H: white
- Iodine, I: purple
- Oxygen, O: red
Structure (determined by X-ray crystallography) from J. Chem. Soc., Perkin Trans. 2 (1997) 589–592.
Model manipulated in CrystalMaker 8.5.
Image generated in Accelrys DS Visualizer.An example of oxidation of alcohol to aldehyde with IBX
(c) V8rik at the English Wikipedia, CC-BY-SA-3.0
IBX_DMSO_oxidative_cleavage
Structure of the IBX-Oxidation