Kyselina krotonová
| Krotonová kyselina | |
|---|---|
 | |
| Obecné | |
| Systematický název | (2E)-but-2-enová kyselina |
| Triviální název | kyselina krotonová |
| Latinský název | acidum crotonicum |
| Anglický název | crotonic acid |
| Německý název | Crotonsäure |
| Sumární vzorec | C₄H₆O₂ |
| Identifikace | |
| Registrační číslo CAS | 107-93-7 |
| Vlastnosti | |
| Molární hmotnost | 86,037 Da |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Kyselina krotonová (kyselina trans-but-2-enová) je nenasycená karboxylová kyselina se vzorcem CH3CH=CHCOOH. Název kyselina krotonová získala díky tomu, že byla mylně považována za produkt zmýdelnění krotonového oleje.[2] Je to bezbarvá krystalická látka charakteristického zápachu, podobného kyselině máselné. Cis- izomer kyseliny krotonové se nazývá izokrotonová kyselina. Kyselina krotonová je rozpustná ve vodě a v mnoha organických rozpouštědlech.
Výroba
Kyselinu krotonovou lze získat několika způsoby:
- Knoevenagelovou kondenzací acetaldehydu s kyselinou malonovou v pyridinu.[3]
- alkalickou hydrolýzou allylkyanidu po intramolekulárním přesmyku dvojné vazby:[4]
- Dehydratací kyseliny 3-hydroxymáselné:[5]
Vlastnosti
Kyselina krotonová krystalizuje v monoklinické soustavě v prostorové grupě P21/a s mřížkovými parametry a = 971 pm, b = 690 pm, c = 775 pm a β = 104.0°.[6]
Reaktivita
Krotonovou kyselinu lze redukovat na máselnou hydrogenací nebo redukcí zinkem a kyselinou sírovou.[7]
S chlorem nebo bromem reaguje za vzniku 2,3-dihalobutanové kyseliny:[7]
Adicí bromovodíku vzniká 3-brommáselná kyselina.[7][8]
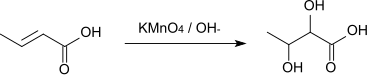
Reakcí s alkalickým roztokem manganistanu draselného vzniká 2,3-dihydroxymáselná kyselina.[7]
Reakcí s alkoholy za přítomnosti kyselého katalyzátoru vznikají estery.
Kyselina krotonová reaguje s kyselinou chlornou za vzniku 2-chlor-3-hydroxymáselné kyseliny. Ta může být redukována sodným amalgámem na kyselinu máselnou, dehydratována pomocí kyseliny sírové na 2-chlorbutenovou kyselinu, reagovat s chlorovodíkem za vzniku 2,3-dichlorbutenové kyseliny nebo s ethoxidem draselným za vzniku 3-methyloxiran-2-karboxylové kyseliny:[5]
Kyselina krotonová reaguje s amoniakem v poloze alfa v přítomnosti octanu rtuťnatého. Tato reakce poskytuje DL-threonin.[9]
Využití
Kyselina krotonová se používá hlavně jako komonomer s vinylacetátem. Výsledné kopolymery se používají v barvách a lepidlech.[10]
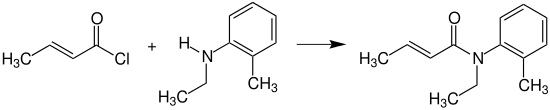
Chlorid krotonové kyseliny reaguje s N-ethyl-2-methylanilinem (N- ethyl-o-toluidinem) za vzniku krotamitonu, který se používá jako prostředek proti svrabu.[11]
Bezpečnost
LD50 krotonové kyseliny je 1 g/kg.[10] Dráždí oči, kůži a dýchací systém.
Reference
V tomto článku byl použit překlad textu z článku Crotonic acid na anglické Wikipedii.
- ↑ a b Crotonic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Crotonic acid | chemical compound. Encyclopedia Britannica [online]. [cit. 2020-12-07]. Dostupné online. (anglicky)
- ↑ a b BEYER, HANS 1905-1971. Lehrbuch der organischen Chemie. 20., überarb. u. erg. Aufl. vyd. Stuttgart: [s.n.] XVI, 954 S s. Dostupné online. ISBN 978-3-7776-0406-0, ISBN 3-7776-0406-2. OCLC 310841763
- ↑ RINNE, A.; TOLLENS, B. VIII. Ueber das Allylcyanür oder Crotonitril. Justus Liebigs Annalen der Chemie. 1871, roč. 159, čís. 1, s. 105–109. Dostupné online [cit. 2020-12-07]. ISSN 1099-0690. DOI 10.1002/jlac.18711590110. (anglicky) Archivováno 11. 3. 2021 na Wayback Machine.
- ↑ a b BEILSTEIN, Friedrich Konrad. Handbuch der organischen Chemie. [s.l.]: Hamburg ; Leipzig : L. Voss 1640 s. Dostupné online.
- ↑ SHIMIZU, Shozo; KEKKA, Shinji; KASHINO, Setsuo. Topochemical Studies. III. The Crystal and Molecular Structures of Crotonic Acid, CH3CH=CHCOOH, and Crotonamide, CH3CH=CHCONH2. Bulletin of the Chemical Society of Japan. 1974-07-01, roč. 47, čís. 7, s. 1627–1631. Dostupné online [cit. 2020-12-07]. ISSN 0009-2673. DOI 10.1246/bcsj.47.1627.
- ↑ a b c d SIR IAN HEILBRON. Dictionary Of Organic Compounds Volume One Abadole Cytosine. [s.l.]: Oxford University Press 682 s. Dostupné online.
- ↑ LOVÉN, J. M.; JOHANSSON, Hjalmar. Einige schwefelhaltige β-Substitutionsderivate der Buttersäure. Berichte der deutschen chemischen Gesellschaft. 1915, roč. 48, čís. 2, s. 1254–1262. Dostupné online [cit. 2020-12-07]. ISSN 1099-0682. DOI 10.1002/cber.19150480205. (anglicky) Archivováno 11. 3. 2021 na Wayback Machine.
- ↑ CARTER, H. E.; WEST, H. D. dl-Threonine. Org. Synth.. 1955. Dostupné online. (anglicky); Coll. Vol.. S. 813. (anglicky)
- ↑ a b SCHULZ, Rolf P.; BLUMENSTEIN, Jürgen; KOHLPAINTNER, Christian. Crotonaldehyde and Crotonic Acid. [s.l.]: Wiley‐VCH Verlag GmbH & Co. KGaA. Dostupné online. ISBN 978-3-527-30673-2. DOI 10.1002/14356007.a08_083. (anglicky) DOI: 10.1002/14356007.a08_083.
- ↑ KLEEMANN, AXEL. Pharmazeutische Wirkstoffe : Synthesen, Patente, Anwendungen. 2., neubearbeitete und erw. Aufl. vyd. Stuttgart: Thieme xxvi, 1040 pages s. Dostupné online. ISBN 3-13-558402-X, ISBN 978-3-13-558402-7. OCLC 9564549
Externí odkazy
 Obrázky, zvuky či videa k tématu Krotonová kyselina na Wikimedia Commons
Obrázky, zvuky či videa k tématu Krotonová kyselina na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Autor: MegaByte07, Licence: CC BY-SA 3.0
Reaktion von Crotonsäure mit alkalischer Permanganatlösung
Autor: MegaByte07, Licence: CC BY-SA 3.0
Oxidation von Crotonaldehyd
Autor: MegaByte07, Licence: CC BY-SA 3.0
Veresterung von Crotonsäure mit Ethanol