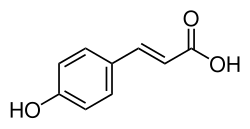
Kyselina p-kumarová
| Kyselina p-kumarová | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | (2E)-3-(4-hydroxyfenyl)prop-2-enová kyselina |
| Anglický název | p-Coumaric acid |
| Sumární vzorec | C9H8O3 |
| Vzhled | krystalická pevná látka |
| Identifikace | |
| Registrační číslo CAS | 501-98-4 |
| EC-no (EINECS/ELINCS/NLP) | 231-000-0 |
| PubChem | 637542 |
| ChEBI | 32374 |
| SMILES | C1=CC(=CC=C1\C=C\C(=O)O)O |
| InChI | InChI=1S/C9H8O3/c10-8-4-1-7(2-5-8)3-6-9(11)12/h1-6,10H,(H,11,12)/b6-3+ |
| Vlastnosti | |
| Molární hmotnost | 164,16 g/mol |
| Teplota tání | 210–213 °C (483–486 K) |
| Rozpustnost ve vodě | slabě rozpustná |
| Rozpustnost v polárních rozpouštědlech | rozpustná v ethanolu |
| Rozpustnost v nepolárních rozpouštědlech | rozpustná v diethyletheru |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R36/37/38 |
| S-věty | S24/25 |
Některá data mohou pocházet z datové položky. | |
Kyselina p-kumarová ([parakumarová]) je organická sloučenina, hydroxyderivát kyseliny skořicové. Je jedním z izomerů kyseliny kumarové společně s kyselinou o-kumarovou a m-kumarovou, které se liší pozicí hydroxylové skupiny na benzenovém jádru. p-Kumarová kyselina je ze všech tří izomerů v přírodě nejrozšířenější, existuje jako cis- a trans-izomer.
Výskyt
Kyselina p-kumarová se nachází v liáně Gnetum cleistostachyum.
V potravinách
Kyselinu p-kumarovou lze nalézt v nejrůznějších jedlých rostlinách jako jsou podzemnice olejná, rajče jedlé, mrkev obecná, bazalka a česnek. Vyskytuje se rovněž ve vínu, v octu.[2] a v zrnech ječmene.[3]
Kyselina p-kumarová se také nachází v pylu, odkud se dostává do medu.[4]
Deriváty
Glykosidy kyseliny p-kumarové se dají nalézt v chlebech obsahujících lněná semena.[5]
Diestery kyseliny p-kumarové jsou součástí karnaubského vosku.
Biosyntéza
Kyselina p-kumarová je vytvářena z kyseliny skořicové působením P450-závislého enzymu trans-cinnamát 4-monooxygenázy (C4H):
Také vzniká z L-tyrosinu působením tyrosinové amoniaklyázy:

 + NH3 + H+
+ NH3 + H+
Biochemie
Kyselina p-kumarová je prekurzorem 4-ethylfenolu, který vytváří kvasinky Brettanomyces ve víně. Nejprve dojde k přeměně kyseliny na 4-vinylfenol za katalýzy enzymem cinamátdekarboxylázou.[6] 4-vinylfenol je následně působením vinylfenolreduktázy redukován na 4-ethylfenol.

Enzym cis-p-kumarát glukosyltransferáza využívá UDP-glukózu a cis-p-kumarát k tvorbě 4′-O-β-D-glukosyl-cis-p-kumarátu a UDP. Tento enzym patří mezi glykosyltransferázy, přesněji mezi hexosyltransferázy.[7]
V bachoru ovcí, které byly krmeny senem, se vyskytuje kyselina floretová, jež vzniká hydrogenací 2-propenového postranního řetězce kyseliny p-kumarové.[8]
Reference
V tomto článku byl použit překlad textu z článku p-Coumaric acid na anglické Wikipedii.
- ↑ a b 4-Hydroxycinnamic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ CARRERO GÁLVEZ, Miguel; GARCÍA BARROSO, Carmelo; PÉREZ-BUSTAMANTE, Juan Antonio. Analysis of polyphenolic compounds of different vinegar samples. Zeitschrift für Lebensmittel-Untersuchung und -Forschung. 1994, s. 29–31. doi:10.1007/BF01192948.
- ↑ QUINDE-AXTELL, Zory; BAIK, Byung-Kee. Phenolic Compounds of Barley Grain and Their Implication in Food Product Discoloration. Journal of Agricultural and Food Chemistry. 2006, s. 9978–9984. doi:10.1021/jf060974w. PMID 17177530.
- ↑ MAO, W.; SCHULER, M. A.; BERENBAUM, M. R. Honey constituents up-regulate detoxification and immunity genes in the western honey bee Apis mellifera. Proceedings of the National Academy of Sciences of the United States of America. 2013, s. 8842–6. doi:10.1073/pnas.1303884110. PMID 23630255.
- ↑ STRANDÅS, C.; KAMAL-ELDIN, A.; ANDERSSON, R.; ÅMAN, P. Phenolic glucosides in bread containing flaxseed. Food Chemistry. 2008, s. 997–999. doi:10.1016/j.foodchem.2008.02.088.
- ↑ Brettanomyces Monitoring by Analysis of 4-ethylphenol and 4-ethylguaiacol [online]. [cit. 2017-11-07]. Dostupné v archivu pořízeném dne 2008-02-19.
- ↑ RASMUSSEN, Susanne; RUDOLPH, Hansjörg. Isolation, purification and characterization of UDP-glucose: cis-p-coumaric acid-β-D-glucosyltransferase from sphagnum fallax. Phytochemistry. 1997, s. 449–453. doi:10.1016/S0031-9422(97)00337-3.
- ↑ CHESSON, A.; STEWART, C. S.; WALLACE, R. J. Influence of plant phenolic acids on growth and cellulolytic activity of rumen bacteria. Applied and Environmental Microbiology. 1982, s. 597–603. PMID 16346090.
Externí odkazy
 Obrázky, zvuky či videa k tématu kyselina p-kumarová na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina p-kumarová na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Chemical structure of p-coumaric acid.
Structure of Cinnamic acid
Ball-and-stick model of the coumaric acid molecule, a phenylpropanoid of the cinnamic acid class.
Structure of L-tyrosin
Chemical diagram showing the biosynthesis of 4-ethylphenol. p-Coumaric acid is converted by the enzyme cinnamate decarboxylase to 4-vinylphenol (4-hydroxystyrene). 4-Vinyl phenol reduced by vinyl phenol reductase to give 4-ethylphenol.