Kyselina trifluoroctová
| Kyselina trifluoroctová | |
|---|---|
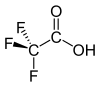 Strukturní vzorec | |
 Molekula | |
| Obecné | |
| Systematický název | trifluorethanová kyselina |
| Ostatní názvy | TFA |
| Funkční vzorec | CF3COOH |
| Sumární vzorec | C2HF3O2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 76-05-1 |
| EC-no (EINECS/ELINCS/NLP) | 200-929-3 |
| Indexové číslo | 607-091-00-1 |
| SMILES | FC(F)(F)C(O)=O |
| Vlastnosti | |
| Molární hmotnost | 114,03 g/mol |
| Teplota tání | −15,4 °C |
| Teplota varu | 72,4 °C |
| Hustota | 1,535 1 g/cm³ (20 °C) |
| Disociační konstanta pKa | 0,3 |
| Rozpustnost ve vodě | mísitelná |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R20 R35 R52/53 |
| S-věty | (S1/2) S9 S26 S27 S28 S45 S61 |
Některá data mohou pocházet z datové položky. | |
Kyselina trifluoroctová (TFA) je chemická sloučenina s chemickým vzorcem CF3CO2H. K této karboxylové kyselině jsou navázány tři velmi elektronegativní atomy fluoru. Kyselina je derivátem od kyseliny octové, je přitom téměř stotisíckrát kyselejší. Kyselina je široce používána v organické chemii.[2]
Odkazy
Reference
- ↑ a b Trifluoroacetic acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ LÓPEZ, Simón E.; SALAZAR, José. Trifluoroacetic acid: Uses and recent applications in organic synthesis. Journal of Fluorine Chemistry. Roč. 156, s. 73–100. Dostupné online [cit. 2017-10-20]. DOI 10.1016/j.jfluchem.2013.09.004.
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu kyselina trifluoroctová na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyselina trifluoroctová na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Structure of Trifluoroacetic acid, Perfluoroacetic acid, Trifluoracetic acid, Trifluoroethanoic acid; Perfluoroacetic acid





