Kyslík
| Kyslík | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ↓ Periodická tabulka ↓ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obecné | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Název, značka, číslo | Kyslík, O, 8 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cizojazyčné názvy | lat. oxygenium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina, perioda, blok | 16. skupina, 2. perioda, blok p | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemická skupina | Nekovy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Koncentrace v zemské kůře | 480000 ppm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Koncentrace v mořské vodě | 857 000 mg/l | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | Bezbarvý plyn | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Registrační číslo CAS | 7782-44-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relativní atomová hmotnost | 15,9994 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomový poloměr | 60 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentní poloměr | 66 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsův poloměr | 152 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronová konfigurace | [He] 2s2 2p4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační čísla | −II, −I, +II | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativita (Paulingova stupnice) | 3,44 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizační energie | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| První | 1313,9 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Druhá | 3388,3 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Třetí | 5300,5 KJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Látkové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografická soustava | Krychlová | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární objem | 17,36×10−6 m3/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mechanické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hustota | 1,429 kg/m3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenství | Plynné | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak syté páry | 1000 Pa při 61K | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku | 330 m/s | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 0,02658 W⋅m−1⋅K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termodynamické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota tání | −218,79 °C (54,36 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota varu | −182,95 °C (90,2 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo tání | 0,444 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo varu | 6,82 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Měrná tepelná kapacita | 29,378 Jmol−1K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektromagnetické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Standardní elektrodový potenciál | 1,23 V | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetické chování | Paramagnetický | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bezpečnost | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [1] Nebezpečí[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| R-věty | R8 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S-věty | S2, S17 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Kyslík (chemická značka O, latinsky oxygenium) je plynný chemický prvek, tvořící druhou hlavní složku zemské atmosféry. Je biogenním prvkem a jeho přítomnost je nezbytná pro existenci většiny živých organismů na této planetě. Autorem jeho českého názvu je Jan Svatopluk Presl.[2] Při dýchání vzduchu o obsahu kyslíku větším než 75 % (za normálního atmosférického tlaku) však dochází k většinou nenávratnému poškození plic.
Alotropie kyslíku
Kyslík vytváří řadu alotropických modifikací:
- volné kyslíkové radikály
- dikyslík – nejobvyklejší plynná forma kyslíku, O2
- trikyslík (neboli ozon)
- pevný kyslík
Izotopy kyslíku
Kyslík má tři stabilní izotopy 16O, 17O a 18O, bylo však popsáno i několik radioizotopů.
Historie výzkumu kyslíku
Jeden z prvních známých experimentů zkoumajících vztah mezi spalováním a vzduchem popsal ve 3. století před naším letopočtem řecký učenec Filón Byzantský. Pozoroval, že po převrácení nádoby přes hořící svíčku a obklopení hrdla nádoby vodou začne voda stoupat. Nesprávně předpokládal, že část vzduchu v nádobě mohla uniknout póry ve skle. Až o mnoho století později, v 15. století, zkoumal vlastnosti vzduchu Leonardo da Vinci a zjistil, že část vzduchu se spotřebuje při spalování a dýchání.
Polský alchymista a lékař Michal Sendivoj na začátku 17. století popsal látku obsaženou ve vzduchu a označil ji jako „cibus vitae“ (potrava života). Toto jeho zjištění ale ještě za objev kyslíku považováno není.
Na konci 17. století Robert Boyle zjistil, že vzduch je pro spalování nezbytný. Anglický chemik John Mayow ukázal, že oheň potřebuje k hoření pouze část vzduchu, kterou nazval spiritus nitroaereus. Experimentem zjistil, že umístění myši nebo zapálené svíčky do uzavřené nádoby nad vodou způsobí, že voda stoupne a část objemu vzduchu nahradí. Z toho odvodil, že nitroaereus je spotřebováván jak při dýchání, tak při spalování. Mayow také soudil, že plíce oddělují nitroaereus od vzduchu a předávají jej do krve, a že teplo a pohyb svalů zvířat vyplývají z reakce nitroaerea s určitými látkami v těle.[3]
Robert Hooke, Ole Borch nebo Michail Lomonosov ve svých experimentech v 17. a 18. století kyslík vyráběli, ale nikdo z nich jej neurčil jako chemický prvek.
O vysvětlení jevů vznikajících při spalování a korozi se pokoušela v 18. století tzv. flogistonová teorie. Podle této teorie, formulované v roce 1667 německým lékařem a alchymistou Johannem Joachimem Becherem a o něco později později zpopularizované Georgem Stahlem, byly všechny hořlavé materiály tvořeny ze dvou částí. Jedna část, nazývaná flogiston, se podle této teorie při spalování uvolnila; zbývající „deflogistikovaná“ část neboli calx byla považována za podstatu spáleného materiálu. Předpokládalo se, že vysoce hořlavé materiály, které zanechávají malé zbytky, jako je dřevo nebo uhlí, jsou převážně z flogistonu; nehořlavé látky, které korodují, například železo, obsahovaly flogistonu velmi málo. Vzduch nehrál v teorii flogistonu žádnou roli, ani nebyly prováděny žádné kvantitativní experimenty; stačilo pozorování, že po spálení se materiál stane lehčím a tedy se spálením něco ztratí.
Za objevitele kyslíku je někdy považován švédský lékárník Carl Wilhelm Scheele, který v letech 1771–1772 vyráběl plynný kyslík zahříváním oxidu rtuťnatého a různých dusičnanů. Pojmenoval tento plyn „ohnivý vzduch“, svůj objev však publikoval až v roce 1777. Mezitím nezávisle na Scheeleovi v roce 1774 provedl britský duchovní Joseph Priestley experiment, při kterém zaměřil sluneční světlo na oxid rtuťnatý obsažený ve skleněné trubici. Uvolňovaný plyn pojmenoval „dephlogisticated air“, tedy deflogistikovaný vzduch. Zjistil, že svíčky v plynu hořely jasněji a že myš byla aktivnější a při dýchání tohoto plynu žila déle. Zkusil plyn dýchat také sám a nezaznamenal výraznou odlišnost od běžného vzduchu, ale pociťoval při tom zvláštní lehkost. Své poznatky publikoval v roce 1775 a proto za objevitele kyslíku je obvykle považován on.
Autorem prvních kvantitativních experimentů s oxidací a prvního správného vysvětlení, jak funguje spalování, byl Antoine Lavoisier. Jeho experimenty vyvrátily flogistonovou teorii a prokázaly, že látka objevená Priestleyem a Scheeleem je chemický prvek. Dokázal také, že vzduch je směsí dvou plynů; pro „dýchatelnou“ část vzduchu, která je nezbytná pro spalování a dýchání, navrhl název oxygen („kyselinu tvořící“), protože se – mylně, jak později prokázal např. Humphry Davy – domníval, že kyslík je nezbytnou složkou všech kyselin. Pro druhou složku vzduchu navrhl název azote (z řeckého „bez života“) – nynější český název je dusík.
Původní atomová teorie Johna Daltona z roku 1801 předpokládala, že se každý chemický prvek skládá ze stejných a dále nedělitelných atomů a že prvky ve sloučeninách by za normálních okolností měly mít vůči sobě jednoduché hmotnostní poměry. Podle Daltona měl například být vzorec vody HO, takže by atomová hmotnost kyslíku byla 8krát větší než u vodíku (později zjištěná hodnota je asi 16krát). V roce 1805 Joseph Louis Gay-Lussac a Alexander von Humboldt ukázali, že voda se skládá ze dvou objemů vodíku a jednoho objemu kyslíku; a roku 1811 Amedeo Avogadro dospěl ke správné interpretaci složení vody na základě pravidla, kterému se nyní říká Avogadrův zákon.
Koncem 19. století si vědci uvědomili, že vzduch lze zkapalnit a jeho součásti izolovat jeho stlačením a ochlazením. Objev kapalného kyslíku oznámil švýcarský chemik a fyzik Raoul-Pierre Pictet v roce 1877; zkapalněný kyslík ve stabilním stavu ale vyrobili až v roce 1883 polští vědci Zygmunt Wróblewski a Karol Olszewski a v roce 1891 skotský chemik James Dewar dokázal vyrobit dostatečné množství tekutého kyslíku pro další studium. Komerční způsob výroby tekutého kyslíku pak nezávisle vyvinuli v roce 1895 německý inženýr Carl von Linde a britský inženýr William Hampson (oba snižovali teplotu vzduchu, dokud nezkapalnil, a poté postupně vyvařovali a zachytávali odděleně jednotlivé plyny).
V roce 1901 bylo poprvé prokázáno svařování pomocí spalování směsi acetylenu a stlačeného kyslíku; tento způsob svařování a řezání kovu se stal běžným.
V roce 1923 americký vědec Robert Goddard vyvinul raketový motor spalující kapalné palivo; použil benzín jako palivo a kapalný kyslík jako okysličovadlo a v roce 1926 jeho malá raketa (hmotnost 2,72 kg) doletěla do vzdálenosti 56 metrů při maximální rychlosti 97 km/h.
Základní fyzikálně-chemické vlastnosti
Kyslík je velmi reaktivní permanentní plyn, nezbytný pro existenci života na naší planetě. Slučování kyslíku s ostatními prvky se nazývá hoření, pokud je látka zahřátá na zápalnou teplotu. Jde prakticky vždy o exotermní reakci, která vede k uvolnění značného množství tepelné energie. Produkty hoření se nazývají oxidy (dříve kysličníky).
Výskyt v přírodě
Na Zemi je kyslík velmi rozšířeným prvkem. V minulosti planety byl jeho obsah většinou nižší, v několika obdobích prvohor a druhohor ale i vyšší než dnes.[4]
- V atmosféře tvoří plynný kyslík 21 objemových procent.
- Voda oceánů, které pokrývají 2/3 zemského povrchu, je hmotnostně z 90 % složena z kyslíku.
- V zemské kůře je kyslík majoritním prvkem, je přítomen téměř ve všech horninách. Jeho obsah je odhadován na 46 až 50 hmotnostních procent.
- V hlubších vrstvách zemského tělesa zastoupení kyslíku klesá a předpokládá se, že v zemském jádře je přítomen pouze ve stopách.
- Ve vesmíru je zastoupení kyslíku podstatně nižší. Na 1 000 atomů vodíku zde připadá pouze jeden atom kyslíku.
Anorganické sloučeniny
Ve svých sloučeninách se kyslík vyskytuje převážně v mocenství O−II, výjimečně pak jako O−I a O+I a také O −
2 v superoxidech (KO2 superoxid draselný) a O −
3 v ozonidech.
Záporně dvojmocný kyslík je přítomen ve velmi široké škále sloučenin. Především jsou to oxidy, vlastnosti jednotlivých sloučenin jsou detailněji popsány v kapitolách příslušných jednotlivým prvkům.
Kyslík je přítomen ve většině anorganických kyselin a jejich solí. Z těch nejdůležitějších je možno jmenovat uhličitany (CO3)−II, křemičitany (SiO3)−II, sírany (SO4)−II, dusičnany (NO3)− a fosforečnany (PO4)−III.
Alkalické sloučeny hydroxidy se vyznačují přítomnosti skupiny -OH. Mezi nejznámější patří hydroxid sodný NaOH, draselný KOH a vápenatý, hašené vápno Ca(OH)2.
Ve valenci O−I vystupuje kyslík v peroxidech, nejznámější z nich je peroxid vodíku H2O2. Tato kapalná sloučenina má silné oxidační účinky a v praxi se používá ve formě svých vodných roztoků v medicíně pro dezinfekci a v chemii jako oxidační činidlo. Peroxid sodný Na2O2 je pevná, hygroskopická látka, která nachází uplatnění jako velmi energetické oxidační činidlo.
Pouze fluor vykazuje větší elektronegativitu než kyslík a tvoří s ním několik fluoridů, v nichž se kyslík vyskytuje v mocenství O+I i O+II. Všechny fluoridy kyslíku jsou značně nestálé, přesto však existuje reálná možnost jejich využití jako raketového paliva.[zdroj?!]
Organické sloučeniny
Kyslík se vyskytuje ve velkém množství organických látek. Řada těchto sloučenin je součástí všech živých organismů, protože kyslík patří mezi základní biogenní prvky. Základní skupiny organických sloučenin s obsahem kyslíku jsou:
- alkoholy, obsahující skupinu C-OH
- fenoly, které skupinu -OH mají připojenu k aromatickému jádru
- ethery, obsahující skupinu C-O-C
- peroxidy, obsahující skupinu C-O-O-C
- aldehydy, obsahující skupinu HC=O
- ketony, obsahující skupinu C-CO-C
- karboxylové kyseliny, obsahující skupinu -COOH
- estery, obsahující skupinu R-CO-OR
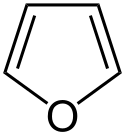
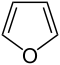
- z heterocyklických sloučenin je možno uvést např. furan:
Využití atmosférického kyslíku
Jedná se o neviditelnou složku vzduchu nutnou pro spalování prakticky každého fosilního paliva (technologická oxidace fosilních paliv)
- výroba elektrické energie – spalování fosilních paliv v tepelných elektrárnách (často v kombinaci s výrobou technologického tepla)
- výroba technologického tepla – spalování fosilních paliv v teplárnách (často v kombinaci s výrobou elektrické energie)
- pohon motorů a turbín – ve všech druzích spalovacích motorů a turbín
- vytápění domácností v domovních kotelnách, kamnech či v krbech
- příprava pokrmů (kupř. plynové sporáky)
- nouzové osvětlování (kupř. svíčky, petrolejové lampy)
Nežádoucí chemicko-technologický či fyzikálně-chemický proces, koroze kovů je způsobená nežádoucí oxidací kovů a dalšími doprovodnými chemickými reakcemi.
Výroba a využití
Kyslík se prakticky výlučně vyrábí destilací zkapalněného vzduchu. Vyrobený kyslík se uchovává buď ve zkapalněném stavu ve speciálních Dewarových nádobách (viz obrázek) nebo plynný v ocelových tlakových lahvích. Vzhledem k vysoké reaktivitě čistého kyslíku je nezbytné, aby se nedostal do přímého kontaktu s organickými látkami. Proto se žádné součásti aparatury pro uchovávání a manipulaci s kapalným nebo stlačeným kyslíkem nesmí mazat organickými tuky nebo oleji.
- Kyslíkové koncentrátory jsou přístroje, které nepotřebují žádnou zásobu kyslíku v podobě lahví, ale umožňují vyvíjení vyšší koncentrace neomezeně, nebo dle nastavení.
- V medicíně se čistý kyslík používá při operacích a traumatických stavech pro podporu pacientova dýchání a lepšímu okysličení organismu. Směsi kyslíku s inertními plyny slouží potápěčům k potlačení dekompresní nemoci. Je součástí i všech ostatních dýchacích plynů, které se používají pro potápění do velkých hloubek.
- Také vysokohorští horolezci a letci se v nutných případech uchylují k dýchání čistého kyslíku. I piloti stíhacích letadel jsou vybaveni směsmi stlačených plynů, jejichž základní složkou je kyslík. To proto, že zvýšením koncentrace kyslíku se zvýší jeho parciální tlak a ulehčí se tak dýchání v řídké atmosféře a předejde vysokohorské nemoci.
- Američtí astronauti programu Apollo dýchali také atmosféru z téměř čistého kyslíku, což umožnilo snížit tlak v kabině zhruba na třetinu běžné hodnoty a tak odlehčit její hermetickou konstrukci. To se ale stalo osudným posádce Apolla 1, která ve vysoce hořlavé atmosféře uhořela. Všechny skafandry pro výstup do kosmu používají kyslíkovou atmosféru kvůli co nejnižšímu přetlaku, protože přetlak omezuje pohyblivost skafandru.
- Při hoření směsi kyslíku s acetylenem lze dosáhnout teploty cca 3 150–3 200 °C. Proto se kyslíko-acetylenový plamen využívá k řezání oceli a tavení kovů s vysokým bodem tání, například platinových kovů.
- Při výrobě oceli je nutné především odstranit z matrice železa přebytečný uhlík, který je ve formě karbidu železa. Tento přebytečný uhlík spolu s dalšími příměsmi se odstraňuje spálením obvykle v tzv. konvertoru, a to vháněním vzduchu v Bessemerově a Thomasově konvertoru nebo vháněním čistého kyslíku do roztaveného železa v kyslíkovém konvertoru), kde za vysoké teploty taveniny dochází k oxidaci přítomného uhlíku na plynné oxidy, které odcházejí jako spaliny.
- Kapalný kyslík většinou slouží jako okysličovadlo raketových motorů při letech kosmických lodí.
- Kyslík se používá jako jedna ze složek pro náplň některých typů palivových článků.
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Oxygen na anglické Wikipedii.
- ↑ a b Oxygen. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Ďasík, voník, ytřík a platík. Český rozhlas Střední Čechy [online]. 2005-04-01 [cit. 2025-04-08]. Dostupné online.
- ↑ World of Chemistry contributors. World of Chemistry. [s.l.]: Thomson Gale, 2005. ISBN 978-0-669-32727-4. Kapitola John Mayow.
- ↑ Sperling; E. A.; et al. (2022). Breathless through Time: Oxygen and Animals across Earth’s History. The Biological Bulletin. 243 (2): 000–000. doi:10.1086/721754
Literatura
- Cotton F.A., Wilkinson J.: Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.: Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood – A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu kyslík na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyslík na Wikimedia Commons  Galerie kyslík na Wikimedia Commons
Galerie kyslík na Wikimedia Commons Téma Kyslík ve Wikicitátech
Téma Kyslík ve Wikicitátech Slovníkové heslo kyslík ve Wikislovníku
Slovníkové heslo kyslík ve Wikislovníku- (anglicky) Oxidizing Agents > Oxygen
- (anglicky) Oxygen (O2) Properties, Uses, Applications
- (anglicky) Oxygen on In Our Time at the BBC
Média použitá na této stránce
Visible spectrum of oxygen
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for oxidizing substances
Structure of furan
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for gases under pressure