Můstkový ligand

V koordinační chemii se jako můstkový ligand označuje ligand, který je navázán na dva nebo více atomů, často iontů kovů.[1] Tyto ligandy mohou být jednoatomové i víceatomové. Jako můstkové ligandy mohou fungovat mnohé komplexní organické sloučeniny, a tak se takto označují obvykle jen malé ligandy, jako jsou pseudohalogenidy, případně ligandy vytvořené přímo za účelem propojení dvou kovů.
Při pojmenovávání komplexů, ve kterých jeden atom vytváří můstek mezi kovy, se před název ligandu přidává řecké písmeno mí (μ),[2] s číslem v dolním indexu, který označuje počet atomů kovů ligandu. μ2 se obvykle zapisuje jednodušeji jako μ. Při popisu komplexů je třeba nezaměňovat μ za η (éta), jež slouží k označení hapticity. Ligandy nevytvářející můstky se nazývají koncové (terminální) ligandy.
Příklady anorganických můstkových ligandů
Můstek mohou vytvořit téměř všechny ligandy, výjimky představují aminy a amoniak.[3]
K častým anorganickým můstkovým ligandům patří většina běžných aniontů:
| Můstkový ligand | Název | Příklad |
|---|---|---|
| OH− | hydroxido | [Fe2(OH)2(H2O)8]4+ |
| O2− | oxido | [Cr2O7]2− |
| SH− | hydrosulfido | Cp2Mo2(SH)2S2 |
| NH2− | amido | HgNH2Cl |
| N3− | nitrido | [Ir3N(SO4)6(H2O)3]4− |
| CO | karbonyl | Fe2(CO)9 |
| Cl− | chlorido | Nb2Cl10 |
| H− | hydrid | B2H6 |
| CN− | kyanido | Fe7(CN)18 |
Mnoho jednoduchých organických liganů vytváří mezi atomy kovů silné můstky; jako příklady lze uvést organické deriváty výše uvedených ligandů (R = alkyl nebo aryl): OR−, SR−, amido (NR -
2 ), imido (NR2−), fosfido (PR -
2 ) a fosfinidinové ligandy (PR2−).
Sloučeniny
- Sloučeniny obsahující můstkové ligandy
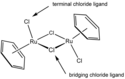
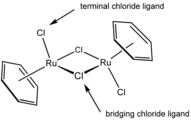
- V tomto komplexu, dimeru (benzen)ruthenium dichloridu, jsou dva chloridové ligandy koncové a dva vytvářejí můstky.
- V komplexu Co3(CO)9(CtBu) vytváří ligand CtBu můstek mezi třemi atomy, i když se tato skutečnost do vzorce obvykle nezapisuje.
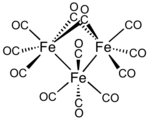
- U dodekakarbonylu triželeza vytvářejí dva CO ligandy můstky a zbylých deset jsou koncové ligandy. Koncové a můstkové CO ligandy se rychle vyměňují.
- Dimer chloridu niobičného (NbCl5) obsahuje dva můstkové a osm koncových chloridových ligandů.
- Sloučenina [Au6C(PPh3)6]2+ obsahuje μ6-karbidový ligand,; značka μ se zde většinounepoužívá.
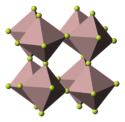
- U oxidu rheniového jsou všechny oxidové ligandy μ2. Tyto oxidové ligandy drží pohromady kovová centra.
- Molekuly chloridu zirkoničitého (ZrCl4) obsahují koncové i dvojnásobně můstkové chloridové ligandy.
- Octan rhodnatý má čtyři octanové skupiny jako můstkové ligands.
- VO(HPO4)*0,5 H2O má dvojici vanadičitých center spojených molekulami vody.[4]
Vazby
U dvojnásobných (μ2-) ligandů se vyskytují čtyřelektronové a dvouelektronové vazebné interakce. Tyto stavy se u prvků vlastní skupiny dají zapsat jako [Me2Al(μ2-Cl)2 a [Me2Al(μ2-Me)2. Tuto analýzu ztěžují možné vazby mezi kovy. Výpočetními studiemi bylo potvrzeno, že u většiny sloučenin s kovy oddělenými můstkovými ligandy vazby kov–kov nejsou přítomny, například nonakarbonyl diželeza, Fe2(CO)9 neobsahuje vazby železo–železo a nachází se v něm tricentrické dvouelektronové vazby mezi třemi můstkovými CO ligandy.[5]

Polyfunkční ligandy
Polyfunkční ligandy se mohou na kovy navázat různými způsoby a mohou tak i různě vytvářet můstky mezi nimi, například sdílením jednoho nebo i více atomů. Příklady takových ligandů jsou oxoanionty CO 2−
3 a podobné karboxyláty, dále PO 3−
4 a polyoxometaláty. Tyto můstkové dvojice kovů jsou obsaženy například v některých organofosforečných sloučeninách, jako je bis(difenylfosfino)methan (dppm). Ph2PCH2PPh2.
Odkazy
Související články
Reference
V tomto článku byl použit překlad textu z článku Bridging ligand na anglické Wikipedii.
- ↑ The IUPAC Compendium of Chemical Terminology: The Gold Book. Příprava vydání Victor Gold. 4. vyd. Research Triangle Park, NC: International Union of Pure and Applied Chemistry (IUPAC) Dostupné online. doi:10.1351/goldbook.b00741. (anglicky) DOI: 10.1351/goldbook.
- ↑ Nomenclature of inorganic chemistry. IUPAC recommendations 2005. Cambridge: Royal Society of Chemistry xii, 366 pages s. Dostupné online. ISBN 978-0-85404-438-2, ISBN 0-85404-438-8. OCLC 60838140 S. 163–165.
- ↑ H. Werner. The Way into the Bridge: A New Bonding Mode of Tertiary Phosphanes, Arsanes, and Stibanes. Angewandte Chemie International Edition. 2004, s. 938–954. doi:10.1002/anie.200300627. PMID 14966876.
- ↑ H.-J. Koo; M. Whangbo; P. D. VerNooy; C. C. Torardi; W. J. Marshall. Flux growth of vanadyl pyrophosphate, (VO)2P2O7, and spin dimer analysis of the spin exchange interactions of (VO)2P2O7 and vanadyl hydrogen phosphate, VO(HPO4).0.5H2O. Inorganic Chemistry. 2002, s. 4664–4672. doi:10.1021/ic020249c. PMID 12206689.
- ↑ a b J. C. Green; M. L. H. Green; G. Parkin. The occurrence and representation of three-centre two-electron bonds in covalent inorganic compounds. Chemical Communications. 2012, s. 11481–11503. doi:10.1039/c2cc35304k. PMID 23047247.
Média použitá na této stránce
Ball-and-stick model of the part of the crystal structure of zirconium(IV) chloride, ZrCl4. Crystal structure data from 3DChem.
An example of a μ3 bridging ligand. The compound is a (Co(CO)3)3(μ3-(C-tBu))
Chemical diagram showing a μ2 bridging ligand (L) between two metal atoms (M)
Autor: Smokefoot, Licence: CC BY-SA 3.0
representations of two kinds of bridging ligand
Structural formula of the niobium pentachloride dimer, Nb2Cl10.
X-ray crystallographic data from Acta Cryst. (1991). C47, 2435-2437.Autor: Smokefoot, Licence: CC BY-SA 3.0
revised structure of Fe3(CO)12 showing only 2 Fe-Fe bonds, consistent with contemp bonding theory
structure of Au6C(PPh3)6++
structure of benzeneRuCl2
Ball-and-stick model of the rhodium(II) acetate hydrate dimer (dirhodium tetraacetate dihydrate), C8H16O10Rh2, as found in the crystal structure.
X-ray diffraction data from Acta Cryst. (1971). B27, 1664-1671.
Model constructed in CrystalMaker 8.1.
Image generated in Accelrys DS Visualizer.Autor: Smokefoot, Licence: CC BY-SA 4.0
sructure ofthe compound from Xray coordinates


![Sloučenina [Au6C(PPh3)6]2+ obsahuje μ6-karbidový ligand,; značka μ se zde většinounepoužívá.](http://upload.wikimedia.org/wikipedia/commons/thumb/5/5f/Au6C%28PPh3%296.png/138px-Au6C%28PPh3%296.png)

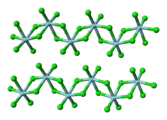

![VO(HPO4)*0,5 H2O má dvojici vanadičitých center spojených molekulami vody.[4]](http://upload.wikimedia.org/wikipedia/commons/thumb/9/95/VO%28HPO4%290.5H2O.tif/lossless-page1-185px-VO%28HPO4%290.5H2O.tif.png)