Methyltrioxorhenium
| Methyltrioxorhenium | |
|---|---|
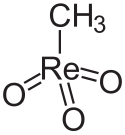
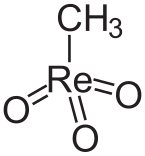 Strukturní vzorec methyltrioxorhenia | |
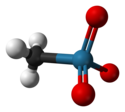
 Kuličkový model molekuly methyltrioxorhenia | |
| Obecné | |
| Systematický název | Methyltrioxorhenium |
| Anglický název | Methylrhenium trioxide |
| Německý název | Methyltrioxorhenium |
| Sumární vzorec | CH3ReO3 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 70197-13-6 |
| PubChem | 2734010 |
| SMILES | C[Re](=O)(=O)=O |
| InChI | InChI=1/CH3.3O.Re/h1H3;;;;/rCH3O3Re/c1-5(2,3)4/h1H3 |
| Vlastnosti | |
| Molární hmotnost | 249,24 g/mol |
| Teplota tání | 112 °C |
| Rozpustnost ve vodě | vysoce rozpustný |
| Bezpečnost | |
| [1] Varování[1] | |
Některá data mohou pocházet z datové položky. | |
Methyltrioxorhenium (MTO) je organokovová sloučenina se vzorcem CH3ReO3. Je to těkavá, bezbarvá pevná látka používaná jako katalyzátor. Oxidační stav rhenia je +VII, molekula má tvar trigonální pyramidy.[2]
Příprava
Sloučenina je dostupná komerčně, lze ji připravit několika způsoby, typickou metodou je reakce oxidu rhenistého s tetramethylcínem:[3]
- Re2O7 + (CH3)4Sn → CH3ReO3 + (CH3)3SnOReO3
Jsou známy i další alkyl- a arylderiváty. Tyto sloučeniny se chovají jako Lewisovy kyseliny, vytváří adukty 1:1 a 1:2 s halogenidy a aminy.
Využití
Využívá se jako heterogenní katalyzátor v mnoha procesech. Imobilizovaný na Al2O3/SiO2, katalyzuje metatezi olefinů při teplotě 25 °C.[4]
V roztoku katalyzuje oxidace peroxidem vodíku.[5] Terminální alkyny oxiduje na odpovídající kyselinu nebo ester, interní pak na diketony. Oxidace alkenů vede ke tvorbě epoxidů.[5] Také dokáže katalyzovat oxidaci aminů na N-oxidy pomocí peroxouhličitanu sodného.[5][6]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Methylrhenium trioxide na anglické Wikipedii.
- ↑ a b Methyltrioxorhenium(VII). pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ HERRMANN, Wolfgang A.; KIPROF, Paul; RYPDAL, Kristin. Multiple bonds between main-group elements and transition metals. 86. Methyltrioxorhenium(VII) and trioxo(.eta.5-pentamethylcyclopentadienyl)rhenium(VII): structures, spectroscopy and electrochemistry. Journal of the American Chemical Society. 1991-08, roč. 113, čís. 17, s. 6527–6537. Dostupné online [cit. 2021-01-07]. ISSN 0002-7863. doi:10.1021/ja00017a025. (anglicky)
- ↑ HERRMANN, W.A.; KRATZER, R. M.; FISCHER, R. W. Alkylrhenium Oxides from Perrhenates: A New, Economical Access to Organometallic Oxide Catalysts. Angew. Chem. Int. Ed. Engl.. 1997, roč. 36, čís. 23, s. 2652–2654.
- ↑ KÜHN, Fritz E.; SCHERBAUM, Andrea; HERRMANN, Wolfgang A. Methyltrioxorhenium and its applications in olefin oxidation, metathesis and aldehyde olefination. Journal of Organometallic Chemistry. 2004-11, roč. 689, čís. 24, s. 4149–4164. Dostupné online [cit. 2021-01-07]. doi:10.1016/j.jorganchem.2004.08.018. (anglicky)
- ↑ a b c MTO - Methyltrioxorhenium. www.organic-chemistry.org [online]. [cit. 2021-01-07]. Dostupné online.
- ↑ JAIN, Suman; JOSEPH, Jomy; SAIN, Bir. Rhenium-Catalyzed Highly Efficient Oxidations of Tertiary Nitrogen Compounds to N -Oxides Using Sodium Percarbonate as Oxygen Source. Synlett. 2006-09, roč. 2006, čís. 16, s. 2661–2663. Dostupné v archivu pořízeném dne 2018-06-02. ISSN 0936-5214. doi:10.1055/s-2006-951487. (anglicky)
Externí odkazy
 Obrázky, zvuky či videa k tématu Methyltrioxorhenium na Wikimedia Commons
Obrázky, zvuky či videa k tématu Methyltrioxorhenium na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for oxidizing substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Structure of Methylrhenium trioxide
Ball-and-stick model of the methylrhenium trioxide molecule