Methylvinylketon
| Methylvinylketon | |
|---|---|
 Zjednodušený racionální vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | Butenon |
| Ostatní názvy | But-3-en-2-on, methylenaceton, MVK |
| Anglický název | Methyl vinyl ketone |
| Německý název | Methylvinylketon |
| Funkční vzorec | H2C=CH-CO-CH3 |
| Sumární vzorec | C4H6O |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 78-94-4 |
| PubChem | 6570 |
| SMILES | CC(=O)C=C |
| InChI | InChI=1/C4H6O/c1-3-4(2)5/h3H,1H2,2H3 |
| Vlastnosti | |
| Molární hmotnost | 70,090 g/mol |
| Teplota tání | −7 °C (266 K) |
| Teplota varu | 81,4 °C (354,6 K) |
| Rozpustnost ve vodě | rozpustný |
| Rozpustnost v polárních rozpouštědlech | rozpustný v polárních organických rozpouštědlech |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Methylvinylketon (MVK, systematický název butenon), je reaktivní organická sloučenina a nejjednodušší enon. Je užitečným meziproduktem při syntéze dalších sloučenin.
Výroba
MVK se průmyslově vyrábí kondenzací acetonu a formaldehydu, po níž následuje dehydratace. Podobně se dá získat Mannichovou reakcí diethylamoniumchloridu (chloridu kationtu odvozeného od diethylaminu) s acetonem za vzniku Mannichova adduktu[2]
- CH3C(O)CH3 + CH2O + [H2NEt2]Cl → [CH3C(O)CH2CH2N(H)Et2]Cl + H2O
který je následně zahříván, čímž se vytvoří chlorid amonný a MVK.[2]
- [CH3C(O)CH2CH2N(H)Et2]Cl → CH3C(O)CH=CH2 + [H2NEt2]C
Reaktivita a použití
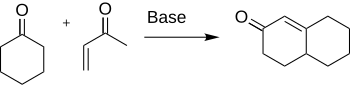
MVK může působit jako alkylační činidlo, jelikož je účinným Michaelovým akceptorem. Byl používán na přípravu steroidů Robinsonovou anelací:
Jeho alkylační vlastnosti způsobují vysokou toxicitu, ale dělají z něj užitečný meziprodukt v organické syntéze. MVK spontánně polymerizuje. Obvykle se skladuje v hydrochinonu, který polymerizaci inhibuje.

Jako elektrofilní alken může tvořit adukty s cyklopentadienem. Vzniklý norbornenový derivát je meziproduktem při syntéze pesticidu biperidenu a přes svůj kyanohydrin také vinklozolinu. Rovněž se jedná o prekurzor syntetického vitaminu A.
MVK se též používá na výrobu některých léčiv jako jsou etorfin, buprenorfin, butaklamol a etretinát.
Bezpečnost
MVK je značně nebezpečný, při vdechnutí způsobuje kašlání a dušnost i při nízkých koncentracích. Také snadno způsobuje dráždění očí, kůže a sliznic.
Reference
V tomto článku byl použit překlad textu z článku Methyl vinyl ketone na anglické Wikipedii.
- ↑ a b Methyl vinyl ketone. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ a b L. WILDS, Alfred; NOWAK, Robert M.; MCCALEB1, Kirtland E. 1-Diethylamino-3-butanone. Organic Syntheses. 1957, s. 18. doi:10.15227/orgsyn.037.0018.
Externí odkazy
 Obrázky, zvuky či videa k tématu Methylvinylketon na Wikimedia Commons
Obrázky, zvuky či videa k tématu Methylvinylketon na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances
Chemical diagram for methyl vinyl ketone
Autor: Jynto (talk), Licence: CC0
Ball-and-stick model of the methyl vinyl ketone molecule, the simplest enone.
Color code:
- Carbon, C: black
- Hydrogen, H: white
- Oxygen, O: red
Chemical structure of vinclozolin
Autor: Ehart4, Licence: CC BY-SA 3.0
This is the general description of the Robinson Annulation reaction.
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances