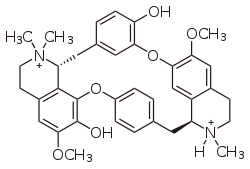
Myorelaxans
Myorelaxancia (jednotné číslo myorelaxans) jsou látky, které uvolňují spazmy (křeče) a vedou k relaxaci příčně pruhovaného svalstva. Existují dva druhy myorelaxancií, periferní a centrální myorelaxancia. Periferní jsou vysoce účinné látky používané při operacích, způsobují celkové ochrnutí (například přírodní kurare), centrální pouze snižují napětí svalstva a používají se například při léčbě bolesti zad, kde ale nemusejí být účinné.[1]
Periferní myorelaxancia
Působící přes NM receptory
- kurarimimetika, kurareformní látky
- látky blokující stah kosterních svalů periferními mechanismy, zásahem do procesů neurotransmise na nervosvalovém spojení; snižují svalový tonus, vyvolávají úplnou relaxaci kosterních svalů, nepůsobí na hladké svaly. Jejich použití je omezeno na anestezii při operacích, dochází k přechodnému ochrnutí.
Přenos vzruchu
Na nervosvalovém spojení končí pouze jedno nervové vlákno. Neurotransmiterem je acetylcholin (ACH). ACH je uvolněn akčním potenciálem a difunduje přes synaptickou štěrbinu k NM receptorům, které jsou lokalizované v membráně svalové buňky. Aktivací těchto receptorů se zvyšuje permeabilita pro Na+ a K+ ionty, membrána depolarizuje a tato změna potenciálu se nazývá ploténkový potenciál. Pokud je tento potenciál dostatečně vysoký, dochází k depolarizaci membrány a impuls se šíří z nervosvalového spojení do svalové buňky, vzniká akční potenciál svalové buňky a svalová buňka se kontrahuje.
Podle mechanismu, kterým periferní myorelaxancia vyvolávají blokádu přenosu, rozdělujeme
- myorelaxancia kompetitivní (nedepolarizující)
- myorelaxancia nekompetitivní (depolarizující)
Kompetitivní (nedepolarizující) myorelaxancia
Mechanismus účinku
Obsazují postsynaptické nikotinové receptory a zabraňují působení ACH, jsou to kompetitivní antagonisté ACH. Nevyvolávají depolarizaci, podle velikosti molekuly se také nazývají pachykurarové látky. Mezi další účinky patří účinek na žírné buňky, mohou uvolňovat histamin (pruritus, bronchospasmus…). Účinky nedepolarizujících myorelaxancií je možné ukončit podáním inhibitorů ACH-esterázy, kdy nahromadění endogenní ACH vytěsní myorelaxancium z vazby na receptor.
Zástupci

d-tubokurarin, pipekuronium, pankuronium (dlouhotrvající úč.), vekuronium, alkuronium (střednědobý úč.), gallamin
Farmakologické účinky
Účinky nedepolarizujících myorelaxancií se manifestují na kosterních svalech počáteční únavou, slabostí žvýkacích svalů, obtížnými pohyby bulbů a obtížemi při mluvení, následované ochablostí víček, diplopií, dysfagií. Paralýza kosterních svalů postupuje od periferie k trupu, ochabuje svalstvo krku, břišní svaly, dochází k relaxaci bránice s rizikem periferní zástavy dýchání. Po celou dobu je zachováno vědomí i schopnost vnímat bolest, proto se podávají až po aplikaci celkového anestetika. Účinek je závislý na dávce, obvykle trvá 12-30 min.
Nežádoucí účinky
Hlavním nebezpečím je zástava dechu obrnou dýchacích svalů. Další je riziko vyplavení histaminu s následnou hypotenzí, bronchospazmem a zvýšením bronchiální sekrece a salivace. Myorelaxační účinek může být výrazně prodloužen při poruchách funkce jater a ledvin a u pacientů s myopatií. Tubokurarin může vyvolat hypotenzi, pravděpodobně vyvolanou vyplavením histaminu (premedikace antihistaminiky), pankuronium a gallamin zvyšují srdeční frekvenci. Antidotem jsou inhibitory ACH-esterázy, nejčastěji neostigmin, pyridostigmin (zvýšení dostupnosti ACH inhibicí ACH-esterázy a také zvýšeným uvolňováním ACH z nervových zakončení) a edrofonium.
Interakce
Celková anestetika – zvyšují stupeň nervosvalového bloku v závislosti na dávce; ATB (zejména aminoglykosidy) – zvýšení nervosvalové blokády; lokální anestetika – potencují blokádu
Klinická farmakologie – indikace
Nedepolarizující myorelaxancia se používají k dosažení svalové relaxace u déle trvajících operací, podmínku použití je zajištění řízeného dýchání, a k diagnostice myasthenia gravis, již ve velmi malých množstvích vyvolávají silnou myorelaxaci.
Chemie
Všechny látky jsou strukturálně podobně ACH. Nedepolarizující mají strukturu ACH schovanou v objemných cyklických strukturách – isochinolinové deriváty a steroidy (bazické androstany). Přítomnost kvarterního dusíku zajišťuje nízkou lipofilitu a tím brání přestupu přes HEB do CNS.
Nekompetitivní (depolarizující) myorelaxancia
Mechanismus účinku
Jejich působení je dvoufázové. V první fázi vyvolávají depolarizaci a kontrakci kosterních svalů za pomoci stimulace NM receptorů. Tento účinek má delší trvání než účinek vyvolaný endogenní ACH. Přetrvávající depolarizace vede ke ztrátě elektrické dráždivosti membrány, dochází k depolarizační membráně. Depolarizovaná ploténka není schopná reagovat na ACH impulsy, tuto blokádu nelze odstranit nahromaděným ACH. Podáním ACH-esterázy může být stav spíše prohlouben, protože dojde ke zpomalení odbourávání depolarizujícího myorelaxancia. Není znám antagonista této fáze depolarizace. V druhé fázi se účinek depolarizujícího myorelaxancia zmenšuje, dochází k částečné repolarizaci, která ale nestačí k obnovení polarizovatelnosti membrány. V této fázi může být účinek myorelaxancia zmírněn podání ACH-esterázy.
Zástupci
Suxamethonium (sukcinylcholin je jeho (účinný) metabolit, vzniklý odbouráním jednoho cholin ze dvou z molekuly), dekamethonium
Farmakologické účinky
Depolarizující myorelaxancia vyvolávají nejprve svalové záškuby, po kterých nastupuje stádium relaxace. K relaxaci dochází nejprve na končetinách a poté se rozšiřuje na svalstvo břicha a hlavy. Efekt látek je jen několikaminutový. Sukcinylcholin je rozkládán cholinesterázou, při jejím nedostatku může být jeho účinek výrazně prodloužen.
Nežádoucí účinky
U depolarizujících myorelaxancií může docházet k periferní zástavě dechu. Po podání suxamethonia (především u pacientů s popáleninami, úrazy, selháním ledvin) může dojít ke zvýšení plazmatických hladin draslíku a poruchám srdečního rytmu až srdeční zástavě. Suxamethonium také zvyšuje nitrooční a nitrolební tlak, proto je kontraindikován u glaukomu. Po podání suxamethonia může dojít k alergické reakci nebo k výskytu přetrvávajících bolestí ve svalech, které mohou být vyvolány i svalovým poškozením v důsledku nesynchronizovaných kontrakcí v počátcích jeho působení. Suxamethonium zvyšuje intragastrický tlak (náchylnost ke zvracení, riziko aspirace žaludečního obsahu) a po jeho podání si pacienti stěžují na bolest svalů, doprovázenou myoglobinurie (poškození svalů nesynchronizovanými kontrakcemi sousedních svalových vláken před nástupem paralýzy). Může se objevit i maligní hypertermie, velmi závažný stav, který může končit i fatálně. Řeší se intenzivním ochlazováním a podáním dantrolenu.
Interakce
ATB (zejména aminoglykosidy) – zvýšení nervosvalové blokády; lokální anestetika – potencují blokádu, depolarizující jsou antagonizována nedepolarizujícími, ty se podávají v neparalyzujících dávkách jako prevence k fascikulací (svalové záškuby) a pooperačních bolestí.
Klinická farmakologie – indikace
Depolarizující myorelaxancia působí velmi krátce a využívají se tam, kde je nutná krátká a rychlá svalová relaxace (např. intubace, endoskopie). Aplikují se až po podání celkového anestetika. Dále je lze využít proti křečím různé etiologie a při umělé plicní ventilaci ke snížení rezistence hrudníku.
Chemie
Opět strukturálně podobné ACH, většinou zdvojená molekula ACH, lineární struktura. Kvarterní dusík zabraňuje přestupu přes HEB do CNS.
Působící jiným mechanismem
Působící presynapticky
Zástupcem je botulotoxin A. Jedná se o proteinový komplex neurotoxinu A, který je produkován Clostridium botulinum. Botulotoxin A interferuje s proteiny odpovědnými v nervovém zakončení motorického nervu za skladování neurotransmiteru, inhibuje synaptobrevin a další bílkoviny, a inhibuje tak uvolňování ACH z nervového zakončení. K obnovení funkce dochází až po vytvoření nových bílkovin membrány vezikul. Používá se u blefarospasmu, k mírnění projevů spastické tortikollis a jiných neurologických poruchách, které jsou doprovázeny spazmy (mozková obrna). V moderní době jsou injekce botulotoxinu používány v estetické medicíně
Působící postsynapticky
Zde je zástupcem dantrolen (derivát hydantoinu). Mechanismem účinku dantrolenu je blokáda uvolňování iontů vápníku ze sarkoplazmatického retikula přes vazbu na ryanodinové receptory. Tím dochází k přerušení spojení mezi excitací a kontrakcí kosterních svalů. Je používán v terapii maligní hypertermie. Maligní hypertermie je charakterizována vzestupem koncentrace vápníku v myocytech, který je provázen hypertermií a metabolickou acidózou. Dantrolen však musí být podán včas, tj. dříve než se vyplaví všechny zásoby vápníku za sarkoplazmatického retikula.
Centrální myorelaxancia
Do velké míry snižují klidový tonus svalů bez ztráty jejich volní kontrakce. Způsobují útlum polysynaptických drah v CNS, tím tlumí různé reflexy, které vedou ke spastickým reakcím. Všeobecným nežádoucím účinkem je celkové snížení svalového tonu s rizikem posturální nestability, dále ospalost, zmatenost (projevy celkového útlumu CNS).
Zástupci
baklofen, tetrazepam, chlorzoxazon, tolperizon, tizanidin
Indikace
Poranění míchy, porodní poškození mozku, spasticita spojená se sclerosis multiplex, adjuvantní léky u spastických stavů různé etiologie
Baklofen
Mechanismus účinku
Působí přes GABA receptory. Baklofen je selektivní agonista na GABAB lokalizovaných presynapticky. Zde podráždění znamená inhibici produkce cAMP, otevření K+ kanálů a hyperpolarizaci membrány, snížení vstupu Ca2+ iontů. V důsledku tohoto dojde k inhibici uvolňování neurotransmiteru z presynaptického zakončení neuronu.
Nežádoucí účinky
Sedace (útlum), změny chování, hypotonie, zmatenost, cefalgie (bolest hlavy), nauzea (nevolnost)
Interakce
Účinek a toxicitu baklofenu mohou zvyšovat tricyklická antidepresiva, sám zvyšuje hodnoty jaterních transamináz
Tizanidin
Tizanidin má výrazné alfa2mimetické účinky, posiluje jak presynaptickou, tak postsynaptickou inhibici v míše a tím snižuje uvolňování excitačních působků, zejména NMDA. Nežádoucí účinky v podobě ospalosti, hypotenze, sucha v ústech a tělesné slabosti.
Na českém trhu se tizanidin objevuje pod názvem Sirdalud ve variantách 2 mg a 4 mg. V září 2023 bylo na recepty vydáno přes 11 000 balení slabší varianty a 6 000 balení varianty 4 mg.[2][3]
Ostatní – látky ze skupiny benzodiazepinů
Mechanismus účinku
Benzodiazepiny selektivně obsazují specifické vazebné místo na GABAA receptoru, který je spřažen s transmembránovým chloridovým kanálem. Touto vazbou alostericky zvyšují afinitu vazebného místa pro GABA. Výsledkem je zvýšení influxu Cl− iontů do cytoplasmy a prohloubení postsynaptického inhibičního potenciálu. Dále se předpokládá existence dvou skupin benzodiazepinových receptorů BZD-1 (sedativní, anxiolytické a hypnotické účinky) a BZD-2 (antikonvulzivní a myorelaxační účinky). Většina benzodiazepinů působí na všechny typy receptorů. Benzodiazepiny mají výbornou biologickou dostupnost, silnou vazbu na bílkoviny, snadno prostupují HEB a jsou biotransformovány pomocí CYP 450 a následně glukurovány.
Nežádoucí účinky
Sedace (útlum), riziko vzniku závislosti, riziko respiračního útlumu
Interakce
Na úrovni vazby na plazmatické bílkoviny, na úrovni CYP 450, alkohol
Chemie centrálních myorelaxancií
a) deriváty propandiolu – meprobamat, guaifenesin
b) heterocyklické sloučeniny – tetrazepam, chlorzoxazon
c) centrální myorelaxancia jiných struktur – memantin, chlorpromazin
dále tolperison, lanperison (látky ze skupiny aminoketonů) – účinek na úrovni míchy nebo mozkového kmene
Myorelaxancia z přírodních zdrojů (farmakognosie)
Jediným zástupcem periferních myorelaxancií ve farmakognosii je kurare, indiánský šípový jed používaný indiány v Jižní Americe k lovu zvěře. Kurare vznikne zahuštěním vodního extraktu z částí rostlin rodu Chondrodendron, Telitoxicum, Anomospermum a Strychnos. Účinný je pouze při parenterální aplikaci. Dříve se kurare dělilo dle typů obalů, které jsou specifické pro jednotlivé oblasti, na tukokurare (bambusové roury), postkurare (hliněné nádoby) a kalebasové kurare (plody lahvovníku). V současnosti se kurare dělí dle botanického původu a chemické konstituce obsahových látek na dvě skupiny.
1) Menispermaceae kurare
Zdroj
Chondrodendron tomentosum (Menispermaceae), keř rostoucí v Jižní Americe; další zdroje rostliny rodu Anospermum a Telitoxicum.
Droga
Vodní extrakt kořenů, listů, kůry, který je zahuštěný do pevné konzistence
Obsahové látky
Směs alkaloidů s převahou tubokurarinu. Ten se získává izolací z vodného roztoku jako pikrát, pro aplikaci se používá chlorid. Dále terciární aminy – isochondrodendrin, kurin, chondrokurin, isochondrokurin.
Indikace
Svalové relaxans v hrudní a břišní chirurgii při celkové anestezii, k uvolnění spasticity svalů, tetanických křečí, diagnostika myastenia gravis.
Chemie
Z chemického hlediska patří mezi bisbenzylisochinolinové deriváty s kvarterním dusíkem, spojené hlava-pata. Patří mezi alkaloidy odvozené od fenylalaninu.
2) Loganiaceae kurare
Zdroj
Strychnos toxifera, S. crevauxii, S. castelnaei (Loganiaceae)
Droga
Vodní extrakt listů a kůry, který je zahuštění do pevné konzistence
Obsahové látky
Deriváty bisondolových alkaloidů typu strychninu – C-toxiferin, C-kurarin, dále monomerní strychninové nebo karbolinové akaliody.
Indikace
Svalové relaxans v hrudní a břišní chirurgii při celkové anestezii, k uvolnění spasticity svalů, tetanických křečí, diagnostika myastenia gravis, pro výrobu polosyntetického alkuroniumchloridu
Chemie
Z chemického hlediska patří mezi bisindolové alkaloidy, je to dimer strychninu. Patří mezi alkaloidy odvozené od tryptofanu.
Reference
- ↑ https://medicalxpress.com/news/2021-07-muscle-largely-ineffective-pain.html - Muscle relaxants largely ineffective for low back pain
- ↑ SIRDALUD 2 MG TBL NOB 30 - Léky jasně. lekyjasne.cz [online]. 2023-11-08 [cit. 2023-11-11]. Dostupné online.
- ↑ SIRDALUD 4 MG TBL NOB 30 - Léky jasně. lekyjasne.cz [online]. 2023-11-08 [cit. 2023-11-11]. Dostupné online.
Literatura
- Lincová, Farghali: Základní a aplikovaná farmakologie. Galén 2002.
- Katzung, B.G.: Základní a klinická farmakologie. H&H 2006.
- Hynie, Sixtus: Farmakologie v kostce. Triton 2001.
- Silbernagl, Stefan: Atlas fyziologie člověka. Grada 2004.
- Tomko, Jozef: Farmakognózia. Osveta 1999.
Externí odkazy
 Obrázky, zvuky či videa k tématu myorelaxans na Wikimedia Commons
Obrázky, zvuky či videa k tématu myorelaxans na Wikimedia Commons
Média použitá na této stránce
Chemical structure of tubocurarine (cation part)