Myosin
Myosin, někdy také myozin nebo svalník (zast.), je označení pro skupinu proteinů řazených mezi tzv. molekulární motory, které jsou za pomoci hydrolýzy ATP schopny vytvářet sílu a aktivní směrovaný pohyb v buňce. Vážou se na aktin, spolu s nímž a dalšími proteiny jsou zodpovědné za svalový stah; dále se také podílejí na aktivním vnitrobuněčném transportu váčků a pohybu membrán. Vyskytují se u eukaryotických organismů, včetně např. rostlin.[1]
Struktura a typy
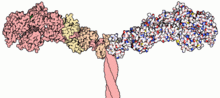
Dodnes bylo odhaleno asi 150 genů kódujících myosiny a tvořících tzv. myosinovou superrodinu. Rozdělují se do asi 18 tříd označovaných římskými číslicemi I–XVIII. Všechny mají přibližně společnou strukturu: globulární hlavičku, jež se váže na aktin a též hydrolyzuje ATP, „krk“ s regulačními místy pro vazbu kalmodulinu a konečně dlouhý ocásek. Právě ocáskovitá („tail“) doména vykazuje nejvyšší rozmanitost a je schopná se vázat na celou řadu buněčných struktur.[1]
- Myosin I – monomerický myosin, který má vazebná místa pro váčky – transport po aktinových vláknech
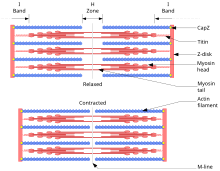
- Myosin II – struktura tvořena více molekulami – transport membránových struktur, patří sem však i svalové myosiny zajišťující svalový stah
Odkazy
Reference
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu myosin na Wikimedia Commons
Obrázky, zvuky či videa k tématu myosin na Wikimedia Commons - Myosin Video Archivováno 2. 6. 2008 na Wayback Machine. Vnitrobuněčný transport – animace, jak se myosin pohybuje
Média použitá na této stránce
Autor:
David Richfield (User:Slashme) When using this image in external works, it may be cited as follows:
- Richfield, David (2014). "Medical gallery of David Richfield". WikiJournal of Medicine 1 (2). DOI:10.15347/wjm/2014.009. ISSN 2002-4436.
Sarcomere
Autor: David S. Goodsell of The Scripps Research Institute, Licence: Attribution
Part of the myosin structure, atoms in the heavy chain are colored red on the left-hand side, and atoms in the light chains are colored orange and yellow. From: Houdusse, A., Kalabokis, V. N., Himmel, D., Szent-Gyorgyi, A. G., Cohen, C.: Atomic structure of scallop myosin subfragment S1 complexed with MgADP: a novel conformation of the myosin head. Cell 97 pp. 459 (1999)

