NMDA receptor
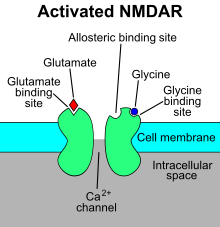
Na N-metyl-D-aspartát receptor (také známý jako NMDA receptor nebo NMDAR), je glutamátový receptor a iontový kanál (převážně Ca2+) v nervové buňce. NMDA receptor je jedním ze tří typů ionotropních glutamátových receptorů vedle AMPA a kainátových receptorů. Aktivuje se, když se naváže glutamát a glycin (nebo D-serin) a umožní pozitivně nabitým iontům proudit skrz buněčnou membránu.[2] NMDA receptor je důležitý pro regulaci synaptické plasticity a paměťové funkce.[3]
NMDAR je specifický typ ionotropního glutamátového receptoru.[4] Název NMDA receptoru pochází od zkratky názvu jeho agonisty N-methyl-D-aspartátu (NMDA), který se selektivně váže na NMDA receptor a nikoli na jiné glutamátové receptory. Aktivace NMDA receptorů vede k otevření iontového kanálu, který je neselektivní pro kationty s kombinovaným reverzním potenciálem okolo 0 mV. Při otevírání a zavírání iontového kanálu je především řízen navázáním ligandu, aktuální průtok přes iontový kanál je napěťově řízený. Extracelulární ionty hořčíku (Mg2+) a zinku (Zn2+) se mohou vázat na konkrétní místa na receptoru, a tím blokovat průchod ostatních kationtů přes otevřený iontový kanál. Depolarizace buňky uvolňuje a vypuzuje ionty Mg2+ a Zn2+ z pórů, což umožňuje napěťově řízený tok iontů sodíku (Na+) a malého množství vápníku (Ca2+) do buňky a draslíku (K+) ven z buňky.[5][6][7][8]
Ca2+ tok přes NMDARs je považován za rozhodující v synaptické plasticitě, buněčného mechanismus pro učení a paměť. Otevírání a zavírání (gating) NMDA receptoru je komplexní. I přesto, že je to v první řadě ligandem řízený kanál, vykazuje i slabší napěťově závislou modulaci. Ligandové řízení vyžaduje spoluaktivaci dvou ligandů: glutamátu a dále buď D-serinu nebo glycinu.[9] Napěťově závislý proud kanálem je způsoben především vazbou iontů Mg2+ nebo Zn2+ na protein.
Aktivita NMDA receptoru je ovlivněna mnoha psychoaktivními drogami, jako je fencyklidin (PCP), alkohol (ethanol) a dextromethorfanu (DXM). Anestetické a analgetické účinky léků typu ketamin a oxid dusný jsou způsobeny částečně také díky vazbě na NMDA receptory. Roku 1989 byl memantin uznán jako nekompetitivní antagonista NMDA receptoru, vstupující do kanálu receptoru po jeho aktivaci, a tím blokující tok iontů.[10][11][12]
NMDA receptorové kanály hrají důležitou roli v synaptické plasticitě a synaptickém vytváření hlubší paměti, učení a formování neuronových sítí během vývoje v centrálním nervovém systému (CNS). Přehnaná aktivace receptoru způsobuje nadměrný příliv Ca2+ a může vést k excitotoxicitě, která je zahrnuta do některých neurodegenerativních poruch. Zablokování NMDA receptorů by proto mohlo být teoreticky užitečné v léčbě těchto onemocnění.[13][14][15]
Nicméně hypofunkce NMDA receptorů (kvůli nedostatku glutathionu nebo z jiných příčin) způsobuje snížení synaptické plasticity[16] a může mít i další negativní následky. Hlavním problémem využití antagonistů NMDA receptorů pro účely neuroprotekce je, že fyziologická aktivita NMDAR je nezbytná pro normální funkci neuronů. Úspěšné klinické použití těchto antagonistů by vyžadovalo blokaci pouze nadměrné aktivace bez zasahování do normální funkce.[17]
NMDA receptor

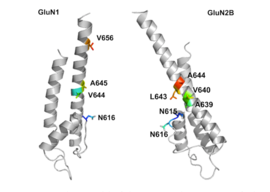
NMDAR je proteinový receptor sestávající z rec. pro glutamát a iontového kanálu a je aktivován navázáním glycinu a glutamátu.[18] Receptor je heteromerický komplex, který spolupracuje s mnoha intracelulárními proteiny skrze tří různé podjednotky: NR1, NR2 a NR3. NR1 má osm různých podjednotek generovaných alternativním přepisem jednoho genu. K dispozici jsou čtyři různé NR2 podjednotky (A-D) plus NR3A a NR3B podjednotky. Šest samostatných genů kóduje NR2 a NR3.[19][20] Všechny podjednotky mají společnou membránovou topologii, které dominuje velký extracelulární N-konec, oblast membrány zahrnující tři transmembránové segmenty: znovuvstupující pórovou smyčku (reentrant pore loop), extracelulární smyčku mezi transmembránovými segmenty, které nejsou strukturálně dobře známé, a intracelulární C-konec; které se liší velikostí v závislosti na podjednotce a poskytují mnoho míst pro interakce s mnoha intracelulárními proteiny.[21] Obrázek 1 ukazuje základní strukturu NR1/NR2 podjednotek, které tvoří vazebné místo pro memantin, Mg2+, MK-801, ketamin a amantadin.
Kinetika receptoru
Receptor působí tonickou anebo fázickou aktivací, za běžných okolností je glutamát rychle (cca 1ms) odstraněn ze synaptické štěrbiny transportéry, tj. fázická aktivace. Při prolongované přítomnosti dochází k tonické aktivaci s podstatně odlišnou biexponenciální kinetikou.
Následuje kalcium- a glycin-dependentní desenzitizace, tj. přechod do inaktivního stavu. Otevírání a desenzitizace je modulována mj. neurosteroidy (např. pregnenolon sulfát) nebo cholesterolem.
NMDA receptory hrají klíčovou roli v indukci LTP (long term potentiation, dlouhodobé potenciace receptorů), metabotropní efekt via druhý posel Ca2+ + detekce koincidencí (blokáda Mg2+ ) s určitými výjimkami, např. v hyppocampu , kde je non-NMDA-dependentní forma LTP.
Vliv na excitotoxicitu přes aktivaci receptorů s GluN2B pro-apoptotickou , potenciální využití ifenprodilu jako neuroprotektiva), zejména extrasynapticky a aktivace receptorů s GluN2A za fyziologických okolností je anti-apoptotická. Antagonisty jsou ketamin, fencyclidin, dizocilpin, AP5, ethanol, KYNA a memantin.
Reference
V tomto článku byl použit překlad textu z článku NMDA receptor na anglické Wikipedii.
- ↑ Laube B, Hirai H, Sturgess M, Betz H, Kuhse J. Molecular determinants of agonist discrimination by NMDA receptor subunits: analysis of the glutamate binding site on the NR2B subunit. Neuron. 1997, s. 493–503. DOI 10.1016/S0896-6273(00)81249-0. PMID 9115742.
- ↑ FURUKAWA, Hiroyasu; SINGH, Satinder K; MANCUSSO1, Romina; GOUAUX, Eric. Subunit arrangement and function in NMDA receptors. Nature. November 2005, s. 185–92. DOI 10.1038/nature04089. PMID 16281028.
- ↑ Li F, Tsien JZ. Memory and the NMDA receptors. N. Engl. J. Med.. 2009, s. 302–3. DOI 10.1056/NEJMcibr0902052. PMID 19605837.
- ↑ Moriyoshi K, Masu M, Ishii T, Shigemoto R, Mizuno N, Nakanishi S. Molecular cloning and characterization of the rat NMDA receptor.. Nature. November 1991, s. 31–37. Dostupné online. DOI 10.1038/354031a0. PMID 1834949.
- ↑ Dingledine R, Borges K, Bowie D, Traynelis SF. The glutamate receptor ion channels. Pharmacol. Rev.. March 1999, s. 7–61. Dostupné online. PMID 10049997.
- ↑ Liu; ZHANG, J. Recent development in NMDA receptors. Chinese medical journal. 2000, s. 948–56. PMID 11775847.
- ↑ Cull-Candy S, Brickley S, Farrant M. NMDA receptor subunits: diversity, development and disease. Curr. Opin. Neurobiol.. June 2001, s. 327–35. Dostupné online. DOI 10.1016/S0959-4388(00)00215-4. PMID 11399431.
- ↑ Paoletti P, Neyton J. NMDA receptor subunits: function and pharmacology. Curr Opin Pharmacol. February 2007, s. 39–47. DOI 10.1016/j.coph.2006.08.011. PMID 17088105.
- ↑ Kleckner NW, Dingledine R. Requirement for glycine in activation of NMDA-receptors expressed in Xenopus oocytes. Science. August 1988, s. 835–7. DOI 10.1126/science.2841759. PMID 2841759.
- ↑ Johnson J.W., Kotermanski S.E. Mechanism of action of memantine. Current Opinion in Pharmacology. 2006, s. 61–67. DOI 10.1016/j.coph.2005.09.007.
- ↑ DOMINGUEZ, Evangelyn; CHIN, Ting-Yu; CHEN, Chih-Ping; WU, Tzong-Yuan. Management of moderate to severe Alzheimer's disease: Focus on memantine. Taiwanese Journal of Obstetrics and Gynecology. December 2011, s. 415–423. DOI 10.1016/j.tjog.2011.10.004.
- ↑ CHEN, Huei-Sheng Vincent; LIPTON, Stuart A. The chemical biology of clinically tolerated NMDA receptor antagonists. Journal of Neurochemistry. June 2006, s. 1611–1626. DOI 10.1111/j.1471-4159.2006.03991.x. PMID 16805772.
- ↑ Kemp J. A., McKernan R. M. NMDA receptor pathways as drug targets. Nature Neuroscience. 2002, s. 1039–1042. DOI 10.1038/nn936.
- ↑ Lipton S.A. Paradigm shift in neuroprotection by NMDA receptor blockade: Memantine and beyond. Nature Reviews Drug Discovery. 2006, s. 160–170. DOI 10.1038/nrd1958. PMID 16424917.
- ↑ KOCH, Horst; SZECSEY, Alexander; HAEN, Ekkehard. NMDA-antagonism (Memantine): An Alternative Pharmacological Therapeutic Principle in Alzheimers and Vascular Dementia. Current Pharmaceutical Design. 1 January 2004, s. 253–259. DOI 10.2174/1381612043386392.
- ↑ STEULLET, P; NEIJT, H.C; CUÉNOD, M; DO, K.Q. Synaptic plasticity impairment and hypofunction of NMDA receptors induced by glutathione deficit: Relevance to schizophrenia. Neuroscience. 2006, s. 807–19. DOI 10.1016/j.neuroscience.2005.10.014. PMID 16330153.
- ↑ LIPTON, Stuart A. Failures and successes of NMDA receptor antagonists: Molecular basis for the use of open-channel blockers like memantine in the treatment of acute and chronic neurologic insults. NeuroRx. January 2004, s. 101–110. DOI 10.1602/neurorx.1.1.101. PMID 15717010.
- ↑ FURUKAWA, Hiroyasu; SINGH, Satinder K; MANCUSSO, Romina; GOUAUX, Eric. Subunit arrangement and function in NMDA receptors. Nature. 10 November 2005, s. 185–192. DOI 10.1038/nature04089. PMID 16281028.
- ↑ Loftis J. M., Janowsky A. The N-methyl-D-aspartate receptor subunit NR2B: localization, functional properties, regulation, and clinical implications. Pharmacol Ther. 2003, s. 55–85. DOI 10.1016/s0163-7258(02)00302-9. PMID 12493535.
- ↑ KRISTIANSEN, Lars V; HUERTA, Ibone; BENEYTO, Monica; MEADOR-WOODRUFF, James H. NMDA receptors and schizophrenia. Current Opinion in Pharmacology. February 2007, s. 48–55. DOI 10.1016/j.coph.2006.08.013. PMID 17097347.
- ↑ LIMAPICHAT, Walrati; YU, Wesley Y.; BRANIGAN, Emma; LESTER, Henry A.; DOUGHERTY, Dennis A. Key Binding Interactions for Memantine in the NMDA Receptor. ACS Chemical Neuroscience. 20 February 2013, s. 255–260. DOI 10.1021/cn300180a.
Externí odkazy
 Obrázky, zvuky či videa k tématu NMDA receptor na Wikimedia Commons
Obrázky, zvuky či videa k tématu NMDA receptor na Wikimedia Commons
Média použitá na této stránce
Autor: Tinktura1, Licence: CC BY-SA 4.0
The transmembrane segments of the NMDA receptor, showing the NR1/NR2B subunit and binding pockets.


