Naftalen
| Naftalen | |
|---|---|
 | |
 | |
| Obecné | |
| Systematický název | naftalen |
| Anglický název | naphthalene |
| Sumární vzorec | C10H8 |
| Vzhled | bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 91-20-3 |
| EC-no (EINECS/ELINCS/NLP) | 202-049-5 |
| Indexové číslo | 601-052-00-2 |
| Vlastnosti | |
| Molární hmotnost | 128,170 52 g/mol |
| Teplota tání | 80 °C |
| Teplota varu | 218 °C |
| Hustota | 1,14 g/cm³ |
| Rozpustnost ve vodě | 30 mg/l |
| Bezpečnost | |
| [1] Varování[1] | |
| H-věty | H351 H302 H410 |
| R-věty | R22 R40 R50/53 |
| S-věty | (S2) S36/37 S46 S60 S61 |
Některá data mohou pocházet z datové položky. | |
Naftalen (též naftalín) je bílá, krystalická, aromatická látka, známá jako hlavní přísada kuliček proti molům (naftalínu). Naftalen je těkavá, hořlavá, zdraví škodlivá látka se slabě narkotickými účinky. Molekula se skládá ze dvou benzenových jader (kruhů), naftalen je nejjednodušším polycyklickým uhlovodíkem. Získává se z černouhelného dehtu. Převádí se na ftalanhydrid, který se dále používá při výrobě plastů, barviv a organických rozpouštědel. Používá se též jako dezinfekce nebo insekticid[2], hlavně na moly. Jako náhražka naftalínových kuliček se dnes spíše používá p-dichlorbenzen. Naftalen snadno sublimuje.
Historie
V letech 1819–1820 oznámili dva chemici objev bílé krystalické látky se štiplavým zápachem. Látka byla objevena při destilaci černouhelného dehtu. V roce 1821 John Kidd popsal další vlastnosti této neznámé látky a způsoby její produkce a navrhl název naftalín. Bod tání naftalenu se pohybuje mezi 79 a 83 °C. Hustota je 1,14 g/cm³. Naftalen je člověku i přírodě škodlivý. Empirický vzorec naftalenu (C5H4) objevil v roce 1826 Michael Faraday. Strukturu dvou spojených benzenových jader navrhl Emil Erlenmeyer v roce 1866 a o tři roky později ji potvrdil Carl Graebe.
Struktura a reaktivita
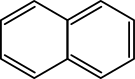
Molekula naftalenu se skládá ze dvou spojených benzenových jader. Podle toho je klasifikován jako polyjaderný aromatický uhlovodík (PAH). Naftalen má tři rezonanční struktury a dva druhy rovnocenných vodíků. Typ alfa se nachází v polohách 1, 4, 5 a 8, typ beta v polohách 2, 3, 6 a 7.
Na rozdíl od benzenu nejsou vazby mezi jednotlivými uhlíky stejně dlouhé. Vazba mezi C1–C2, C3–C4, C5–C6 a C7–C8 měří 1,36 Å, vazby mezi ostatními uhlíky jsou dlouhé 1,42 Å. Toto bylo ověřeno rentgenovou difrakcí a lze to již očekávat z rezonančních struktur, kde vazby C1–C2, C3–C4, C5–C6 a C7–C8 jsou dvojné ve dvou ze tří struktur.

Stejně jako benzen podléhá naftalen elektrofilní aromatické substituci (SEAr). Pro některé SEAr je naftalen reaktivnější než benzen. Podléhá Friedelově-Craftsově alkylaci, může také reagovat s alkeny a alkoholy za katalýzy kyselinou sírovou.
Naftalen může být za vysokého tlaku hydrogenován na 1,2,3,4-tetrahydronaftalen, což je látka používaná jako rozpouštědlo a prodávající se pod názvem tetralin. Další hydrogenovanou formou je dekalin (též bicyklo[4.4.0]dekan, nebo cis-dekalin). Oxidací naftalenu (pomocí O2 za katalýzy V2O5) získáme anhydrid kyseliny ftalové.

Produkce
Nejvíce naftalenu se získá z černouhelného dehtu. V letech 1960–1990 se naftalen získával také při frakční destilaci ropy.
Naftalen je nejhojnější samostatná složka černouhelného dehtu. Složení černouhelného dehtu závisí na uhlí, ze kterého se získává. Obsah naftalenu bývá kolem 10 hmotnostních %. Při průmyslové výrobě (destilace dehtu) se získává olej, který obsahuje až 50 hmotnostních %. Tento olej se promývá kapalným hydroxidem sodným, aby se z něj odstranily kyselé složky, především fenoly, dále pak kyselinou sírovou pro odstranění zásaditých složek. Jedná se o frakční destilaci, při které je naftalen odizolován. Výsledkem celého procesu je 95 hmotnostních % surového naftalenu. Hlavní vedlejší složkou (nečistotou) je thionaftalen. Naftalen získaný z ropy je obvykle čistší než ten z černouhelného dehtu. Pokud není naftalen dostatečně čistý, může se dočistit rekrystalizací v organických rozpouštědlech.
Stopové množství naftalenu je produkováno magnoliemi a některými typy vysoké zvěře.[zdroj?]
Hlavním výrobcem naftalenu v České republice je firma DEZA ve Valašském Meziříčí.[3]
Použití
V domácnostech se naftalen nejvíce používá jako vykuřovací prostředek nebo jako pevné kuličky proti molům. V hermeticky uzavřených obalech jsou obsaženy naftalenové kuličky. Naftalenové výpary zabíjí larvy molů, které ničí oblečení.
V minulosti byl naftalen také podáván dobytku, aby zahubil různé parazitující červy.
Větší množství naftalenu se používá jako výchozí látka pro výrobu dalších chemických látek, například anhydridu kyseliny ftalové, který se vyrábí z o-xylenu a ten z naftalenu. Další deriváty naftalenu zahrnují sulfonované alkyl-naftaleny (tenzidy) a karbaryly (insekticidy). Substituované naftaleny v kombinaci s elektron-donorovými funkčními skupinami (alkoholy, amidy) nebo s elektron-akceptorními funkčními skupinami (kyselina sírová) jsou meziprodukty při výrobě barviv. Hydrogenované formy naftalenu Tetralin a Dekalin se používají jako slabě těkavá organická rozpouštědla.
Zdravotní rizika
Do těla vstupuje vdechováním, hlavně u dětí je možnou cestou kontakt s pokožkou nebo tkáněmi oka. Způsobuje bolesti hlavy, zvracení a zvýšené pocení, případně křeče či průjmy. Naftalen také způsobuje rozklad červených krvinek (hemolýza) a nekrózu jater, které doprovází chudokrevnost, horečka, zvýšení počtu bílých krvinek (leukocytóza), žloutenka a porucha funkce jater. Největší nebezpečí hrozí u těhotných žen a kojenců, neboť látka prochází placentou a proniká i do mateřského mléka.
Lidé, hlavně děti, se mohou s naftalenem dostat do styku např. při používáni kuliček proti molům nebo používáním deodorantů obsahujících naftalen. Příznaky toho stavu jsou únava, nechutenství, nervozita a bledá pokožka.
Havárie
Koncem října 2008 uniklo asi 20 tun naftalenu z podniku DEZA Valašské Meziříčí, ale firma problém zamlčela. Problém se začal řešit, až když si obyvatelé v okolí stěžovali na silný zápach. Uniklý naftalen zčásti ztuhl v kanalizaci, kterou ucpal. Vedení města Valašské Meziříčí je situací znepokojeno, i proto s podnikem uzavřel dohodu zahrnující povinnost vzájemně se informovat.[4]
Odkazy
Související články
- Toluen
- Xylen
- Nitrobenzen
- Anilin
- Styren
- Fenol
- Benzen
- Antracen
- 1,2-dihydronaftalen
- Tetrahydronaftalen
- Dekahydronaftalen
Reference
- ↑ a b Naphthalene. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ BUCKPITT, Alan; KEPHALOPOULOS, Stylianos; KOISTINEN, Kimmo, et al. WHO Guidelines for Indoor Air Quality: Selected Pollutants. Geneva: World Health Organization, 2010. ISBN 978-9289002141.
- ↑ Budoucnost bez jedů. bezjedu.arnika.org [online]. [cit. 2009-08-16]. Dostupné v archivu pořízeném dne 2009-08-15.
- ↑ Valašskomeziříčská chemička Deza tajila únik naftalenu Archivováno 14. 2. 2009 na Wayback Machine., ČT24, 8. 11. 2008
Externí odkazy
 Obrázky, zvuky či videa k tématu naftalen na Wikimedia Commons
Obrázky, zvuky či videa k tématu naftalen na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
Skeletal formula of Naphthalene
Naphthalene is an organic compound with formula C
10H 8. It is the simplest polycyclic aromatic hydrocarbon, and is a white crystalline solid with a characteristic odor that is detectable at concentrations as low as 0.08 ppm by mass. As an aromatic hydrocarbon, naphthalene's structure consists of a fused pair of benzene rings. It is best known as the main ingredient of traditional mothballs.
Unlike benzene, the carbon–carbon bonds in naphthalene are not of the same length. The bonds C1–C2, C3–C4, C5–C6 and C7–C8 are about 1.36 Å (136 pm) in length, whereas the other carbon–carbon bonds are about 1.42 Å (142 pm) long. This difference, which was established by X-ray diffraction, is consistent with the valence bond model of bonding in naphthalene that involves three resonance structures (as shown); whereas the bonds C1–C2, C3–C4, C5–C6 and C7–C8 are double in two of the three structures, the others are double in only one.Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances









