O-fenylendiamin
| o-fenylendiamin | |
|---|---|
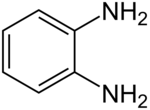 Strukturní vzorec | |
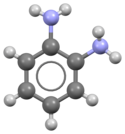
 Tyčinkový model molekuly | |
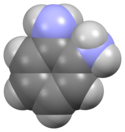
 Prostorový model molekuly | |
| Obecné | |
| Systematický název | Benzen-1,2-diamin |
| Ostatní názvy | o-fenylendiamin, ortho-fenylendiamin |
| Funkční vzorec | C6H4(NH2)2 |
| Sumární vzorec | C6H8N2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 107-15-3 |
| EC-no (EINECS/ELINCS/NLP) | 202-430-6 |
| PubChem | 7243 |
| ChEBI | 34043 |
| SMILES | Nc1ccccc1N |
| InChI | 1S/C6H8N2/c7-5-3-1-2-4-6(5)8/h1-4H,7-8H2 |
| Číslo RTECS | SS7875000 |
| Vlastnosti | |
| Molární hmotnost | 108,14 g/mol |
| Teplota tání | 102 až 104 °C (375 až 377 K)[1] |
| Teplota varu | 257 °C (530 K)[1] |
| Hustota | 1,031 g/cm3 |
| Disociační konstanta pKa | 0,80 (dvakrát protonovaná forma, 20 °C) 4,57 (konjugovaná kyselina, 20 °C) |
| Rozpustnost ve vodě | rozpustný v horké vodě (0,4 g/100 ml při 35 °C[1]) |
| Tlak páry | 1,3 Pa (20 °C)[1] |
| Měrná magnetická susceptibilita | −6,66×105 μm3/g |
| Bezpečnost | |
| [2] Nebezpečí[2] | |
| H-věty | H301 H312 H317 H319 H332 H341 H351 H400 H410 |
| P-věty | P201 P202 P261 P264 P270 P271 P272 P273 P280 P281 P301+310 P302+352 P304+340 P305+351+338 P308+313 P312 P321 P322 P330 P333+313 P337+313 P363 P405 P501[1] |
| Teplota vzplanutí | 156 °C (429 K)[1] |
Některá data mohou pocházet z datové položky. | |
o-Fenylendiamin (ortho-fenylendiamin) systematický název benzen-1,2-diamin, je organická sloučenina se vzorcem C6H4(NH2)2, která patří mezi aromatické diaminy. Je strukturním izomerem m-fenylendiaminu a p-fenylendiaminu.
Výroba a příprava
o-Fenylendiamin se obvykle vyrábí reakcí 2-nitrochlorbenzenu s amoniakem a následnou hydrogenací vzniklého 2-aminonitrobenzenu:[3]
- ClC6H4NO2 + 2 NH3 → H2NC6H4NO2 + NH4Cl
- H2NC6H4NO2 + 3 H2 → H2NC6H4NH2 + 2 H2O
V laboratoři se připravuje přímo redukcí 2-aminonitrobenzenu práškovým zinkem v ethanolu a následným přečištěním za vzniku hydrochloridu diaminu.[4] Tento priodukt na vzduchu tmavne; nečistoty z něj lze odstranit přidáním dithioničitanu sodného a aktivního uhlí do horkého vodného roztoku, následovaným pomalým chlazením vedoucím ke krystalizaci.
Reakce a použití
o-Fenylendiamin kondenzuje s aldehydy a ketony. Reakcemi s karboxylovými kyselinami a jejich deriváty z něj vznikají benzimidazoly; podobným způsobem se vyrábí herbicid benomyl. Produktem reakce o-fenylendiaminu s dimethyloxalátem je chinoxalindion. Kondezacemi s xanthátovými estery se tvoří merkaptoimidazoly, používané jako antioxidanty ve výrobcích z pryže. Působením kyseliny dusité na o-fenylendiamin vzniká benzotriazol, používaný jako inhibitor koroze. Kondenzacemi substituovaných o-fenylendiaminů s diketony se vyrábějí mnohá léčiva.[5]
Fenylendiaminy jsou významnými prekurzory ligandů. Deriváty Schiffových bází, odvozené například od salicylaldehydu, jsou velmi dobrými ligandy. Oxidací komplexů kov-fenylendiamin vznikají diiminové sloučeniny, které mají výrazné zbarvení a často se vyskytují v několika různých oxidačních stavech.[6]
Bezpečnost
Střední smrtelná dávka (LD50) o-fenylendiaminu ve vodném roztoku je 44 mg/l, tedy asi 1000krát vyšší než u p-fenylendiaminu. S aniliny se obvykle nakládá jako s karcinogeny. V mnoha oblastech byl o-fenylendiamin nahrazen bezpečnějšími látkami, jako je například 3,3',5,5'-tetramethylbenzidin.
Reference
V tomto článku byl použit překlad textu z článku o-Phenylenediamine na anglické Wikipedii.
- ↑ a b c d e f https://pubchem.ncbi.nlm.nih.gov/compound/7243
- ↑ a b O-Phenylenediamine. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Robert A. Smiley "Phenylene- and Toluenediamines" in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. DOI:10.1002/14356007.a19_405
- ↑ E. L. MARTIN. o-Phenylenediamine. Org. Synth.. 1943. Dostupné online. (anglicky); Coll. Vol.. S. 501. (anglicky)
- ↑ Heterocyclic quinones. Quinoxaline-5,6 and 5,8 diones, potential antitumoral agents. European Journal of Medicinal Chemistry. 1981, s. 545–550.
- ↑ L. F. Warren. Synthesis of [M'-N4] and [M'-N6] Complexes Based on o-Benzoquinone Diimine with Cobalt, Iron, and Ruthenium. Inorganic Chemistry. 1977, s. 2814–2819.
Externí odkazy
 Obrázky, zvuky či videa k tématu O-fenylendiamin na Wikimedia Commons
Obrázky, zvuky či videa k tématu O-fenylendiamin na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for substances hazardous to human health.
Space-filling model of the o-Phenylenediamine molecule (also known as benzene-1,2-diamine), i.e. C6H4(NH2)2, as found in the crystal structure.
Structure determined by X-ray crystallography reported in Acta Cryst. (2010). C66, o198–o201 (CSD Entry: BAGFIY01).
Colour code:
- Carbon, C: dark-grey
- Hydrogen, H: light-grey
- Nitrogen, N: light-blue
Ball-and-stick model of the o-Phenylenediamine molecule (also known as benzene-1,2-diamine), i.e. C6H4(NH2)2, as found in the crystal structure.
Structure determined by X-ray crystallography reported in Acta Cryst. (2010). C66, o198–o201 (CSD Entry: BAGFIY01).
Colour code:
- Carbon, C: dark-grey
- Hydrogen, H: light-grey
- Nitrogen, N: light-blue
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances