Octan palladnatý
| Octan palladnatý | |
|---|---|
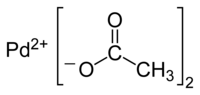 Strukturní vzorec | |
 Model struktury trimerní formy | |
 Model struktury polymerní formy | |
| Obecné | |
| Systematický název | ethanoát palladnatý |
| Triviální název | octan palladnatý |
| Anglický název | Palladium(II) acetate |
| Funkční vzorec | (CH3COO)2Pd |
| Sumární vzorec | C4H6O4Pd |
| Vzhled | hnědožlutá pevná látka (trimer) světle růžový prášek (polymer) |
| Identifikace | |
| Registrační číslo CAS | 3375-31-3 |
| PubChem | 167845 |
| SMILES | [Pd+2].[O-]C(=O)C.[O-]C(=O)C |
| InChI | 1S/2C2H4O2.Pd/c2*1-2(3)4;/h2*1H3,(H,3,4);/q;;+2/p-2 |
| Číslo RTECS | AJ1900000 |
| Vlastnosti | |
| Molární hmotnost | 224,50 g/mol |
| Teplota rozkladu | 205 °C (478 K) |
| Rozpustnost ve vodě | slabě rozpustný |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Octan palladnatý je organická sloučenina, palladnatá sůl kyseliny octové. Je považován za reaktivnější než odpovídající sloučenina platiny. Je rozpustný v mnoha organických rozpouštědlech a často se používá jako katalyzátor organických reakcí a jako prekurzor dalších palladnatých katalyzátorů.
Struktura
I když má tato sloučenina poměr atomů palladia a octanových ligandů 1:2, jak odpovídá jejich oxidačním číslům, skutečná molekulární struktura závisí na způsobu přípravy.
Tak jak byl připraven Wilkinsonem a pomocníky roku 1965 a v roce 1970 studován Skapským a Smartem pomocí jednokrystalové rentgenové difrakce, jde o hnědožlutou pevnou látku krystalizující v jednoklonných vrstvách. Bylo zjištěno, že jeho struktura je trimerní, složená z rovnostranných trojúhelníků, kde je každý atom Pd navázán na dvě acetátové skupiny. Každý atom kovu zaujímá přibližně čtvercovou rovinnou koordinaci.[2][3]
Octan palladnatý připravený lehce odlišným způsobem byl izolován jako světle růžový prášek, u něhož byla rentgenovou difrakcí zjištěna struktura v podobě dlouhých řetězců atomů palladia, z nichž je každý propojen se sousední dvojicí acetátových můstků, kde je koordinační geometrie kolem každého atomu palladia čistě čtvercově rovinná.[4]
Příprava
Octan palladnatý může být připraven v trimerní formě průtokem horké koncentrované kyseliny octové a kyseliny dusičné skrz houbovité palladium. Přebytečné množství houbovitého palladia nebo vyšší tok plynného dusíku zabraňuje kontaminaci produkty obsahujícími dusitanový ligand místo jednoho z acetátů (Pd3(OAc)5NO2).[5][6]
- Pd + 4 HNO3 → Pd(NO3)2 + 2 NO2 + 2 H2O
- Pd(NO3)2 + 2 CH3COOH → Pd(O2CCH3)2 + 2 HNO3
Tato nitrovarianta má odlišnou rozpustnost a jinou katalytickou aktivitu u mnoha reakcí. Zabránění nebo omezení její tvorby je důležité prospolehlivé používání octanu palladnatého.[7]
Podobně se připravuje propionát palladnatý; ostatní karboxyláty se získávají reakcí octanu palladnatého s odpovídající karboxylovou kyselinou.[2] Rovněž octan palladnatý je možné připravit reakcí jiného palladnatého karboxylátu s kyselinou octovou. Tato výměna ligandů začínající přečištěným karboxylátem je alternativním způsobem získávání octanu palladnatého bez kontaminatních nitrosloučenin.[7]
Reakce
Při zahřívání s alkoholy, nebo delším varu v jiných rozpouštědlech, se tato látka rozkládá na kyselinu octovou a kovové palladium.[2]
Použití
Katalýza
Octan palladnatý je katalyzátorem mnoha organických reakcí u řady druhů sloučenin, jako jsou alkeny, dieny a alkyl-, aryl- a vinylhalogenidy, při nichž se tvoří reaktivní addukty. Π-allyl koordinace a koordinace alkenů na octan palladnatý zahrnuje donaci typu sigma z π-orbitalu alkenu nebo π-allylu za současného zpětného π-navázání na prázdný π* orbital alkenu či π-allylu. Čím větší je sigma donace na kov, tím větší je zpětné navázání. Čím větší je zpětné navázání, tím větší je snížení řádu vazby.[8] Redukce alkenů nebo π-allylů octanem palladnatým obrací reaktivitu organického ligandu tím, že umožní spíše reakce s nukleofily než s elektrofily.[9]
Příklady reakcí katalyzovaných octanem palladnatým jsou:
- Vinylace, například Heckova reakce
- Přesmyk acyklických dienů, například Copeův přesmyk
- Karbonylační reakce jako je tvorba esterů z aryljodidů adicí oxidu uhelnatého a alkoholu nebo fenolu[10]
- Redukční aminace aldehydů nebo ketonů za použití mravenčanu draselného[11]
- Wackerův proces: oxidace ethenu ve vodě za vzniku acetaldehydu (prekurzoru polyvinylacetátu, běžné složky lepidel)
- Buchwaldova-Hartwigova aminace arylhalogenidů/pseudohalogenidů s alkyl- nebo arylaminy[12]
Tato látka převádí arylbromidy na aryltrimethylsilany, důležité funkční skupiny v řadě organických sloučenin jako je fungicid „Latitude“:
- RC6H4Br + Si2(CH3)6 → RC6H4Si(CH3)3 + Si(CH3)3Br
Octan palladnatý je kompatibilní s elektronovými vlastnostmi arylbromidů a tato metoda na rozdíl od mnoha jiných způsobů syntézy nevyžaduje vybavení pro vysoké tlaky.[13]
Prekurzor ostatních sloučenin palladia
Octan palladnatý se používá k tvorbě dalších palladnatých sloučenin; například fenylpalladiumacetát, používaný k izomerizaci allylalkoholů, se získává následující reakcí:
- Hg(C6H5)(CH3COO) + Pd(CH3COO)2 → Pd(C6H5)(O2CCH3) + Hg(O2CCH3)2
Octan palladnatý také reaguje s acetylacetonem (ligand „acac“) za vzniku acetylacetonátu palladnatého (Pd(acac)2), monomerní molekuly, která je prekurzorem kovového palladia.
Světlem či teplem se octan palladnatý redukuje za vzniku tenkých vrstev palladia a může vytvářet nanovlákna a koloidy.[5]
Odkazy
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu octan palladnatý na Wikimedia Commons
Obrázky, zvuky či videa k tématu octan palladnatý na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Palladium(II) acetate na anglické Wikipedii.
- ↑ a b Palladium(II) acetate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ a b c T. A. Stephenson; S. M. Morehouse; A. R. Powell; J. P. Heffer and G. Wilkinson. 667. Carboxylates of palladium, platinum, and rhodium, and their adducts. Journal of the Chemical Society (Resumed). 1965, s. 3632. DOI 10.1039/jr9650003632. (anglicky)
- ↑ Skapski, A C.; M. L. SMART. The Crystal Structure of Trimeric Palladium(II) Acetate. J. Chem. Soc. D. 1970, s. 658b–659. DOI 10.1039/C2970000658b. (anglicky)
- ↑ Kirik, S.D.; MULAGALEEV, S.F.; BLOKHIN, A.I. [Pd(CH 3 COO) 2 ] n from X-ray powder diffraction data. Acta Crystallogr. C. 2004, s. m449-m450. DOI 10.1107/S0108270104016129. (anglicky)
- ↑ a b Bakhmutov, V. I.,; BERRY, J. F.; COTTON, F. A.; IBRAGIMOV, S.; MURILLO, C. A. Non-Trivial Behavior of Palladium(II) Acetate. Dalton Transactions. 2005, s. 1989–1992. DOI 10.1039/b502122g. PMID 15909048. (anglicky)
- ↑ High Purity Homogeneous Catalyst [online]. Engelhard, September 2005 [cit. 2006-02-24]. Dostupné v archivu pořízeném dne 17 March 2006. (anglicky)
- ↑ a b RITTER, Stephen K. Chemists introduce a user's guide for palladium acetate. Chemical & Engineering News. May 2, 2016, s. 20-21. (anglicky)
- ↑ Toreki, R. "Allyl Ligands." The Organometallic HyperTextBook. 20 Nov. 2003. Chemglass. 01 Apr. 2006<http://www.ilpi.com/organomet/allyl.html>.
- ↑ Suggs, J W. "Palladium: Organometallic Chemistry." Encyclopedia of Inorganic Chemistry. Ed. R B. King. 8 vols. Chichester: Wiley, 1994.
- ↑ NIKITIN, Kirill V.; ANDRYUKHOVA, N.P.; BUMAGIN, N.A.; BELETSKAYA, I.P. Synthesis of Aryl Esters by Pd-catalysed Carbonylation of Aryl Iodides. Mendeleev Communications. 1991, s. 129–131. DOI 10.1070/MC1991v001n04ABEH000080. (anglicky)
- ↑ Basu, B., Satadru J., Mosharef H. B., and Pralay D. A Simple Protocol for the Direct Reductive Amination of Aldehydes and Ketones Using Potassium Formate and Catalytic Palladium Acetate. ChemInform. 2003, s. 555–557. DOI 10.1002/chin.200330069. (anglicky)
- ↑ Buchwald-Hartwig Cross Coupling Reaction [online]. Organic Chemistry Portal. Dostupné online. (anglicky)
- ↑ Gooben, L J. "Research Area "New Pd-Catalyzed Cross-Coupling Reactions"" 28 Feb. 2006<http://www.mpi-muelheim.mpg.de/kofo/bericht2002/pdf/2.1.8_gossen.pdf Archivováno 12. 7. 2007 na Wayback Machine.>
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Ball-and-stick model of the linear polymeric form of palladium(II) acetate, Pd(OAc)2, as found in the crystal structure reported in Acta Cryst. (2004) C60, m449–m450.
Colour code:
- Carbon, C: grey
- Hydrogen, H: white
- Oxygen, O: red
- Palladium, Pd: greenish-blue
Diagram of the structural formulae of the constituent ions of palladium(II) acetate, Pd(OAc)2.
For the actual structure of the substance when solid, see Category:Crystal structures of palladium(II) acetate.
Structure drawn in ChemBioDraw Ultra 12.0.Ball-and-stick model of the cyclic trimeric form of palladium(II) acetate, Pd(OAc)2, as found in the crystal structure of the hydrate reported in I. J. S. Fairlamb, Angew. Chem. Int. Ed. (2015) 54, 10415-10427.
Colour code:
- Carbon, C: grey
- Hydrogen, H: white
- Oxygen, O: red
- Palladium, Pd: greenish-blue
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for environmentally hazardous substances








