Organofluoridy

A: fluormethan
B: isofluran
C: dichlordifluormethan
D: 1,1,1,2-tetrafluorethan
E: kyselina trifluormethansulfonová
F: polytetrafluorethylen
G: perfluoroktansulfonát (PFOS)
H: fluoruracil
I: fluoxetin
Organofluoridy jsou organické sloučeniny obsahující ve svých molekulách vazby uhlík–fluor. Mají mnoho různých využití, od odpuzování vody po léčiva, chladiva a katalyzátory. Některé z těchto sloučenin přispívají k poškozování ozonové vrstvy a globálnímu oteplování, případně se hromadí v organismech a jsou toxické. Při jejich používání jsou často nutné zvláštní postupy pro nakládání s fluoračními činidly.
Vazba uhlík–fluor
Fluor se v několika ohledech liší od ostatních substituentů vyskytujících se v organických molekulách. Fyzikální i chemické vlastnosti organofluoridů jsou tak mnohdy odlišné od ostatních halogenderivátů.
- Vazba uhlík–fluor je jednou z nejsilnějších v organické chemii, s průměrnou energií okolo 480 kJ/mol[1]. Je tak výrazně silnější než vazby uhlíku s ostatními halogeny (například energie vazeb C-Cl se pohybují kolem 320 kJ/mol[1]), čímž propůjčuje organofluoridům vysokou tepelnou a chemickou stálost.
- Tato vazba je krátká (kolem 140 pm[1]).
- Van der Waalsův poloměr fluorového substituentu je pouze 147 pm,[1], tedy nejmenší ze všech heteroatomů a poměrně blízký vodíku (120 pm). Toto společně s malou délkou vazeb C-F vysvětluje, proč se u polyfluorovaných sloučenin nevyskytuje sterické napětí a také je další příčinou tepelné stability. Fluorové substituenty u polyfluorovaných sloučenin účinně stíní uhlíkovou kostru a zabraňují tak atakům různých činidel, což jim dodává vysokou chemickou stabilitu.
- Fluor má nejvyšší elektronegativitu: 3,98.[1] Vazby C-F tak mívají velké dipólové momenty (1,41 D[1]).
- Atomy fluoru mají nejnižší polarizovatelnost: 0,56 10−24 cm3.[1] disperzní síly mezi polyfluorovanými sloučeninami jsou tak velmi slabé a při fluoracích tak často dochází ke snížení teploty varu a navýšení hydrofobicity a lipofobicity oproti ostatním organohalogenidům, které jsou lipofilnější.
Na rozdíl od arylchloridů a arylbromidů arylfluoridy obtížně vytvářejí Grignardova činidla. Arylfluoridy, jako jsou například fluoroaniliny a fluorofenoly, se mnohdy účastní nukleofilních substitucí.
Druhy organofluoridů
Fluorouhlíky
Fluorouhlíky, neboli perfluorované uhlovodíky, obsahují pouze atomy uhlíku a fluoru. Mohou být, v závislosti na molární hmotnosti, plynné, kapalné i pevné. Nejjednodušším zástupcem této skupiny je plynný tetrafluormethan (CF4). Kapalné skupenství mají například perfluoroktan a perfluordekalin. Fluorouhlíky s jednoduchými vazbami jsou stabilní, nenasycené vykazují vyšší reaktivitu, obzvláště pokud obsahují trojné vazby. Fluorourovodíky jsou chemicky i tepelně stálejší než uhlovodíky, protože vazby C-F jsou málo reaktivní; také se vyznačují výraznou lipofobicitou. Omezené Van der Waalsovy síly dodávají některým fluorouhlíkům využití v mazivech a někdy i vysokou těkavost. Kapalné fluorouhlíky mají využití v lékařství jako přenašeče kyslíku.
Struktury organofluoridů se mohou lišit. Perfluorované sloučeniny mají snahu se vyskytovat odděleně od uhlovodíků, tato vlastnost se využívá například u kyseliny perfluoroktanové při zpracování fluoropolymerů. Aromatické perfluorované uhlovodíky na rozdíl od alifatických obvykle s nefluorovanými sloučeninami vytvářejí směsi, ve kterých se objevují donor-akceptorové interakce pí-systémů.

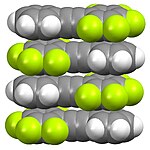
Fluoropolymery
Existuje řada fluorovaných polymerů, od plně fluorovaných, jako je polytetrafluorethylen (PTFE) po částečně fluorované, například polyvinylidenfluorid ([CH2CF2]n) a polychlortrifluorethylen ([CFClCF2]n). Evropská unie částečně fluorované uhlovodíky (HFC) označuje jako F-plyny a připravila zákaz budoucího používání těchto plynů.[4]
Fluorované uhlovodíky
Fluorované uhlovodíky, organické sloučeniny obsahující atomy fluoru a vodíku, jsou nejrozšířenější skupinou organofluoridů. Používají se nappříklad v klimatizačních přístrojích a jako chladiva,[5] kde nahrazují dříve používané chlorfluorované uhlovodíky, jako je dichlordifluormethan, a hydrochlorfluorované uhlovodíky, jako dichlorfluormethan. Mají menší vliv na poškozování ozonové vrstvy, ovšem působí jako skleníkové plyny.
Fluorouhlovodíky s nízkým počtem vazeb C-F se chovají podobně jako uhlovodíky, od kterých jsou odvozeny, ovšem mají odlišnou reaktivitu; například jak uracil, tak i fluorouracil jsou bezbarvé pevné látky s vysokými teplotami tání, ovšem druhá z těchto látek je účinným protinádorovým léčivem. Vazby C-F se do léčiv zavádějí právě za účelem pozměnění reaktivity.[6] Řada léčiv a agrochemikálií obsahuje pouze jeden fluorový nebo trifluormethylový substituent.
Fluorokarbeny
Jako příklad, jak fluorové substituenty mění reaktivitu sloučenin, lze uvést také difluorkarben, CF2, který se vyskytuje v singletovém základním stavu, zatímco u methylenu (CH2) je základní stav tripletový.[7] Tento rozdíl má význam v tom, že se difluorkarben používá jako prekurzor tetrafluoroethylenu.
Perfluorované sloučeniny
Perfluorované sloučeniny jsou strukturně podobné fluorouhlíkům, obsahují však i jiné atomy, například dusík či jod, nebo iontové skupiny, které mají například perfluorované karboxylové kyseliny.
Způsoby vytváření vazeb C–F
Organofluoridy lze připravit mnoha různými způsoby, které závisí na potřebné míře a regiochemii fluorace a vlastnostech prekurzorů. Přímou fluorací uhlovodíků F2, obvykle zředěným N2, vznikají vysoce fluorované sloučeniny:
- R3CH + F2 → R3CHF + HF
Mnohé tyto reakce jsou ovšem neselektivní a musí se provádět opatrně, protože může dojít k nekontrolovatelnému „hoření“ uhlovodíků v F2, obdobnému jako je hoření v kyslíku (O2). Byly tak vyvinuty jiné postupy; ty se dělí na dvě skupiny.
Elektrofilní fluorace
Při elektrofilních fluoracích se používají zdroje fluoridových iontů (F+). Tyto zdroje, jako například F-TEDA-BF4 často obsahují vazby N-F. Asymetrické fluorace, kdy vzniká pouze jeden ze dvou možných enantiomerů, vyžadují elektrofilní fluorační činidla.[8]
Jako příklad lze uvést přípravu prekurzorů protizánětlivých léčiv:[9]
Elektrosyntetické metody
Významným druhem elektrofilní fluorace je elektrosyntéza. Tímto způsobem většinou dochází k perfluoraci, tedy nahrazení všech vazeb C–H vazbami C–F. Uhlovodík bývá rozpuštěn nebo rozptýlen v roztoku HF a směs je elektrolyzována při napětí 5 až 6 V za použití niklových anod.[10] Tímto způsobem byl poprvé připraven perfluorpyridin (C5F5N) z pyridinu (C5H5N). Bylo popsáno několik obměn tohoto postupu, například použití hydrogendifluoridu draselného nebo organických rozpouštědel.
Nukleofilní fluorace
Fluoraci lze provést nejen elektrofilně, ale také nukleofilně , s využitím zdrojů fluoridových (F−) iontů, které zpravidla nahrazují ionty chloridové nebo bromidové. Nejjednodušší jsou podvojné záměny s použitím fluoridů alkalických kovů.[11] U alifatických sloučenin se tento postup někdy nazývá Finkelsteinova reakce, zatímco u aromatických jde o Halexův proces.
- R3CCl + MF → R3CF + MCl (M = Na, K, Cs)
Alkylfluoridy je možné připravit reakcemi alkoholů s Olahovými činidly (například fluoridem pyridinia) nebo jinými fluoridačními činidly.
Rozklady aryldiazoniumtetrafluorboritanů při Sandmeyerových[12] nebo Balzových–Schiemannových reakcích využívají jako zdroje F− tetrafluorboritany.
- ArN2BF4 → ArF + N2 + BF3
I když vypadá fluorovodík jako nepravděpodobný nukleofil, tak je při přípravách organofluoridů nejčastějším nukleofilem. Tyto reakce často katalyzují fluoridy kovů, jako je fluorid chromitý. 1,1,1,2-tetrafluorethan, látka nahrazující chlorfluorované uhlovodíky, se vyrábí takto:[13]
- Cl2C=CClH + 4 HF → F3CCFH2 + 3 HCl
Tato metoda zahrnuje dva druhy reakcí, podvojnou záměnu F− za Cl− a hydrofluoraci alkenu.
Deoxofluorace
Při deoxofluoracích jsou hydroxylové a karbonylové skupiny nahrazovány fluoridovými. K výměně kyslíku u karbonylů se používá fluorid siřičitý:
- RCO2H + SF4 → RCF3 + SO2 + HF
Místo SF4 se může použít DAST, NEt2SF3 nebo bis(2-methoxyethyl)aminofluorid síry. Tyto reaktanty se snadněji skladují a jsou selektivnější:[14]
Reakce bis(2-methoxyethyl)aminofluoridu síry
Z fluorovaných sloučenin
Řada organofluorových sloučenin se vyrábí z reaktantů obsahujících perfluoralkylové a perfluorarylové skupiny; například jako zdroj trifluormethylových skupin může sloužit (trifluormethyl)trimethylsilan, CF3Si(CH3)3.[15] K jiným používaným zdrojům patří CF3X (X = Br, I), C6F5Br a C3F7I. Tyto sloučeniny vytváří Grignardova činidla, která následně mohou reagovat that s mnoha různými elektrofily. Rozvoj fluoračních metod je z velké části řízen vývojem sloučenin sloýužících k zavádění fluorovaných řetězců.
Dalším významným využitím fluorovaných reaktantů je průmyslová výroba tetrafluoroethylenu (přes difluorkarbenový meziprodukt). Tento proces začíná tepelnou (při 600-800 °C) dehydrochlorací chlordifluormethanu:[6]
- CHClF2 → CF2 + HCl
- 2 CF2 → C2F4
K tvorbě chlorfluorkarbenu, meziproduktu cyklopropanačních reakcí, se používá fluordichloroctan sodný (CAS 2837-90-3).
Způsoby navazování 18F
Radiofarmaka obsahující fluor mají využití v 18F-pozitronové emisní tomografii a jejich potřeba podnítila vývoj nových způsobu tvorby vazeb C–F. Vzhledem ke krátkému poločasu přeměny 18F musí tyto syntézy být vysoce účinné, rychlé a snadno proveditelné.[16]
Jako příklad lze uvést přípravu (18F)-fludeoxyglukózy náhradou triflátové skupiny nukleofilním 18F−:
Biologický význam
Biologicky vznikající organofluoridy byly nalezeny u mikroorganismů a rostlin, ovšem nikoliv u živočichů.[17] Nejčastější takovou sloučeninou je kyselina fluoroctová, která slouží jako ochrana proti býložravcům u nejméně 40 rostlinám rostoucím v Austrálii, Brazílii a Africe.[18]
K dalším biologicky tvořeným organofluoridům patří ω-fluorované mastné kyseliny, fluoraceton a kyselina 2-fluorcitronová, jež se pravděpodobně tvoří z fluoracetaldehydu.[17] Biologické tvorby vazeb uhlík-fluor je například schopen enzym adenosylfluoridsyntáza.[19]
Uměle vytvořené vazby C-F jsou časté v léčivech a agrochemikáliích, protože zde stabilizují uhlíkaté řetězce; malý kovalentní poloměr atomu fluoru navíc umožňuje jeho funkci jako bioisosteru vodíku. Zavádění vazeb uhlík-fluor do molekul léčiv je jedním z hlavních úkolů farmaceutické chemie, protože jejich přítomnost zvyšuje pravděpodobnost nalezení účinného léčiva přibližně desetkrát.[20]
Kolem 20 % léčiv a 30 až 40 % agrochemikálií patří mezi organofluoridy.[20]
Použití
Vazby C-F lze nalézt například v léčivech, agrochemikáliích, polymerech, chladivech, tenzidech, anestetikách a katalyzátorech.
Léčiva a agrochemikálie
Vazby uhlík-fluor se často vyskytují v léčivech a agrochemikáliích, protože jsou metabolicky stabilní a fluor funguje jako bioisoster vodíku. Jako příklady léčiv obsahujících fluor lze uvést 5-fluoruracil, flunitrazepam, fluoxetin, paroxetin, ciprofloxacin, meflokin a flukonazol. Fluorované ethery, například methoxyfluran, enfluran, isofluran, sevofluran a desfluran se používají jako anestetika. Fluorovaná anestetika jsou méně hořlavá než diethylether a cyklopropan. Perfluorované alkany slouží jako náhražky krve.
Hnací plyny v inhalátorech
Fluorouhlíky také slouží jako hnací plyny v inhalátorech používaných pacienty s astmatem. Tyto hnací plyny obvykle obsahují hydrofluoroalkany (HFA), jež nahradily chlorfluorované uhlovodíky (CFC). Inhalátory obsahující CFC byly v roce 2008 zakázány Montrealským protokolem,[21] protože přispívají k poškozování ozonové vrstvy.
Fluorované tenzidy
Fluorované sloučeniny, obsahující polyfluorované hydrofobní řetězce a hydrofilní části, slouží jako tenzidy, protože se v důsledku své lipofilicity hromadí na rozhraní kapaliny a vzduchu. Mají nízké povrchové energie a výrazně snižují povrchové napětí. Nejvíce jsou prozkoumány kyselina perfluoroktansulfonová (PFOS) a kyselina perfluoroktanová, jsou známy svou toxicitou a dlouhým setrváváním v lidských tělech a životním prostředí.
Rozpouštědla
Fluorované sloučeniny mohou být použity jako rozpouštědla. Dichlordifluormethan a chlordifluormethan se často používaly jako chladiva. Vzhledem k tomu, že CFC požkozují ozonovou vrstvu tvorbou radikálů homolytickým štěpením vazeb uhlík-chlor, tak bylo jejich používání výrazně omezeno. Hydrofluorované uhlovodíky (HFC), jako je tetrafluorethan, je mohou nahradit, protože ozonovou vrstvu nepoškozují.
Dobrá rozpustnost kyslíku v perfluorovaných sloučeninách vyplývající z jejich lipofilicity, se využívá například u perfluordekalinu k nahrazování krve a přenosu kyslíku do plic.
1,1,1,2-tetrafluorethan se používá k extrakci látek, jako jsou taxol, pupalkový olej a vanilin. 2,2,2-trifluorethanol je polární rozpouštědlo odolné vůči oxidaci.[22]
Organofluorové reaktanty
Rozvoj organofluorové chemie přinesl řadu reaktantů využitelných i v jiných oblastech. Kyselina trifluormethansulfonová (CF3SO3H) a kyselina trifluoroctová (CF3CO2H) mají v organické syntéze. Jejich značná kyselost je způsobena elektronegativitou atomů fluoru v trifluormethylových skupinách, která stabilizuje záporný náboj. Triflátový anion, konjugovaná zásada kyseliny trifluormethansulfonové, je dobrou odstupující skupinou v substitučních reakcích.
Fluorové fáze
Vysoce fluorované substituenty, jako je perfluorhexyl (C6F13), pozměňují vlastnosti molekul jako rozpouštědel, což usnadňuje přečišťování produktů v organické syntéze.[23][24] Sloučeniny bohaté na fluor se přednostně rozpouštějí v rozpouštědlech, které také obsahují více fluorových atomů. Vzhledem k nízké reaktivitě vazeb C-F lze tyto fluorová rozpouštědla použít i u jinak obtížně rozpustitelných látek. Příkladem může být použití fluoroalkylovaných hydridů cínů při redukcích, kde se produkty snadno oddělují od zbytků reaktantů extrakcí fluorovanými rozpouštědly.[25]
Hydrofobní fluorované iontové kapaliny, jako například organické soli bistriflimidového a hexafluorfosforečnanového aniontu, mohou tvořit fáze, které nejsou rozpustné ani ve vodě, ani v organických rozpouštědlech, za vzniku vícefázových kapalin.
Organofluoridové ligandy a přechodné kovy
Organofluoridové ligandy mají své využití také v organokovové a koordinační chemii. Jednou z vlastností ligandů obsahujících fluor je možnost použití 19 ke zkoumání reakcí. Organofluoridy mohou sloužit jako „sigma-donorové ligandy“, jak je níže znázorněno na titanitém komplexu [(C5Me5)2Ti(FC6H5)]BPh4. Nejčastěji se ovšem fluorouhlíkové substituenty používají ke zvýšení Lewisovské kyselosti kovových center; jako příklad lze použít Eufod, komplex trojmocného europia, který obsahuje perfluorheptylovaný acetylacetonátový ligand. Tato sloučenina a jí podobné mají využití v organické syntéze a NMR spektroskopii.

V oblastech, kde se překrývají organokovová chemie a materiálové vědy, mohou fluorované organické ligandy sloužit k upravování vlastností molekul. Míra a regiochemie fluorace metalovaných 2-fenylpyridinových ligandů v platnatých komplexech mají velký vliv na emisní vlastnosti komplexů.[26]
Trifenylfosfin lze upravit navázáním perfluoralkylových substituentů, které mu dodávají rozpustnost v perfluorhexanu a superkritickém oxidu uhličitém. Příkladem takového komplexu může být [(C8F17C3H6-4-C6H4)3P.[27]
Aktivace vazeb C-F
V organokovové chemii se využívá štěpení vazeb C-F reaktanty založenými na přechodných kovech. K tomuto účelu byly vyvinuty stechiometrické i katalytické reakce; jde také o předmět zájmu v organické syntéze a odstraňování cizorodých látek z životního prostředí.[28] Aktivace vazeb C-F se dělí na tyto skupiny: (i) oxidační adice fluorouhlíků, (ii) tvorba vazeb M–C eliminací HF, (iii) tvorba vazeb M–C eliminací fluorosilanů, (iv) hydrodefluorace fluorouhlíků tvorbou vazeb M–F, (v) nukleofilní ataky fluorovodíků, a (vi) defluorace fluorouhlíků. Jako příklad aktivace vazby C-F řízené kovem může být uvedena defluorace fluorhexanu hydridem zirkonatým:
- (C5Me5)2ZrH2 + 1-FC6H13 → (C5Me5)2ZrH(F) + C6H14
Fluorouhlíkové kationty v Zieglerových–Nattových katalyzátorech
Atomy fluoru jsou častými součástmi nekoordinujících a slabě koordinujících aniontů. Tetrakis(pentafluorofenyl)boritanové, B(C6F5)4−, a tetrakis[3,5-bis(trifluoromethyl)fenyl]boritanové ionty se používají v Zieglerových–Nattových katalyzátorech polymerizace alkenů. Fluorované substituenty dodávají aniontům mírnou zásaditost a zlepšují jejich rozpustnost v mírně zásaditých rozpouštědlech, použitelných se silnými Lewisovými kyselinami.
Materiálové vědy
Organofluoridy mají rovněž řadu využití v materiálových vědách. Vzhledem k nízkým koeficientům tření slouží kapalné fluoropolymery jako maziva. Fluorouhlíky jsou obsaženy v některých mazivech do střelných zbraní. Díky své nehořlavosti jsou také složkami hasicích hmot. Organofluoridy se také nacházejí v displejích z tekutých krystalů. Polymer kyseliny trifluormethansulfonové se používá jako pevná kyselina, v membránách nízkoteplotních palivových článků. Monomer 4,4'-difluorbenzofenon slouží na výrobu polyetherketonů.
Biosyntéza organofluoridů
I přes velký počet přírodních sloučenin obsahujících těžší halogenidy, chloridy, bromidy a jodidy, je známo jen málo biologicky vznikajících sloučenin obsahujících vazby uhlík-fluor.[29] Nejrozšířenější je kyselina fluoroctová, vyskytující se jako toxin v několika druzích rostlin. Dále sem patří kyselina fluorolejová, fluoraceton, nukleocidin (4'-fluor-5'-O-sulfamoyladenosin), fluorthreonin a kyselina fluorcitronová. Mnohé z těchto sloučenin pravděpodobně vzniká z fluoracetaldehydu. Enzym fluorináza katalyzuje syntézu 5'-deoxy-5'-fluoradenosinu.
Historie
Výzkum organofluoridů započal v 19. století společně s rozvojem organické chemie.[13][30]
U příprav prvních organofluoridů byl jako zdroj fluoridových iontů použit fluorid antimonitý. Nehořlavost a netoxičnost chlorfluorovaných uhlovodíků CCl3F a CCl2F2 vedla ve 20. letech 20. století k jejich průmyslovému využívání. V roce 1938 Roy J. Plunkett objevil polytetrafluorethylen (PTFE).[31][32][33]
Další rozvoj vycházel z poznatků získaných při výrobě fluoridu uranového.[6]
Od konce 40. let 20. století bylo vyvinuto několik postupů přípravy organofluoridů založených na elektrofilních fluoracích, u prvních se používal fluorid kobaltitý (CoF3). Joseph H. Simons objevil elektrofluoraci, kterou se daly získat velmi stabilní perfluorované profukty.[10] Tyto nové postupy umožnily tvorbu vazeb C-F bez používání elementárního fluoru a využívání podvojných záměn.
V roce 1957 byly popsány protinádorové účinky 5-fluoruracilu. Tento objev ukázal na jedno z prvních využití racionálního upravování léčiv.[34]
Tento objev vedl k růstu zájmu o fluorovaná léčiva a agrochemikálie. Příprava prvních sloučenin vzácných plynů, například fluoridu xenoničitého (XeF4) poskytlo v 60. letech další skupinu použitelných reaktantů. V 70. letech 20. století bylo do pozitronové emisní tomografie zavedeno používání fluorodeoxyglukózy. Za objev škodlivého vlivu chlorfluorovaných uhlovodíků na ozonovou vrstvu byla udělena Nobelova cena. Tento objev vedl k rozvoji organofluoridových náhražek, které ozonovou vrstvu nepoškozují. V roce 2002 byla popsána fluorináza jako první známý enzym vytvářející vazby C-F.[35]
Bezpečnost
Pouze několik organofluoridů, jako například kyselina fluoroctová a perfluorisobuten, je bioaktivních a výrazněji toxických.
Některé organofluoridy jsou nebezpečné pro zdraví a životní prostředí. Fluorchlorované (CFC) a hydrofluorchlorované uhlovodíky (HCFC) poškozují ozonovou vrstvu a jsou silnými skleníkovými plyny.
V roce 2013 podpořily země G20 snahy o ukončení používání HCFCs. Potvrdily význam Montrealského protokolu.[36]
Odbouratelnost a bioakumulace
Vzhledem k síle vazeb uhlík-fluor se řada umělých fluorovaných organických sloučenin v přírodě nerozkládá. Fluorované tenzidy, jako jsou kyselina perfluoroktansulfonová a kyselina perfluoroktanová, jsou znečišťujícími látkami s celosvětovým rozšířením. CFC a tetrafluormethan byly nalezeny i v horninách.[17]
Odkazy
Související články
Reference
V tomto článku byl použit překlad textu z článku Organofluorine chemistry na anglické Wikipedii.
- ↑ a b c d e f g Kirsch, Peer Modern fluoroorganic chemistry: synthesis, reactivity, applications. Wiley-VCH, 2004.
- ↑ J. Lapasset; J. Moret; M. Melas; A. Collet; M. Viguier; H. Blancou. Crystal structure of 12,12,13,13,14,14,15,15,16,16,17,17,17-tridecafluoroheptadecan-1-ol, C17H23F13O. Zeitschrift für Kristallographie – Crystalline Material. 1996, s. 945–946. doi:10.1524/zkri.1996.211.12.945. Bibcode 1996ZK....211..945L.
- ↑ C. E. Smith, P. S. Smith, R. Ll. Thomas, E. G. Robins, J. C. Collings, Chaoyang Dai, A. J. Scott, S. Borwick, A. S. Batsanov, S. W. Watt, S. J. Clark, C. Viney, J. A. K. Howard, W. Clegg, T. B. Marder. Arene-perfluoroarene interactions in crystal engineering: structural preferences in polyfluorinated tolans. Journal of Materials Chemistry. 2004, s. 413. doi:10.1039/b314094f.
- ↑ NAŘÍZENÍ EVROPSKÉHO PARLAMENTU A RADY o fluorovaných skleníkových plynech[nedostupný zdroj], o změně směrnice (EU) 2019/1937 a o zrušení nařízení (EU) č. 517/2014 (návrh, pdf)
- ↑ Oliver Milman. 100 countries push to phase out potentially disastrous greenhouse gas. The Guardian [online]. 2016-09-22 [cit. 2016-09-22]. Dostupné online.
- ↑ a b c G. Siegemund, W. Schwertfeger, A. Feiring, B. Smart, F. Behr, H. Vogel, B. McKusick "Fluorine Compounds, Organic" in "Ullmann's Encyclopedia of Industrial Chemistry" 2005, Wiley-VCH, Weinheim doi:10.1002/14356007.a11_349
- ↑ Dana Lyn S. Brahms; William P. Dailey. Fluorinated Carbenes. Chemical Reviews. 1996, s. 1585–1632. doi:10.1021/cr941141k. PMID 11848805.
- ↑ Vincent A. Brunet; David O'Hagan. Catalytic Asymmetric Fluorination Comes of Age. Angewandte Chemie International Edition. 2008, s. 1179–1182. doi:10.1002/anie.200704700. PMID 18161722.
- ↑ Stéphane Caron; Robert W. Dugger; Sally Gut Ruggeri; John A. Ragan; David H. Brown Ripin. Large-Scale Oxidations in the Pharmaceutical Industry. Chemical Reviews. 2006, s. 2943–2989. doi:10.1021/cr040679f. PMID 16836305.
- ↑ a b J. H. Simons. The Electrochemical Process for the Production of Fluorocarbons. Journal of the Electrochemical Society. 1949, s. 47–66. doi:10.1149/1.2776733.
- ↑ VOGEL, A. I.; LEICESTER, J.; MACEY, W. A. T. n-Hexyl Fluoride. Org. Synth.. Dostupné online.; Coll. Vol.. S. 525.
- ↑ FLOOD, D. T. Fluorobenzene. Org. Synth.. Dostupné online.; Coll. Vol.. S. 295.
- ↑ a b William R. Dolbier. Fluorine Chemistry at the Millennium. Journal of Fluorine Chemistry. 2005, s. 157–163. doi:10.1016/j.jfluchem.2004.09.033.
- ↑ Gauri S. Lal; Guido P. Pez; Reno J. Pesaresi; Frank M. Prozonic. Bis(2-methoxyethyl)aminosulfur trifluoride: a new broad-spectrum deoxofluorinating agent with enhanced thermal stability. Chemical Communications. 1999, s. 215–216. doi:10.1039/a808517j.
- ↑ PICHIKA RAMAIAH, RAMESH KRISHNAMURTI, AND G. K. SURYA PRAKASH. 1-trifluoromethyl)-1-cyclohexanol. Org. Synth.. 1998, s. 232. Dostupné online.
- ↑ D. Le Bars. Fluorine-18 and Medical Imaging: Radiopharmaceuticals for Positron Emission Tomography. Journal of Fluorine Chemistry. 2006, s. 1488–1493. doi:10.1016/j.jfluchem.2006.09.015.
- ↑ a b c Murphy C.D., Schaffrath C., O'Hagan D.: "Fluorinated natural products: the biosynthesis of fluoroacetate and 4-fluorothreonine in Streptomyces cattleya" Chemosphere. 2003 Jul;52(2):455-61.
- ↑ Alex T. Proudfoot; Sally M. Bradberry; J. Allister Vale. Sodium Fluoroacetate Poisoning. Toxicological Reviews. 2006, s. 213–219. doi:10.2165/00139709-200625040-00002. PMID 17288493.
- ↑ David O'Hagan; Christoph Schaffrath; Steven L. Cobb; John T. G. Hamilton; Cormac D. Murphy. Biochemistry: Biosynthesis of an organofluorine molecule. Nature. 2002, s. 279. doi:10.1038/416279a. PMID 11907567. Bibcode 2002Natur.416..279O.
- ↑ a b Ann M. Thayer. Fabulous Fluorine. Chemical & Engineering News. 2006-06-05, s. 15–24. Dostupné online [cit. 2009-01-17]. doi:10.1021/cen-v084n023.p015.
- ↑ Phase-Out of CFC Metered-Dose Inhalers [online]. [cit. 2017-09-10]. Dostupné online.
- ↑ KABAYADI S. RAVIKUMAR, VENKITASAMY KESAVAN, BENOIT CROUSSE, DANIÈLE BONNET-DELPON, AND JEAN-PIERRE BÉGUÉ. Mild and Selective Oxidation of Sulfur Compounds in Trifluorethanol: Diphenyl Disulfide and Methyle Phenyl Sulfoxide. Org. Synth.. 2003, s. 184. Dostupné online.
- ↑ E. G. Hopea, A. P. Abbotta, D. L. Daviesa, G. A. Solana and A. M. Stuarta "Green Organometallic Chemistry" in Comprehensive Organometallic Chemistry III, 2007, Volume 12, Pages 837-864. doi:10.1016/B0-08-045047-4/00182-5
- ↑ J. A. Gladysz, D. P. Curran, I. T. Horváth (Eds.) "Handbook of Fluorous Chemistry", Wiley–VCH, Weinheim, 2004. ISBN 978-3-527-30617-6.
- ↑ AIMEE CROMBIE, SUN-YOUNG KIM, SABINE HADIDA, AND DENNIS P. CURRAN. Synthesis of Tris(2-Perfluorohexylethyl)tin Hydride: A Highly Fluorinated Tin Hydride with Advantageous Features of Easy Purification. Org. Synth.. Dostupné online.; Coll. Vol.. S. 712.
- ↑ M.E. Thompson, P.E. Djurovich, S. Barlow and S. Marder "Organometallic Complexes for Optoelectronic Applications" Comprehensive Organometallic Chemistry III, 2007, Volume 12, Pages 101-194. doi:10.1016/B0-08-045047-4/00169-2
- ↑ J.C. Peters, J.C. Thomas "Ligands, Reagents, and Methods in Organometallic Synthesis" in Comprehensive Organometallic Chemistry III, 2007, Volume 1, Pages 59-92. doi:10.1016/B0-08-045047-4/00002-9
- ↑ R.N. Perutz and T. Braun "Transition Metal-mediated C–F Bond Activation" Comprehensive Organometallic Chemistry III, 2007, Volume 1, Pages 725-758. doi:10.1016/B0-08-045047-4/00028-5.
- ↑ D. O'Hagan; David B. Harper. Fluorine-Containing Natural Products. Journal of Fluorine Chemistry. 1999, s. 127–133. doi:10.1016/S0022-1139(99)00201-8.
- ↑ Takashi Okazoe; David B. Harper. Overview on the history of organofluorine chemistry from the viewpoint of material industry. Proceedings of the Japan Academy, Series B. 2009, s. 276–289. ISSN 0386-2208. doi:10.2183/pjab.85.276. PMID 19838009. Bibcode 2009PJAB...85..276O.
- ↑ Dr. Roy J. Plunkett: Discoverer of Fluoropolymers. The Fluoropolymers Division Newsletter. 1994, s. 1–2. Dostupné v archivu pořízeném z originálu dne 2003-07-09. doi:10.2183/pjab.85.276. PMID 19838009. Bibcode 2009PJAB...85..276O.
- ↑ Roy J. Plunkett [online]. 2016 [cit. 2018-02-21]. Dostupné online.
- ↑ Center for Oral History. Roy J. Plunkett [online]. [cit. 2018-02-21]. Dostupné online.
- ↑ C. Heidelberger, N. K. Chaudhuri, P. Danneberg, D. Mooren, L. Griesbach, R. Duschinsky, R. J. Schnitzer, E. Pleven, J. Schreiner. Fluorinated Pyrimidines, A New Class of Tumour-Inhibitory Compounds. Nature. 1957, s. 663–666. doi:10.1038/179663a0. PMID 13418758. Bibcode 1957Natur.179..663H.
- ↑ D. O'Hagan; C. Schaffrath; S. L. Cobb; J. T. Hamilton; C. D. Murphy. Biochemistry: biosynthesis of an organofluorine molecule. Nature. 2002, s. 279. doi:10.1038/416279a. PMID 11907567. Bibcode 2002Natur.416..279.
- ↑ U.S. White House Press Secretary. United States, China, and Leaders of G-20 Countries Announce Historic Progress Toward a Global Phase Down of HFCs. obamawhitehouse.archives.gov [online]. 2013-09-06 [cit. 2013-09-16]. Dostupné online.
Média použitá na této stránce
chemical reaction leading to a radiopharmaceutical
reaction catalysed by fluorinase (enzyme)
Illustration of the packing of molecules in the crystal structure of a molecule containing aliphatic fluorocarbon and aliphatic hydrocarbon segments. The picture was created by user TBChem and uploaded on 8/15/2007. The picture was created using Mercury from Cambridge Structural Database entry TULQOG. The literature reference for the compound is J. Lapasset, J. Moret, M. Melas, A. Collet, M. Viguier, H. Blancou, Z. Kristallogr. 1996, 211, 945. Atoms are colored according to element type: carbon (grey), fluorine (green), oxygen (red), hydrogen (white).
chemical reaction effected by the reagent called Selectfluor
Some important organofluorine compounds.
A: Fluoromethane
B: Isoflurane
C: a CFC
D: an HFC
E: Triflic acid
F: Teflon
G: PFOS
H: Fluorouracil
I: Prozac
Illustration of the packing of molecules in the crystal structure of a molecule containing aromatic fluorocarbon and aromatic hydrocarbon moieties. The picture was created by user TBChem and uploaded on 8/15/2007. The picture was created using Mercury from Cambridge Structural Database entry ASIJIV. The literature reference for the compound is C.E. Smith, P.S. Smith, R.Ll. Thomas, E.G. Robins, J.C. Collings, Chaoyang Dai, A.J. Scott, S. Borwick, A.S. Batsanov, S.W. Watt, S.J. Clark, C. Viney, J.A.K. Howard, W. Clegg, T.B. Marder, J. Mater. Chem. 2004, 14, 413. Atoms are colored according to element type: carbon (grey), fluorine (green), hydrogen (white).
structure of Cp*Ti+ adduct of FPh











