Oxalylchlorid
| Oxalylchlorid | |
|---|---|
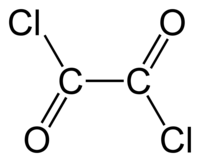 Strukturní vzorec | |
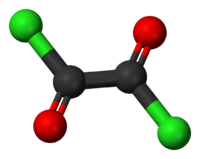 Kuličkový model molekuly | |
 Kalotový model molekuly | |
| Obecné | |
| Systematický název | Oxalyldichlorid |
| Ostatní názvy | Oxaloylchlorid, (di)chlorid kyseliny šťavelové |
| Sumární vzorec | C2O2Cl2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 79-37-8 |
| SMILES | ClC(=O)C(=O)Cl |
| Vlastnosti | |
| Molární hmotnost | 126,93 g/mol |
| Teplota tání | −16 °C (257 K) |
| Teplota varu | 63 až 64 °C (337 K) |
| Hustota | 1,4785 g/cm3 |
| Index lomu | 1,429 |
| Rozpustnost ve vodě | reaguje |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H314 H331 |
| P-věty | P261 P280 P305 P310 P338 P351 |
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | |
| Některá data mohou pocházet z datové položky. | |
Oxalylchlorid (též oxaloylchlorid, systematický název oxalyldichlorid), je organická sloučenina, diacylchlorid kyseliny šťavelové. Používá se jako reaktant v organické syntéze[2]; lze jej připravit reakcí kyseliny šťavelové s chloridem fosforečným.
Oxalylchlorid poprvé připravil roku 1892 francouzský chemik Adrien Fauconnier reakcí diethyloxalátu s chloridem fosforečným.[3]
Reakce
Oxalylchlorid reaguje s vodou, přičemž vznikají pouze plynné produkty: chlorovodík (HCl), oxid uhličitý (CO2) a oxid uhelnatý (CO)
- (COCl)2 + H2O → 2 HCl + CO2 + CO
Touto vlastností se liší od ostatních acylchloridů, které se hydrolyzují na chlorovodík a původní karboxylové kyseliny.
Použití v organické syntéze
Oxidace alkoholů
Roztokem obsahujícím oxalylchlorid a dimethylsulfoxid (DMSO) se přeměňují alkoholy na odpovídající aldehydy a ketony procesem známým jako Swernova oxidace.
Syntéza acylchloridů
Oxalylchlorid se nejčastěji používá společně s N,N-dimethylformamidem (DMF) jako katalyzátorem v organické syntéze k přípravě acylchloridů. Podobně jako thionylchlorid se při této reakci mění na těkavé vedlejší produkty; jeden z menšinových vedlejších produktů je možný karcinogen.[4] Oproti thionylchloridu je mírnějším a selektivnějším reaktantem; je rovněž dražší a tak se většinou používá v menším měřítku.
Tato reakce zahrnuje přeměnu DMF na imidoylchloridový derivát (Me2N=CHCl+), podobně jako v prvním kroku Vilsmeierovy–Haackovy reakce. Imidoylchlorid je účinné chlorační činidlo.
Formylace arenů
Oxalylchlorid reaguje za přítomnosti chloridu hlinitého s aromatickými sloučeninami za vzniku odpovídajících acylchloridů v procesu známem jako Friedelova-Craftsova acylace. Vzniklý acylchlorid může být hydrolyzován na příslušnou karboxylovou kyselinu.
Příprava oxalátových diesterů
Podobně jako ostatní acylchloridy, i oxalylchlorid reaguje s alkoholy za vzniku esterů:
- 2 RCH2OH + (COCl)2 → RCH2OC(O)C(O)OCH2R + 2 HCl
Tyto reakce obvykle probíhají za přítomnosti zásady jako například pyridinu.
Ostatní
Oxalylchlorid byl údajně použit při první syntéze dioxantetraketonu (C4O6).
Odkazy
Související články
- Oxalyl
- Kyselina šťavelová
Externí odkazy
 Obrázky, zvuky či videa k tématu Oxalylchlorid na Wikimedia Commons
Obrázky, zvuky či videa k tématu Oxalylchlorid na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Oxalyl chloride na anglické Wikipedii.
- ↑ a b Oxalyl chloride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Salmon, R. Encyclopedia of Reagents for Organic Synthesis. Oxalyl Chloride. New York: John Wiley & Sons, 2001. DOI 10.1002/047084289X.ro015. (anglicky)
- ↑ FAUCONNIER, Adrien. Action du perchlorure de phosphore sur l'oxalate d'éthyle. Comptes Rendus Hebdomadaires des Séances de l'Académie des Sciences de Paris. 1892, s. 122–123. Dostupné online. (French)
- ↑ CLAYDEN, Jonathan. Organic chemistry. Reprinted (with corrections). vyd. Oxford [u.a.]: Oxford Univ. Press, 2005. Dostupné online. ISBN 978-0-19-850346-0. S. 296. (anglicky)
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for flammable substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for corrosive substances
Conversion of a carboxylic acid to acid chloride using oxalyl chloride and a DMF catalyst
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for toxic substances












