Polyaminy
Polyaminy jsou organické sloučeniny s více než dvěma aminovými skupinami. Mohou být přírodní i umělé. Alifatické polyaminy jsou bezbarvé, hygroskopické a rozpustné ve vodě. Aromatické polyaminy jsou při běžných teplotách krystalické pevné látky.
Přírodní polyaminy
Nízkomolekulární polyaminy se nacházejí ve všech typech organismů. K nejběžnějším patří triamin spermidin a tetraamin spermin; tyto látky jsou svou strukturou podobné diaminům putrescinu a kadaverinu. Metabolismus polyaminů je řízen enzymem ornitindekarboxylázou.[1] Polyaminy se nacházejí ve vysokých koncentracích v mozcích savců.[2]
Syntetické polyaminy
Některé polyaminy se používají v průmyslu a v laboratořích. Mají využití jako aditiva do motorových paliv a jako reaktanty při výrobě epoxidových pryskyřic.[3] K syntetickým polyaminům mimo jiné patří:
- Diethylentriamin, H2N-CH2CH2-NH-CH2CH2-NH2. Od něj odvozený pentamethyldiethylentriamin se používá jako chelatační činidlo v organokovové chemii.
- Triethylentetramin (H2N-CH2CH2-NH-CH2CH2-NH-CH2CH2-NH2), tetraethylenpentamin (H2N-CH2CH2-NH-CH2CH2-NH-CH2CH2-NH-CH2CH2-NH2), pentaethylenhexamin
- Makrocyklické polyaminy: 1,4,7-triazacyklononan a cyklen ((NHCH2CH2)4).
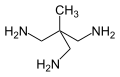
- Tris(2-aminoethyl)amin - rozvětvený polyamin; podobnou látkou je 1,1,1-tris(aminomethyl)ethan.
Polyethylenamin je polymer odvozený od aziridinu.
Biologické účinky
I když byl dobře popsán mechanismus regulace biosyntézy polyaminů, tak jsou jejich biologické funkce známy pouze z části. V amoniové kationtové formě se vážou na DNA. Rovněž spouštějí posun ribozomálního rámce během translace.[4]
Inhibice syntézy polyaminů způsobuje zpomalení nebo zastavení buněčného cyklu, který se může obnovit dodáním polyaminů z vnějšího zdroje. Většina eukaryotních buněk má na svých membránách polyaminový tranportní systém, který přenáší exogenní polyaminy dovnitř buňky. Tento systém je velmi aktivní u rychle se množících buněk a je cílem některých vyvíjených chemoterapeutik.[5]
Polyaminy, jako například NMDA receptory a AMPA receptory, slouží také jako modulátory iontových kanálů. Rovněž spouštějí odpověď kolicin E7 operonu a omezují funkci enzymů nutných k příjmu kolicinu E7, čímž přispívají k snadnějšímu přežití bakterií E. coli vytvářejících tuto látku.[6]
Polyaminy zvyšují propustnost hematoencefalické bariéry.[7]
Podílejí se také na řízení stárnutí rostlinných orgánů a proto bývají řazeny mezi rostlinné hormony.[8] Rovněž se účastní řízení programované buněčné smrti.[9]
Biosyntéza sperminu, spermidinu a theosperminu
Spermidin vzniká v organismech z putrescinu přes dekarboxylovaný S (SAM). Reakci katalyzuje enzym sperminsyntáza.
Spermin se tvoří ze spermidinu za přítomnosti sperminsyntázy.
Thermospermin (NH2-(CH2)3-NH-(CH2)3-NH-(CH2)4-NH2) je strukturní izomer sperminu, ze kterého vzniká působením theosperminsyntázy.[10]
Reference
V tomto článku byl použit překlad textu z článku Polyamine na anglické Wikipedii.
- ↑ A. E. Pegg; P. P. McCann. Polyamine metabolism and function. American Journal of Physiology. 1982, s. 212–221. PMID 6814260.
- ↑ N. Seiler. Handbook of Neurochemistry. New York: Plenum Publishing, 1992. Kapitola Polyamines, s. 223–255.
- ↑ Stephen A. Lawrence. Amines: synthesis, properties and applications. [s.l.]: Cambridge University Press, 2004. Dostupné online. ISBN 978-0-521-78284-5. S. 64.
- ↑ C. Rato; S. R. Amirova; D. G. Bates; I. Stansfield; H. M. Wallace. Translational recoding as a feedback controller: systems approaches reveal polyamine-specific effects on the antizyme ribosomal frameshift. Nucleic Acids Research. 2011, s. 4587–4597. Dostupné online. PMID 21303766.
- ↑ C. Wang; J. G. Delcros; L. Cannon; Fanta Konate; Horacio Carias; John Biggerstaff; Richard Andrew Gardner. Defining the molecular requirements for the selective delivery of polyamine conjugates into cells containing active polyamine transporters. Journal of Medicinal Chemistry. 2003, s. 5129–5138. PMID 14613316.
- ↑ Yi-Hsuan Pan; Chen-Chung Liao. The critical roles of polyamines regulating ColE7 production and restricting ColE7 uptake of the colicin-producing Escherichia coli. Journal of Biological Chemistry. 2006, s. 13083–13091. PMID 14613316.
- ↑ L. Zhang; H. K. Lee; T. H. Pruess; H. S. White; G. Bulaj. Synthesis and applications of polyamine amino acid residues: improving the bioactivity of an analgesic neuropeptide, neurotensin. Journal of Medicinal Chemistry. 2009, s. 1514–1517. PMID 19236044.
- ↑ S. Pandey; S. A. Ranade; P. K. Nagar; N. Kumar. Role of polyamines and ethylene as modulators of plant senescence. Journal of Biosciences. 2000, s. 291–299. PMID 11022232.
- ↑ P. N. Moschou; K. A. Roubelakis-Angelakis. Polyamines and programmed cell death. Journal of Experimental Botany. 2013-11-11, s. 1285–1296. PMID 24218329.
- ↑ A. Takano; J. Kakehi; T. Takahashi. Thermospermine is not a minor polyamine in the plant kingdom. Plant Cell Physiology. 2012, s. 606–616. [851716 Dostupné online]. PMID 22366038.
Externí odkazy
 Obrázky, zvuky či videa k tématu Polyaminy na Wikimedia Commons
Obrázky, zvuky či videa k tématu Polyaminy na Wikimedia Commons
Média použitá na této stránce
Skeletal formula of spermidine (N1-(3-aminopropyl)butane-1,4-diamine).
Structure of 1,1,1-Tris(aminomethyl)ethane, TAME; 2-(Aminomethyl)-2-methyl-1,3-propanediamine
The structure of Cyclen, 1,4,7,10-Tetraazacyclododecane
Skeletal formula of tris(2-aminoethyl)amine. Created using ACD/ChemSketch 10.0, Inkscape, and vim.
(c) Andrew Murkin, CC BY-SA 4.0
Biosyntéza spermidinu a sperminu z putrescinu. Ado = 5'-adenosyl.
Chemical diagram for 1,4,7-triazacyclononane
Chemical structure of spermine.