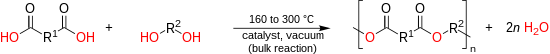Polyestery

Polyestery jsou polymery složené z monomerů obsahujících esterové funkční skupiny.[1] Nejrozšířenější látkou z této skupiny je polyethylentereftalát (PET). Některé polyestery se vyskytují v přírodě, například u rostlin a hmyzu; jiné, jako je polybutylenadipát-tereftalát, jsou umělé. Přírodní polyestery jsou, stejně jako několik umělých, biologicky rozložitelné, většina syntetických ale tuto vlastnost nemá.[1]
Druhy




Polyestery, převážně PET, jsou jednou z nejdůležitějších skupin polymerů; v roce 2000 se jich vyrobilo kolem 30 milionů tun.[2] Jejich struktury i vlastnosti se mohou výrazně lišit; ovlivňuje je druh použité R skupiny.[1]
Přírodní
K přírodním polyesterům patří kutin, jedna ze složek rostlinných kutikul, obsahující omega-hydroxykyseliny a jejich deriváty, propojené esterovými vazbami za tvorby polymerů neurčité velikosti. Polyestery jsou také vytvářeny včelami rodu Colletes, které vyměšují vlákna podobající se celofánu,[3][4]
Syntetické
K syntetickým polyesterům náleží:[1]
- Lineární alifatické vysokohmotnostní polyestery (Mn >10 000) mají nízké teploty tání (40 – 80 °C), jsou polokrystalické a nemají dobré mechanické vlastnosti. Jejich rozklad, způsobený náchylností k hydrolýze, je činí vhodnými v oblastech, kde aby mohlo dojít k poškození životního prostředí, například, u obalů a jednorázových předmětů,[5] nebo v biomedicíně a lécích.[6]
- Alifatické lineární nízkohmotnostní (Mn < 10 000) polyestery s hydroxylovými konci se používají jako makromonomery při výrobě polyuretanů.
- hyperrozvětvené polyestery se používají k upravování tekutosti termoplastů a v lacích[7] protože mívají nízkou viskozitu a dobrou rozpustnost a využitelnost[8]
- Alifaticko–aromatické polyestery, například polyethylentetreftalát (PET) a polybutylentereftalát (PBT), polyhexamethylentereftalát (PHT) a polypropylentereftalát (PTT, Sorona), jsou polokrystalické, s vysokými teplotami tání (160–280 °C).
- Plně aromatické lineární kopolyestery mají dobré mechanické a tepelné vlastnosti a využívají se v řadě náročných prostředí.
- Nenasycené polyestery se vyrábějí z vícesytných alkoholů a nenasycených kyselin a jejich struktury jsou tak překřížené; využití mají jako matrice kompozitních materiálů. Alkydové pryskyřice, vyráběné reakcemi vícesytných alkoholů a mastných kyselin, mají využití v nátěrech a kompozitech, jelikož je lze zesíťovat za přítomnosti kyslíku. Jsou známy také kaučukovité polyestery, označované jako termoplastické polyesterové elastomery.
Nenasycené polyestery patří mezi termosetové pryskyřice. V kapalné podobě slouží jako odlévací hmoty a jako potahové materiály na sklolaminátu. Nenasycené polyestery obohacené o sklolaminát mají využití v trupech sportovních lodí a u automobilů.
V závislosti na struktuře mohou být polyestery termoplasty nebo termosety. Také je lze použít jako umělé pryskyřice; nejčastěji ale jde o termoplasty.[9] Hydroxylové skupiny mohou být zreagovány s izokyanátovými za vzniku dvousložkových struktur použitelných jako nátěry, které je možné obarvit. Polyesterové termoplasty lze po zahřátí tvarovat. I když se za vysokých teplot dají spálit, tak většinou polyestery vykazují samozhášecí vlastnosti. Polyesterová vlákna mívají vysoké hodnoty modulu pružnosti v tahu, nízkou absorpci body a srážejí se méně než jiná průmyslově vyrobená vlákna.
Zvětšení aromatických částí řetězců polyesterů navyšuje jejich teploty skelného přechodu a tání, tepelnou a chemickou stabilitu a odolnost proti rozpouštědlům.
Polyestery mohou být také telechelické oligomery, jako jsou polykaprolaktondiol a polyethylenadipátdiol. Tyto látky se používají jako prepolymery.
Alifatické a aromatické polymery
Tepelně stálé polymery obvykle mají vysoké zastoupení aromatických molekul. Mohou být nepřetržitě používány i za teplot kolem 150 °C,[10] polyamidy a polykarbonáty si zachovávají vlastnosti do teplot okolo 100 °C,[11] a další, například polyethylen a polypropylen vykazují ještě nižší odolnost.
Poly(esterimidy) obsahují aromatické imidové skupiny v hlavních řetězcích, mají vysoká zastoupení aromatických struktur a jsou teplotně stálé. Vyznačují se vysokými teplotami tání, odolností vůči rozkladu oxidací, chemickou stabilitou a odolností ohledně záření. K významným skupinám teplotně stálých polymerů patří polyimidy, polysulfony, polyetherketony a polybenzimidazoly; nejvýznamnějšími z nich jsou polyimidy.[12] Struktury těchto polymerů způsobují jejich obtížnou zpracovatelnost v důsledku vysokých teplot tání a nízké rozpustnosti.[13] Zpracovatelnost lze zlepšit navázáním skupin jako jsou ethery, isopropylideny, hexafluoroisopropylideny nebo karbonyly; tyto skupiny umožňují rotace vazeb kolem aromatických kruhů.[12] Méně symetrické struktury, například obsahující meta- či ortho-vázané monomery, narušují struktury a snižují krystaličnost.[2]
Špatná zpracovatelnost aromatických polymerů také omezuje možnosti jejich výroby a často vyžaduje přidání rozpouštědla, které je silným donorem elektronů, například hexafluorpropan-2-olu nebo triflouoracetonu.
Použití
Následující tabulka znázorňuje podíly hlavních druhů výrobků na celkovém použití polyesterů:
| Druh výrobku | Miliardy USD |
|---|---|
| Textilní vlákna | 86,6[14] |
| Fólie a filmy | 50,0[15] |
| Lahve | 44,0[16] |
| Pryskyřice na laky a vláknové kompozity | 5,5[17] |
| Celkem | 186,0 |
Podrobné údaje k jednotlivým druhům polyesterových výrobků a jejich použití jsou k dosažení ve článcích Polyesterová vlákna, Fólie, Fotografický film, PET láhev, Polyesterové pryskyřice, Lak a Vláknové kompozity.
Výroba
Materiály
Polyethylentereftalát, nejvíce využívaný polyester, se vyrábí z kyseliny tereftalové nebo dimethyltereftalátu, jejího dimethylesteru, a ethylenglykolu. Jeho podíl na obchodu s plasty činí 18 %, což jej řadí na třetí místo po polyethylenu (33,5 %) a polypropylenu (19,5 %).
Důležitost polyethylentereftalátu vyplývá z několika skutečností:
- snadné dostupnosti výchozích látek
- snadné výroby
- nízké toxicity surovin a vedlejších produktů výroby a zpracování
- možnost získávat jej v uzavřeném okruhu za malých emisí do životního prostředí
- velmi dobrých mechanických a chemických vlastností
- recyklovatelnosti a možnosti vytvořit z něj mnoho různých výrobků.
Příprava
Polyestery se připravují polykondenzacemi. Obecná rovnice reakce diolu s dvojsytnou kyselinou vypadá takto:
- (n+1) R(OH)2 + n R'(COOH)2 → HO[ROOCR'COO]nROH + 2n H2O.
Polyestery lze získat mnoha různými reakcemi, nejvýznamnější jsou reakce kyselin s alkoholy, alkoholýzy a/nebo acidolýzy esterů s nízkou molekulovou hmotností, nebo alkoholýzy acylchloridů. Na následujícím obrázku jsou zobrazeny příklady polykondenzací používaných na tvorbu polyesterů; polyestery je také možné vytvořit pomocí otevírání kruhů.
Běžným způsobem provedení polykondenzace je azeotropní esterifikace, kdy se voda vzniklá reakcí alkoholu a karboxylové kyseliny průběžně odstraňuje azeotropní destilací. Pokud jsou teploty tání monomerů dostatečně nízké, tak lze polyester získat přímou esterifikací, kdy se voda odstraňuje podtlakem.
Při průmyslové výrobě alifatických, nenasycených a aromaticko–alifatických polyesterů se používá přímá polyesterifikace za vysokých teplot (150 – 290 °C). Monomery obsahující fenolové terciární alkoholové skupiny špatně reagují s karboxylovými kyselinami a nelze je polymerizovat přímou reakcí alkoholu a kyseliny;[2] přímá výroba PET má ale několik výhod, jako jsou rychlejší průběh reakce, možnost dosáhnout vyšších molekulových hmotností, uvolňování vody namísto methanolu, a nižší náklady na skladování kyseliny oproti esteru.[1]
Transesterifikace
Při transesterifikaci se spojují dva oligomery, kde jeden má na konci řetězce alkoholovou a druhý esterovou skupinu, přičemž se odštěpuje alkohol. Vedlejším produktem je zpravidla methanol.
Pojem transesterifikace se obvykle používá pro reakce hydroxyl–ester, karboxyl–ester a ester–ester; reakce hydroxylů s estery probíhají z těchto nejrychleji a používají se na výrobu řady aromaticko–alifatických a plně aromatických polyesterů.[2] Transesterifikace jsou obzvláště výhodné při použití vysoko tajících a špatně rozpustných dikarboxylových kyselin. Alkoholy jsou navíc těkavější než voda, a tak se i snadněji oddělují.[18]
Plně aromatické polyestery se většinou vyrábějí kondenzacemi diacetátů bisfenolů s aromatickými dikarboxylovými kyselinami nebo bisfenolů s difenylestery aromatických dikarboxylových kyselin (za teplot 220 až 320 °C a odštěpení kyseliny octové), případně z acylchloridů.[2]
Acylace
Při acylacích se používají acylchloridy a místo vody se uvolňuje kyselina chlorovodíková (HCl).
K výrobě polyesterů mohou být použity i reakce diacylchloridů s alkoholy či fenoly.[2][19][20][21] Tyto reakce se provádějí za nižších teplot. Rovnovážné konstanty kondenzací acylchloridů s aryláty byly určeny na 4,7×103 a u polyarylátů na 4,3×103; tento druh reakce se tak často označuje jako „nerovnovážná“ polyesterifikace. Přestože je acylchloridová syntéza předmětem několika patentů, tak její zavedení v průmyslovém měřítku není pravděpodobné.[22] Omezení jsou způsobena nákladností acyldichloridů, jejich náchylností k hydrolýze, a také přítomností vedlejších reakcí.[23]
Reakcemi za vysokých teplot (100 až 300 °C i více) diacylchloridů s dioly se vytváří polyestery a chlorovodík s velkou rychlostí i bez přítomnosti katalyzátorů:[21]
Průběh reakce lze sledovat pomocí titrace vznikajícího chlorovodíku. Jako rozpouštědla lze při reakci použít například chlorované benzeny (například dichlorbenzen), chlorované naftaleny a bifenyly, a nechlorované aromatické sloučeniny, jako jsou terfenyly, benzofenony a dibenzylbenzeny.
Acylacemi lze také vytvořit špatně rozpustné polymery, na jejichž udržení v roztocích jsou třeba vysoké teploty.[23]
Alkohol nebo fenol lze rozpustit ve vodném roztoku hydroxidu sodného za vzniku alkoxidu, přičemž acylchlorid je rozpuštěn v organické sloučenině, která se nemísí s vodou, jako například dichlormethanu, chlorbenzenu nebo hexanu. Reakce poté probíhá rychle i za teplot blízkých pokojové.[21]
Acylacemi se vyrábějí polyaryláty (polyestery založené na bisfenolech), polyamidy, polykarbonáty a polythiokarbonáty. Molekulové hmotnosti produktů vysokoteplotních syntéz bývají omezené vedlejšími reakcemi, čemuž se lze za nižších teplot vyhnout. K látkám vyráběným tímto postupem patří polyaryláty založené na bisfenolu A.[2] Vodu lze někdy nahradit organickým rozpouštědlem, například spojením adiponitrilu a tetrachlormethanu.[21] Využití je omezené u výroby polyesterů založených na alifatických diolech, které mívají vyšší pKa než fenoly a ve vodných roztocích tak nevytvářejí alkoholátové ionty.[2] V jedné fázi lze také uskutečnit zásaditě katalyzované reakce acylchloridů s alkoholy za přítomnosti terciárních aminů, například triethylaminu, nebo pyridinu, které slouží jako akceptory kyseliny:
Acylchloridové polyesterifikace probíhají za pokojové teploty bez přítomnosti katalyzátoru pomalu, aminy je mohou urychlovat několika způsoby, mechanismus není plně znám;[21] terciární aminy ale mohou vyvolávat vedlejší reakce, jako je tvorba ketenů a jejich dimerů.[24]
Silylová metoda
Při silylové metodě acylchlorid reaguje s trimethylsilyletherem odvozeným od alkoholu a vzniká trimethylsilylchlorid.
Acetátová metoda (esterifikace)
Polymerizace s otevíráním kruhu
Alifatické polyestery je možné získat z laktonů, a to za mírných podmínek, přičemž katalyzátory mohou být aniontové, kationtové, organokovové nebo enzymové.[25][26] Jsou rovněž popsány katalytické kopolymerizace epoxidů s cyklickými anhydridy vytvářející funkcionalizované polyestery, ty mohou být nasycené i nenasycené. Průmyslově se využívají i polymerizace s otevíráním kruhu laktonů a laktidů.[27][28]
Ostatní postupy
Některé polyestery lze připravit i jinými postupy, které jsou ale omezeny na laboratorní syntézy za určitých podmínek; jedná se například o reakce solí dikarboxylových kyselin s dialkylhalogenidy nebo bisketenů s dioly.[2]
Místo acylchloridů lze použít sloučeniny označované jako „aktivační činidla“, například karbonyldiimidazol, dicyklohexylkarbodiimid, nebo anhydrid kyseliny trifluoroctové. Polykoindenzace zde probíhá prostřednictvím přeměny karboxylových kyselin na reaktivnější meziprodukty za spotřeby aktivačního činidla. Příkladem může být přeměna N-acylimidazolu za přítomnosti sodného alkoxidu:[2]
Používání aktivačních činidel se zkoumá od 80. let 20. století 1980, reakce ovšem nebyly využity v průmyslu, protože lze podobných výsledků dosáhnout s levnějšími reaktanty.[2]
Termodynamika polykondenzací
Někteří autoři rozdělují polyesterifikace do dvou skupin: na rovnovážné (což jsou většinou reakce alkoholů s kyselinami, alkoholů s estery a kyselin– s estery za vysokých teplot) a nerovnovážné, kde se používají vysoce reaktivní monomery (například acylchloridy či aktivované karboxylové kyseliny, zpravidla v roztocích o nízkých teplotách).[2][19]
Reakce kyselin s alkoholy patří mezi rovnovážné reakce. Poměr množství esterových skupin (-C(O)O-) vytvářejících polymer a vody (H2O) vznikající jako produkt kondenzace oproti kyselině (-C(O)OH) a alkoholu (-OH) lze vyjádřit rovnovážnou konstantou KC:
Rovnovážné konstanty polyesterifikací reakcemi kyselin s alkoholy bývají menší než 10, což nedostačuje k získání polymerů s vysokými molárními hmotnostmi, tedy s průměrnou mírou polymerizace nad 100; průměrnou míru polymerizace (DPn) lze vypočítat z rovnovážné konstanty:[20]
U rovnovážných reakcí je tak nutné průběžně odstraňovat produkt kondenzace, čímž se rovnováha reakce posouvá směrem k polymeru.[20] Produkt kondenzace se odděluje za sníženého tlaku a vysoké teploty (v závislosti na použitém monomeru jde o 150–320 °C), což zabraňuje vedlejším reakcím.[6] S postupem reakce se snižuje koncentrace aktivních konců řetězce a roste viskozita taveniny či roztoku. Rychlost reakce se navyšuje vysokými koncentracemi koncových skupin, k čemuž pomáhají vysoké teploty.
Rovnovážných konstant přesahujících 104 lze dosáhnout pomocí reaktivních výchozích látek (acylchloridů nebo anhydridů) nebo aktivačních činidel, jako je karbonyldiimidazol; poté je možné získat produkty s technicky využitelnými molekulovými hmotnostmi bez odstraňování produktu.
Historie
V roce 1926 zahájil Wallace Carothers výzkum syntetického vlákna, později označovaného nylon.[29] Tento výzkum nebyl zcela dokončen a nedospěl ke zkoumání tvorby polyesteru reakcí ethylenglylolu s kyselinou tereftalovou. První polyester byl patentován roku 1928.[30] Carothersův výzkum obnovil John Rex Whinfield, což vedlo v roce 1941 k patentu na polyethylentereftalát (PET). Polyethylentereftalát je základní látkou pro syntetická polyesterová vlákna, jako jsou Dacron a Terylen. Terve v 70. letech byly vyvinuty analogy PET, které později vedly k vynálezu nenasycených pryskyřic tvrditelných teplem, kopolyesterů z termoplastických elastomerů, kapalných krystalů a v 21. století k vývoji biopolyesterů.[31]
Biologický rozklad a vliv na životní prostředí
Bylo postaveno několik domů z polyesterů vyztužených sklolaminátem, polyurethanem a polymethylmethakrylátem. Jeden z těchto domů byl rozkládán sinicemi a archeami.[32][33]
Síťování
Nenasycené polyestery patří mezi termosety. Obvykle se jedná o kopolymery získávané polymerizací jednoho nebo více diolů s nasycenými a nenasycenými dikarboxylovými kyselinami, například maleinovou a fumarovou, či jejich anhydridy. Dvojné vazby nenasycených polyesterů reagují s vinylovými skupinami monomerů (obvykle styrenu), a vznikají tak trojrozměrné zesíťované struktury, fungující jako termosety. Exotermní zesíťovací reakce jsou spouštěny organickými peroxidy, jako například methylethylketonperoxidem nebo benzoylperoxidem.
Znečištění vod
Skupina vědců z univerzity v Plymouthu 12 měsíců zkoumala osud syntetických materiálů vypláchnutých za různých teplot z domácích praček za použití různých čisticích prostředků, za účelem zjišťování množství uvolněných mikrovláken. Po vyprání 6 kg prádla se průměrně uvolnilo z polyesterovo-bavlněných tkanin 137 951, z polyesterových 496 030 a z akrylových 728 789 vláken.[34][35][36]
Recyklování
Recyklování polymerů nabývá na významu, protože výroba plastů se neustále zvyšuje; předpokládá se, že do roku 2060 by se mohla ztrojnásobit.[37] Plasty lze recyklovat několika způsoby, například mechanicky nebo chemicky. Jedním z nejvíce recyklovaných plastů je PET.[38][39] Esterové vazby v polyesterech je možné hydrolyzovat (v kyselých nebo zásaditých prostředích), methanolyzovat, či glykolyzovat, díky čemuž jsou tyto polymery vhodné pro chemické recyklování.[40]
Enzymová/biologická recyklace PET může být provedena pomocí několika různých enzymů, například PETáz, kutinázy, esteráz či lipáz.[41] PETaázy mohou také rozkládat jiné syntetické polyestery, například polybutylentereftalát, obsahující obdobné esterové vazby.[42]
Odkazy
Reference
V tomto článku byl použit překlad textu z článku Polyester na anglické Wikipedii.
- ↑ a b c d e Köpnick H, Schmidt M, Brügging W, Rüter J, Kaminsky W. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA, June 2000. Kapitola Polyesters.
- ↑ a b c d e f g h i j k l M. E. Rogers, T. E. Long. Synthetic Methods in Step-Growth Polymers. Hoboken, NJ: John Wiley & Sons, 2003.
- ↑ HEFETZ, Abraham; FALES, Henry M.; BATRA, Suzanne W. T. Natural Polyesters: Dufour's Gland Macrocyclic Lactones Form Brood Cell Laminesters in Colletes Bees. Science. 1979, s. 415–417. Dostupné online. doi:10.1126/science.204.4391.415. PMID 17758016. S2CID 41342994. Bibcode 1979Sci...204..415H.
- ↑ Eveleth, R. and D. Chachra. Can Bees Make Tupperware? Scientific American December 19, 2011
- ↑ Kong X., Qi H., Curtis J. M. Synthesis and characterization of high-molecular weight aliphatic polyesters from monomers derived from renewable resources. Journal of Applied Polymer Science. August 2014, s. 40579–40586. doi:10.1002/app.40579.
- ↑ a b Park H. S., Seo J. A., Lee H. Y., Kim H. W., Wall I. B., Gong M. S., Knowles J. C. Synthesis of elastic biodegradable polyesters of ethylene glycol and butylene glycol from sebacic acid. Acta Biomaterialia. August 2012, s. 2911–8. doi:10.1016/j.actbio.2012.04.026. PMID 22522011.
- ↑ Gurunathan T., Mohanty S., Nayak S. K. Hyperbranched polymers for coating applications: a review.. Polymer-Plastics Technology and Engineering. January 2016, s. 92–117. doi:10.1080/03602559.2015.1021482. S2CID 100936296.
- ↑ Testud B., Pintori D., Grau E., Taton D., Cramail H. Hyperbranched polyesters by polycondensation of fatty acid-based AB n-type monomers. Green Chemistry. 2017, s. 259–69. doi:10.1039/C6GC02294D. S2CID 102450135. arXiv 1911.07737.
- ↑ Rosato D. V., Rosato M. V. Plastic product material and process selection handbook. [s.l.]: Elsevier, 2004. Dostupné online. ISBN 978-1-85617-431-2. S. 85.
- ↑ PARKER, David; BUSSINK, Jan; VAN DE GRAMPEL, Hendrik T.; WHEATLEY, Gary W.; DORF, Ernst-Ulrich; OSTLINNING, Edgar; REINKING, Klaus. Ullmann's Encyclopedia of Industrial Chemistry. Polymers, High-Temperature. Redakce Wiley-VCH Verlag GmbH & Co. KGaA. Weinheim, Germany: Wiley-VCH Verlag GmbH & Co. KGaA, 2012-04-15. Dostupné online. ISBN 978-3-527-30673-2. doi:10.1002/14356007.a21_449.pub4. S. a21_449.pub3.
- ↑ H.-G. Elias and R. Mülhaupt, in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH Verlag GmbH & Co. KGaA, Weinheim, Germany, 2015, pp. 1–70
- ↑ a b P. E. Cassidy, T. M. Aminabhavi and V. S. Reddy, in Kirk-Othmer Encyclopedia of Chemical Technology, John Wiley & Sons, Inc., Hoboken, NJ, USA, 2000
- ↑ T. Whelan, Polymer Technology Dictionary, Springer Netherlands, Dordrecht, 1994
- ↑ Polyester [online]. Patagonia, 2024 [cit. 2024-09-25]. Dostupné online. (anglicky)
- ↑ Global Polyester Film Market [online]. Research and Market, 2024 [cit. 2024-09-26]. Dostupné online. (anglicky)
- ↑ PET Bottle Market Report [online]. imarc, 2024 [cit. 2024-09-26]. Dostupné online. (anglicky)
- ↑ Saturated Polyester Resin Market Trends [online]. Grand View Research, 2024 [cit. 2024-09-26]. Dostupné online. (anglicky)
- ↑ Ravve A. Principles of Polymer Chemistry. New York, NY: Springer, 2012.
- ↑ a b S. V. Vinogradova. The basic principles of non-equilibrium polycondensation.. Polymer Science USSR. January 1977, s. 769–808. doi:10.1016/0032-3950(77)90232-5.
- ↑ a b c A. Duda, S. Penczek. Biopolymers Online. Weinheim, Germany: Wiley-VCH Verlag, 2005. doi:10.1002/3527600035.bpol3b12. Kapitola Mechanisms of Aliphatic Polyester Formation, s. 371–383.
- ↑ a b c d e Pilati F. Comprehensive Polymer Science and Supplements. [s.l.]: Elsevier, 1989. Kapitola Polyesters, s. 275–315.
- ↑ K. W. Lienert. Progress in Polyimide Chemistry II. Redakce H. R. Kricheldorf. Berlin, Heidelberg: Springer, 1999. (Advances in Polymer Science; sv. 141). ISBN 978-3-540-64963-2. doi:10.1007/3-540-49814-1_2. Kapitola Poly (ester-imide)s for industrial use., s. 45–82.
- ↑ a b M. Sokolsky-Papkov, R. Langer, A. J. Domb. Synthesis of aliphatic polyesters by polycondensation using inorganic acid as catalyst. Polymers for Advanced Technologies. 2011, s. 502–511. doi:10.1002/pat.1541. PMID 25473252.
- ↑ H. R. Kricheldorf, O. Nuyken, G. Swift. Handbook of Polyermer Synthesis. 2nd. vyd. [s.l.]: CRC Press, 2004. Dostupné online. ISBN 0-367-57822-0. OCLC 1156408945
- ↑ I. K. Varma, A. C. Albertsson, R. Rajkhowa, R. K. Srivastava. Enzyme catalyzed synthesis of polyesters. Progress in Polymer Science. October 2005, s. 949–81. doi:10.1016/j.progpolymsci.2005.06.010.
- ↑ O. Nuyken, S. D. Pask. Ring-Opening Polymerization—An Introductory Review. Polymers. April 2013, s. 361–403. ISSN 2073-4360. doi:10.3390/polym5020361.
- ↑ C. Jérôme, P. Lecomte. Recent advances in the synthesis of aliphatic polyesters by ring-opening polymerization. Advanced Drug Delivery Reviews. June 2008, s. 1056–76. Dostupné online. doi:10.1016/j.addr.2008.02.008. PMID 18403043.
- ↑ O. Dechy-Cabaret, B. Martin-Vaca, D. Bourissou. Controlled ring-opening polymerization of lactide and glycolide. Chemical Reviews. December 2004, s. 6147–76. doi:10.1021/cr040002s. PMID 15584698.
- ↑ How polyester is made - material, manufacture, making, history, used, structure, steps, product, History [online]. [cit. 2018-12-04]. Dostupné online.
- ↑ G. Loasby. The Development of the Synthetic Fibres. Journal of the Textile Institute Proceedings. 1951, s. P411–P441. doi:10.1080/19447015108663852.
- ↑ Tracing the History of Polymeric Materials [online]. 2022-01-03 [cit. 2024-09-26]. Dostupné online. (anglicky)
- ↑ F. Cappitelli, P. Principi, C. Sorlini. Biodeterioration of modern materials in contemporary collections: can biotechnology help?. Trends in Biotechnology. August 2006, s. 350–4. doi:10.1016/j.tibtech.2006.06.001. PMID 16782219.
- ↑ A. Rinaldi. Saving a fragile legacy. Biotechnology and microbiology are increasingly used to preserve and restore the world's cultural heritage. EMBO Reports. November 2006, s. 1075–9. doi:10.1038/sj.embor.7400844. PMID 17077862.
- ↑ M. C. O'Connor. Inside the lonely fight against the biggest environmental problem you've never heard of [online]. 27 October 2014. Dostupné online.
- ↑ WILLIAMS, Alan. Washing clothes releases thousands of microplastic particles into environment, study shows [online]. Plymouth University [cit. 2016-10-09]. Dostupné online.
- ↑ I. E. Napper, R. C. Thompson. Release of synthetic microplastic plastic fibres from domestic washing machines: Effects of fabric type and washing conditions. Marine Pollution Bulletin. November 2016, s. 39–45. doi:10.1016/j.marpolbul.2016.09.025. PMID 27686821.
- ↑ Global plastic waste set to almost triple by 2060, says OECD [online]. [cit. 2022-10-15]. Dostupné online.
- ↑ How to keep a sustainable PET recycling industry in Europe - EPBP - European PET Bottle Platform [online]. [cit. 2022-10-15]. Dostupné online.
- ↑ Which Plastic Can Be Recycled? [online]. [cit. 2022-10-15]. Dostupné online.
- ↑ GHOSAL, Krishanu; NAYAK, Chinmaya. Recent advances in chemical recycling of polyethylene terephthalate waste into value added products for sustainable coating solutions – hope vs. hype. Materials Advances. 2022-02-21, s. 1974–1992. Dostupné online. ISSN 2633-5409. doi:10.1039/D1MA01112J.
- ↑ GHOSAL, Krishanu; NAYAK, Chinmaya. Recent advances in chemical recycling of polyethylene terephthalate waste into value added products for sustainable coating solutions – hope vs . hype. Materials Advances. 2022, s. 1974–1992. Dostupné online. ISSN 2633-5409. doi:10.1039/D1MA01112J.
- ↑ WAGNER-EGEA, Paula; TOSI, Virginia; WANG, Ping; GREY, Carl; ZHANG, Baozhong; LINARES-PASTÉN, Javier A. Assessment of IsPETase-Assisted Depolymerization of Terephthalate Aromatic Polyesters and the Effect of the Thioredoxin Fusion Domain. Applied Sciences. January 2021, s. 8315. ISSN 2076-3417. doi:10.3390/app11188315.
Související články
- Epoxidová pryskyřice
- Polyesterová vlákna
- Glycerinftalát
- PET láhev
- Oligoestery
- Fólie
- Kyselina polymléčná
Externí odkazy
 Obrázky, zvuky či videa k tématu polyestery na Wikimedia Commons
Obrázky, zvuky či videa k tématu polyestery na Wikimedia Commons - Lipázová polyesterifikace
Média použitá na této stránce
Autor: Třídění a recyklace, Licence: CC BY-SA 4.0
PET lahev s neodmímatelným uzávěrem
Autor: Minihaa, Licence: CC0
Overview over some of the most common methods for polyester synthesis.
Autor: Minihaa, Licence: CC0
Synthesis of a polyester using the reactive reagent 1,1′-carbonyldiimidazole carbodiimide.
General synthesis of a polyester via alcoholysis of a low-molecular-weight ester.
Autor: Minihaa, Licence: CC0
Interfacial acyl chloride-based synthesis of a polyester.
Autor: Minihaa, Licence: CC0
Synthesis of a polyester via ring-opening polymerization of a lactone (ε-caprolactone).
Autor: Minihaa, Licence: CC0
Amine-catalysed acyl chloride-based synthesis of a polyester.
Autor: Minihaa, Licence: CC0
General structural formula of a polyester.
Autor: Minihaa, Licence: CC0
General synthesis of a polyester via direct esterification.
Autor: en:User:Pschemp, Licence: CC BY-SA 3.0
Bir polyesterin elektron mikroskobu görüntüsü
Autor: Minihaa, Licence: CC0
Synthesis of a polyester via alcoholysis of an diacyl chloride without a catalyst.
Autor: Antimoni, Licence: CC BY-SA 3.0
washing instructions label for 100% polyester shirt
Autor: Javier Pérez Montes, Licence: CC BY-SA 4.0
Julia, sculpture of Jaume Plensa, located in the Plaza de Colón (Madrid, Spain).
Author: Jaume Plensa (Barcelona, 1955) Title: Julia Year: 2018 Technique: polyester resin and white marble powder Dimensions: 1200 x 367 x 510 cm Category: Patronage project of the María Cristina Masaveu Peterson Foundation
Source: https://www.fundacioncristinamasaveu.com/portfolio/julia/