Polyketidy
Polyketidy jsou rozsáhlou skupinou sekundárních metabolitů, které mohou obsahovat střídající se karbonylové a methylenové skupiny (-CO-CH2-), a nebo být odvozené od prekurzorů s takovými skupinami.[1] Mnoho z nich má lékařské využití nebo je významných v důsledku své akutní toxicity.
- Polyketidy
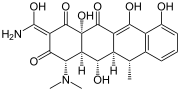
Doxycyklin, další významné antibiotikum.
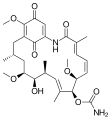
Erythromycin, rovněž antibiotikum.
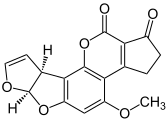
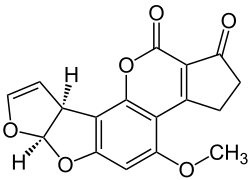
Aflatoxin B1, jedna z nejkarcinogennějších známých sloučenin
Biosyntéza
Polyketidy vznikají v bakteriích, houbách, rostlinách, i některých mořských živočiších. Jejich biosyntéza spočívá v postupné kondenzaci acetylkoenzymu A nebo propionylkoenzymu A s malonyl- či methylmalonylkoenzymem A. Kondenzace bývá doprovázena dekarboxylací a vznikem beta-ketonové funkční skupiny. První kondenzací se vytvoří acetoacetylová skupina, nazývaná diketid. Dalšími kondenzacemi se tvoří triketidy, tetraketidy, atd.[2][3]
Polyketidové řetězce vytvořené polyketidsyntázami mohou mít na sebe napojené téměř jakékoliv substituenty. K modifikacím patří například redukce ketoskupin na methyleny a cyklizace. Řada těchto přeměn probíhá přes enolové tautomery polyketidů.[4]
Polyketidy jsou strukturně rozmanitou skupinou sloučenin.[5]
Lze je rozdělit na tři skupiny: typ I (často jde o makrolidy vytvářené multimodulárními megasyntázami), typ II (mnohdy se jedná o aromatické molekuly vzniklé působením disociovaných enzymů) a typ III (většinou malé aromatické molekuly vznikající v houbách).
Polyketidy jsou vytvářeny multienzymovými polypeptidy připomínajícími eukaryotní syntázy mastných kyselin, které jsou ovšem často mnohem větší. Patří sem acylové přenašečové domény a shluky enzymových jednotek, které mohou fungovat iterativně, přičemž opakují stejné prodlužovací/modifikační kroky (jako při syntéze mastných kyselin), nebo sekvenčně za tvorby heterogennějších polyketidů.[2]
Využití
Na polyketidech jsou založena například některá antibiotika,[6] antimykotika,[7] cytostatika,[8] anticholesteremika,[9] antiparazitika,[7] a přírodní insekticidy.[10]
Příklady
- Makrolidy
- Pikromycin, první izolovaný makrolid[11]
- Antibiotika erythromycin A, klarithromycin a azithromycin
- Anthelmintika avermektin a ivermektin
- Insekticid spinosad (spinosyn)
- Ansamyciny
- Protinádorová léčiva geldanamycin a makbecin,
- Antibiotikum rifamycin
- Polyeny
- Antimykotika amfotericin, nystatin a pimaricin
- Polyethery
- Antibiotikum monensin
- Tetracykliny
- Acetogeniny
- bullatacin
- squamocin
- molvizarin
- uvaricin
- annonacin
- Ostatní
- Imunosupresiva takrolimus (FK506) (imhibitor kalcineurinu) a sirolimus (rapamycin) (inhibitor mTOR)
- Radicikol a pochoninové inhibitory (HSP90)
- Lovastatin, sloužící ke snížení hladiny cholesterolu
- Diskodermolid
- Aflatoxin
- Kyselina usnová
- Anthracimycin
- Anthramycin
Odkazy
Související články
- Esterázy
- Neribozomální peptidy
Externí odkazy
 Obrázky, zvuky či videa k tématu Polyketidy na Wikimedia Commons
Obrázky, zvuky či videa k tématu Polyketidy na Wikimedia Commons
Reference
V tomto článku byl použit překlad textu z článku Polyketide na anglické Wikipedii.
- ↑ The IUPAC Compendium of Chemical Terminology: The Gold Book. Příprava vydání Victor Gold. 4. vyd. Research Triangle Park, NC: International Union of Pure and Applied Chemistry (IUPAC) Dostupné online. DOI 10.1351/goldbook.p04734. (anglicky) DOI: 10.1351/goldbook.
- ↑ a b Donald Voet; Judith G. Voet; Charlotte W. Pratt. Fundamentals of Biochemistry: Life at the Molecular Level. [s.l.]: John Wiley & Sons, 2013. Dostupné online. ISBN 9780470547847. S. 688.
- ↑ James Staunton; Kira J. Weissman. Polyketide Biosynthesis: A Millennium Review. Natural Product Reports. 2001, s. 380–416. DOI 10.1039/a909079g. PMID 11548049.
- ↑ John A. Robinson; Alan Roy Fersht; D. Gani. Polyketide synthase complexes: Their structure and function in antibiotic biosynthesis. Philosophical Transactions of the Royal Society B. 1991, s. 107–114. DOI 10.1098/rstb.1991.0038. PMID 1678529. Bibcode 1991RSPTB.332..107R.
- ↑ Leonard Katz. Manipulation of Modular Polyketide Synthases. Chemical Reviews. 1997, s. 2557–2576. DOI 10.1021/cr960025+. PMID 11851471.
- ↑ 5.13E: Polyketide Antibiotics [online]. 2017-05-09 [cit. 2021-07-05]. Dostupné online.
- ↑ a b Claudia Ross; Viktoria Opel; Kirstin Scherlach; Christian Hertweck. Biosynthesis of antifungal and antibacterial polyketides by Burkholderia gladioli in coculture with Rhizopus microsporus. Mycoses. 2014, s. 48–55. ISSN 1439-0507. DOI 10.1111/myc.12246. PMID 25250879.
- ↑ Lin Jiang; Hong Pu; Jingxi Xiang; Meng Su; Xiaohui Yan; Dong Yang; Xiangcheng Zhu. Huanglongmycin A-C, Cytotoxic Polyketides Biosynthesized by a Putative Type II Polyketide Synthase From Streptomyces sp. CB09001. Frontiers in Chemistry. 2018, s. 254. ISSN 2296-2646. DOI 10.3389/fchem.2018.00254. PMID 30013965. Bibcode 2018FrCh....6..254J.
- ↑ Yolande A. Chan; Angela M. Podevels; Brian M. Kevany; Michael G. Thomas. Biosynthesis of polyketide synthase extender units. Natural Product Reports. 2009, s. 90–114. ISSN 0265-0568. DOI 10.1039/b801658p. PMID 19374124.
- ↑ Hak Joong Kim; Sei-hyun Choi; Byung-sun Jeon; Namho Kim; Rongson Pongdee; Qingquan Wu; Hung-wen Liu. Chemoenzymatic synthesis of spinosyn A. Angewandte Chemie International Edition. 2014-12-01, s. 13 553 – 13 557. ISSN 1521-3773. DOI 10.1002/anie.201407806. PMID 25287333.
- ↑ Hans Brockmann; WILLFRIED HENKEL. Pikromycin, ein bitter schmeckendes Antibioticum aus Actinomyceten. Chemische Berichte. 1951, s. 284–288. DOI 10.1002/cber.19510840306. (anglicky)
Média použitá na této stránce
Structure of Doxycycline (created with BKchem)
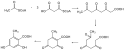
biosynthesis of orsellinic acid
Erythromycin A
(–)-Aflatoxin_B1_Structural_Formulae Aflatoxin_B1
Chemical structure of geldanamycin.