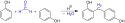Polykondenzace

Polykondenzace je společně s polyadicí jeden z typů stupňovité polymerace – reakce syntetických makromolekulárních látek. V průběhu reakce nevzniká jenom polymer, ale i nízkomolekulární produkt (např. voda, methanol, amoniak).
Nejde o polymerizaci řetězovou, ale o pozvolnější stupňovitou. Ze dvou monomerů vznikne dimer, dále trimer a postupně až polymer. Postupně tedy kondenzují monomery, oligomery a nakonec vznikají polymery (polykondenzáty).
Pokud monomer nese dvě funkční skupiny, vzniká lineární polymer, pokud nese více funkčních skupin, vzniká trojrozměrný polymer. Reaktivita funkčních skupin je v podstatě nezávislá na délce řetězce, na němž jsou umístěny.
Polykondenzace byla pro výrobu poprvé použita v roce 1909, kdy byl kondenzací fenolu s formaldehydem vyroben polymer, který dnes známe pod názvem bakelit. Dnes se polykondenzací vyrábějí polyamidy (nylon, silon), polyestery (tesil), polykarbonáty (makrolon), polyfenoly (bakelit), polyimidy (kapton) nebo silikony. Jako polykondenzaci můžeme klasifikovat i přírodní syntézu bílkovin z aminokyselin.[1]
Průběh polykondenzace
Polymerace probíhá ve třech fázích:
- iniciace, aktivace monomeru přivedením energie potřebné k rozštěpení dvojných nebo trojných vazeb, otevírání těchto vícenásobných vazeb uhlíku.
- propagace, lavinovitý růst řetězec s uvolňováním reakčního tepla, které musí být odváděno.
- terminace, dosažení rovnováhy a ukončení růstu řetězce.
Schéma polykondenzace
aAa + bBb → aABb + ab
aAa + aABb → aABAa + ab
bBb + aABb → bBABb + ab .....,
kde
- aAa, bBb jsou monomery s funkčními skupina a, b
- ab je vedlejší produkt
Ze schématu plyne, že u polykondenzačních reakcí probíhají náhodné reakce mezi všemi počátečními monomery a jejich následnými meziprodukty. Po krátké době zreaguje většina monomerů na polymery o nízkém polymeračním stupni. Vyššího polymeračního stupně lze dosáhnout prodloužením doby polykondenzace nebo odstraňováním vedlejšího produktu.
Příklady polykondenzace
Vznik polyamidu

Reakce kyseliny dikarboxylové s diaminem za vzniku polyamidu a uvolnění vody.[2]
Vznik polyfenolu

Reakce formaldehydu se dvěma fenoly za vzniku difenolu a vody.

Polykondenzace formaldehydu s difenolem a fenolem na polyfenol za uvolnění vody.
Vznik polyesteru

Polykondenzace ethandiolu s karboxylovou kyselinou na polyester za uvolnění vody.
Reference
V tomto článku byly použity překlady textů z článků Condensation polymer na anglické Wikipedii a Polykondensation na německé Wikipedii.
- ↑ LECHNER, M. D. Makromolekulare Chemie : ein Lehrbuch für Chemiker, Physiker, Materialwissenschaftler und Verfahrenstechniker. 4. vyd. Basel: Birkhäuser, 2010. 536 s. Dostupné online. ISBN 978-3-7643-8891-1, ISBN 3-7643-8891-9. OCLC 647854377 S. 119–136. (německy)
- ↑ WOLLRAB, Adalbert. Organische Chemie eine Einführung für Lehramts- und Nebenfachstudenten. 2. vyd. Berlin: Springer-Verlag, 1999. 979 s. Dostupné online. ISBN 978-3-540-43998-1, ISBN 3-540-43998-6. OCLC 50977585 S. 527. (německy)
Externí odkazy
 Obrázky, zvuky či videa k tématu polykondenzace na Wikimedia Commons
Obrázky, zvuky či videa k tématu polykondenzace na Wikimedia Commons
Média použitá na této stránce
Structure of the condensation polymerization between Formaldehyde and Phenole to Bakelite
Reaction scheme of the condensation polymerization of dicarboxylic acid and diamine.
Structure of the condensation polymerization between Formaldehyde and Phenole to Bakelite
Structure of the condensation Polymerization to Polyester