Uhličitan draselný
| Uhličitan draselný | |
|---|---|
 | |
 | |
| Obecné | |
| Systematický název | Uhličitan draselný |
| Triviální název | potaš |
| Anglický název | Potassium carbonate |
| Německý název | Kaliumcarbonat |
| Sumární vzorec | K2CO3 |
| Vzhled | bílá hygroskopická krystalická nebo práškovitá látka |
| Identifikace | |
| Registrační číslo CAS | 584-08-7 |
| PubChem | 516886 |
| Číslo RTECS | TS7750000 |
| Vlastnosti | |
| Molární hmotnost | 138,205 g/mol 165,228 g/mol (seskvihydrát) |
| Molární koncentrace cM | 5,573 mol/dm3 (50% roztok) |
| Teplota tání | 891 °C |
| Hustota | 2,428 g/cm3 (19 °C) 2,155 g/cm3 (seskvihydrát, 19 °C) 1,540 4 g/cm3 (50% roztok) |
| Dynamický viskozitní koeficient | 3,03 cP (917 °C) 1,66 cP (977 °C) 6,071 cP (50% roztok, 20 °C) |
| Kinematický viskozitní koeficient | 3,941 cS (50 roztok, 20 °C) |
| Index lomu | nD= 1,531 seskvihydrát nDa= 1,380 nDb= 1,432 nDc= 1,573 50% roztok nD= 1,416 8 |
| Rozpustnost ve vodě | 105,5 g/100 g (0 °C) 108,2 g/100 g (10 °C) 110,5 g/100 g (20 °C) 112,3 g/100 g (25 °C) 113,7 g/100 g (30 °C) 116,9 g/100 g (40 °C) 126,8 g/100 g (60 °C) 139,2 g/100 g (80 °C) 155,7 g/100 g (100 °C) 274 g/100 g (200 °C) seskvihydrát 158,49 g/100 g (0 °C) 167,25 g/100 g (20 °C) 181,84 g/100 g (40 °C) 202,67 g/100 g (60 °C) 230,90 g/100 g (80 °C) 268,60 g/100 g (100 °C) |
| Rozpustnost v polárních rozpouštědlech | ethanol (ne) aceton (ne) |
| Relativní permitivita εr | 5,66 (18 °C) |
| Měrná magnetická susceptibilita | −6,12×10−6 cm3 g−1 |
| Povrchové napětí | 168,4 mN/m (910 °C) 162,1 mN/m (1 010 °C) |
| Struktura | |
| Krystalová struktura | jednoklonná jednoklonná (seskvihydrát) |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −1 151,0 kJ/mol |
| Entalpie tání ΔHt | 236 J/g |
| Entalpie rozpouštění ΔHrozp | −199 J/g (18 °C) |
| Standardní molární entropie S° | 155,5 JK−1mol−1 |
| Standardní slučovací Gibbsova energie ΔGf° | −1 063,6 kJ/mol |
| Izobarické měrné teplo cp | 0,828 J K−1 g−1 |
| Bezpečnost | |
| [1] Varování[1] | |
| R-věty | R22, R36, R37, R38 |
| S-věty | S22, S26 |
| NFPA 704 | |
Některá data mohou pocházet z datové položky. | |
Uhličitan draselný K2CO3, starším názvem potaš, salajka či draslo (od toho slovo draslík), je bílá, silně hygroskopická sůl kyseliny uhličité. Vodné roztoky jsou silně alkalické. Používá se převážně při výrobě skla, v textilním a papírenském průmyslu, při výrobě mazlavých mýdel, je součástí pracích prášků, při výrobě pigmentů, v barvířství a běličství a při praní vlny, při výrobě léků, v analytické chemii a mnohde jinde. V potravinářství se přidává pod označením E501 z důvodu emulgace a kypření, stabilizace sušeného ovoce, nebo snížení kyselosti kakaového prášku.[2] Používá se také pro přípravu kyanidu draselného a také se používá ve vodních hasicích přístrojích.
Výroba
Nejprve se provede elektrolýza roztoku chloridu draselného za vzniku hydroxidu draselného, vodíku a chloru. Vzniklý hydroxid draselný se pak sytí oxidem uhličitým. Při reakci hydroxidu draselného a oxidu uhličitého vzniká uhličitan draselný.
- 2 KOH + CO2 → K2CO3 + H2O
Ten je pak výchozí látkou pro další sloučeniny draslíku.
Postupy získávání potaše
Historické postupy získávání potaše
Primitivně (od středověku) se potaš získávala spalováním celých stromů „na stojato“. Tzv. popeláři do kmene javorů nebo jiných dřevin vyhloubili otvor, ve kterém udržovali oheň. Strom pomalu vyhořel, aniž by došlo k ohrožení okolního lesa. Popelaření se provádělo pouze za stálého počasí, protože potaš nesměla zmoknout.
Označení potaš pochází ze způsobu jeho získávání: pot ash, tedy popel v hrnci.[V 1] Surové draslo je totiž rozpustné ve vodě, podobně jako soda nebo sůl, které jsou příbuzné.
Tradiční technologie výroby spočívala v loužení dřevěného popela vodou a odpaření přefiltrované louženiny na tzv. surovou potaš neboli flus. Ten již bylo možné užít jako surovinu v některých průmyslových odvětvích. Vyžíháním – kalcinací flusu bylo získáváno čistší kalcinované draslo. Surovinou pro výrobu potaše byl tedy původně dřevěný popel, zprvu speciálně pálený z tvrdého dřeva (javor klen, bříza, buk[4]) v lesích, později (po vydání Lesního řádu v roce 1754) získávaný z dřevního odpadu nebo z popela zbylého po topení v domácnostech. Náhražkově se také využívalo jiného organického materiálu (sláma…).
Užívaná technologie se od 16. do 19. století téměř neměnila a byla v této formě rozšířená prakticky po celém světě.[5]
Suchá těžba
Potaš sice lze přímo těžit, jako minerál, protože je však lehčí než ostatní horniny nad ložiskem, tedy se tlačí vzhůru (Paradox Formation[V 2]), a pro své adsorpční vlastnosti, zachytává v sobě jiné látky a vytváří kapsy: ropy a zemního plynu. Například na velkém nalezišti v Utažské poušti v USA v roce 1963 došlo proražením kapsy plynu k tragické explozi.[V 3]
Současné postupy získávání potaše
Dnes se potaš získává loužením země vodou, kdy se do podzemních ložisek pumpuje voda, která pak druhým vrtem zas tryská ven: již obohacená o rozpuštěné látky z podzemí. Ze solanky se na slunci měsíce nechává odpařovat voda,[V 4] výsledná směs solí se sbírá k dalšímu zpracování.[V 5]
Odkazy
K videu Veritasium o nalezišti Paradox Formation v Utahu
- ↑ Veritasium, čas videa: 2m 12s - pot ash, tedy popel v hrnci.[3]
- ↑ Veritasium, čas videa: 3m 15s - Ložisko se horninami tlačí vzhůru, vytváří kapsy plynu.[3]
- ↑ Veritasium, čas videa: 3m 55s - Paradox Formation na velkém nalezišti v Utažské poušti v USA, v roce 1963 tu došlo k tragické explozi.[3]
- ↑ Veritasium, čas videa: 5m 20s - Potaš se získává loužením země vodou, ta se pak sluncem odpařuje celé měsíce.[3]
- ↑ Veritasium, čas videa: 4m 07s - Loužení je bezpečnější způsob těžby.[3]
Reference
- ↑ a b Potassium carbonate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ E501 - Uhličitany draselné [online]. FÉR potravina [cit. 2020-07-08]. Dostupné online.
- ↑ a b c d e Exploring One Of The Most Mysterious Places; Veritasium. Video online. Zveřejněno 7. srpna 2021. Navštíveno 2021-09-19. (anglicky)
- ↑ http://lesuzdar.lesycr.cz/cs/download/starsi-cisla-v-pdf/2009/lesu-zdar-pdf-unor-2009.pdf
- ↑ http://www.keramika-sklo.cz/zobraz.php?searchtext=grafick%E9ho[nedostupný zdroj]
Literatura
- WOITSCH, JIŘÍ. Zapomenutá potaš : drasláři a draslářství v 18. a 19. století. Praha : Etnologický ústav Akademie věd České republiky, 2003. ISBN 80-85010-53-4.
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.
Externí odkazy
 Obrázky, zvuky či videa k tématu uhličitan draselný na Wikimedia Commons
Obrázky, zvuky či videa k tématu uhličitan draselný na Wikimedia Commons
Média použitá na této stránce
Globally Harmonized System of Classification and Labelling of Chemicals (GHS) pictogram for hazardous substances
The "fire diamond" as defined by NFPA 704. It is a blank template, so as to facilitate populating it using CSS.
Uhličitan draselný - K2CO3
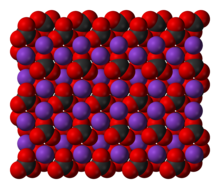
Space-filling model of part of the crystal structure of potassium carbonate, K2CO3.
X-ray crystallographic data from Y. Idemoto, J. W. Richardson Jr., N. Koura, S. Kohara, C.-K. Loong (March 1998). "Crystal structure of (LixK1−x)2CO3 (x = 0, 0.43, 0.5, 0.62, 1) by neutron powder diffraction analysis". J. Phys. Chem. Solids 59 (3): 363-376. DOI:10.1016/S0022-3697(97)00209-6..
Model constructed in CrystalMaker 8.1.
Image generated in Accelrys DS Visualizer.K2CO3






